Содержание
- 3. АМФОТЕРНОСТЬ способность некоторых соединений проявлять в зависимости от условий как кислотные, так и основные свойства. 1814
- 5. они взаимодействуют с кислотами и щелочами. https://youtu.be/7rJj3WTk9Vw Изучаем химию: Амфотерность
- 6. КИСЛОТНЫЕ СВОЙСТВА Амфотерные соединения взаимодействуя с основаниями, ведут себя как кислоты. 2KOH(тв.) + H2ZnO2(тв.) = K2ZnO2
- 8. http://himija8en.blogspot.ru/p/blog-page_23.html Be(OH)2(тв.) +2NaOH(тв.) =Na2BeO2 + 2H2O (метабериллат натрия, или бериллат) Pb(OH)2(тв.) +2NaOH(тв.) = Na2PbO2 + 2H2O
- 9. образуются комплексные соединения: Al(OH)3 + KOH → K[Al(OH)4] (тетрагидроксоалюминат калия); Al(OH)3 + 3KOH → K3[Al(OH)6] (гексагидроксоалюминат
- 10. Амфотерные органические
- 11. Цвиттер-ион (биполярный ион— гибрид) — электронейтральная молекула, которая в своей структуре имеет части с отрицательным и
- 12. Амфотерность аминокислот
- 13. Осуществить превращение, написать электронный баланс, в молекулярно-ионном виде
- 14. Al → А12O3 →AlCl3 → Al(OH)3 → NaAlO2
- 16. Скачать презентацию







![образуются комплексные соединения: Al(OH)3 + KOH → K[Al(OH)4] (тетрагидроксоалюминат калия); Al(OH)3 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/894129/slide-8.jpg)





 Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Смог як хімічне явище
Смог як хімічне явище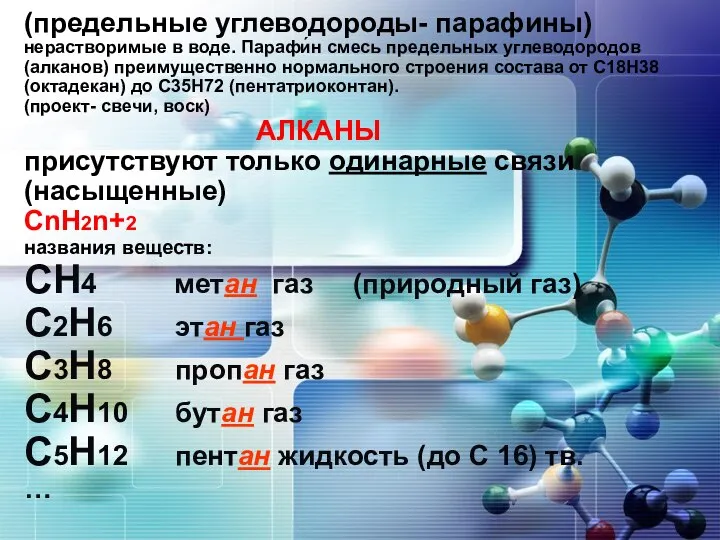 Углеводороды
Углеводороды Алкины. Строение
Алкины. Строение Классификация оксидов по химическим свойствам
Классификация оксидов по химическим свойствам Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Оксиген та кисень
Оксиген та кисень Анализ свойств карбамидоформальдегидных смол
Анализ свойств карбамидоформальдегидных смол Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Вода. Физические и химические свойства
Вода. Физические и химические свойства Белки-1 2020
Белки-1 2020 Производство полимеров в РК
Производство полимеров в РК Альдегиды. Строение молекулы альдегида. Номенклатура и изомерия
Альдегиды. Строение молекулы альдегида. Номенклатура и изомерия Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Оксиды
Оксиды Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Белки
Белки Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера
Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера Углеводы. Общее понятие углеводов
Углеводы. Общее понятие углеводов Применения химического анализа людьми в разных родах занятий
Применения химического анализа людьми в разных родах занятий Пниктогены р-элементы V группы; VA группа; 15 группа
Пниктогены р-элементы V группы; VA группа; 15 группа Материалы, изменившие мир
Материалы, изменившие мир Скорость химической реакции. Химическое равновесие
Скорость химической реакции. Химическое равновесие Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Шаблон для презентации по химии
Шаблон для презентации по химии Альдегиды и кетоны
Альдегиды и кетоны Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов
Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов Молекула воды, какая ты?
Молекула воды, какая ты?