Содержание
- 2. Цели урока: 1)Познакомить учащихся с понятием ионные уравнения и ионные реакции; 2)рассмотреть случаи, при которых реакции
- 3. Ионы Большинство химических реакций протекает в растворах. Растворы электролитов содержат ионы. Ионы – это положительно или
- 4. . Ионные реакции – это реакции между ионами. Ионные уравнения – это уравнения ионных реакций. Например:
- 5. . Реакции ионного обмена записывают тремя уравнениями: молекулярное полное ионное уравнение сокращенное ионное уравнение
- 6. . Реакции ионного обмена протекают до конца в тех случаях, когда образуется ОСАДОК (МАЛОРАСТВОРИМОЕ ВЕЩЕСТВО) ГАЗ
- 7. Реакции ионного обмена, идущие с выделением осадка
- 8. Реакции ионного обмена, идущие с выделением газа
- 10. . Реакции нейтрализации – реакция взаимодействия сильной кислоты с щелочью. Это частный случай реакции обмена. Например:
- 11. Домашнее задание: § 38, упр. 1,2.
- 12. Решение ионных уравнений. 14.04.2021.
- 13. Если врезультате реакции выделяется малодиссоциирующее (мд) вещество – вода KOH + HCl → KCl + H2O
- 14. Если врезультате реакции выделяется нерастворимое в воде вещество CuCl2 + KOH→KCl+ Cu(OH)2↓ Al2(SO4)3 + BaCl2 →
- 15. Если врезультате реакции выделяется газообразное вещество K2S + HCl → KCl + H2S↑ Na2CO3 + HNO3
- 16. Домашнее задание: §38, упр.3; подготовиться к проверочной работе
- 17. Обобщение темы Тест «Проверь себя»: 1) Ионные реакции – это реакции между: а) нейтральными атомами б)
- 18. . 4) Какое вещество надо добавить к соляной кислоте, чтобы в результате реакции выделился газ: а)
- 19. Ответы: 1. б 2. а 3. а 4. в 5. г
- 21. Скачать презентацию


















 Дивный мир турмалинов
Дивный мир турмалинов Коррозия металлов
Коррозия металлов Химическая лаборатория
Химическая лаборатория Биогаз. Технология производства
Биогаз. Технология производства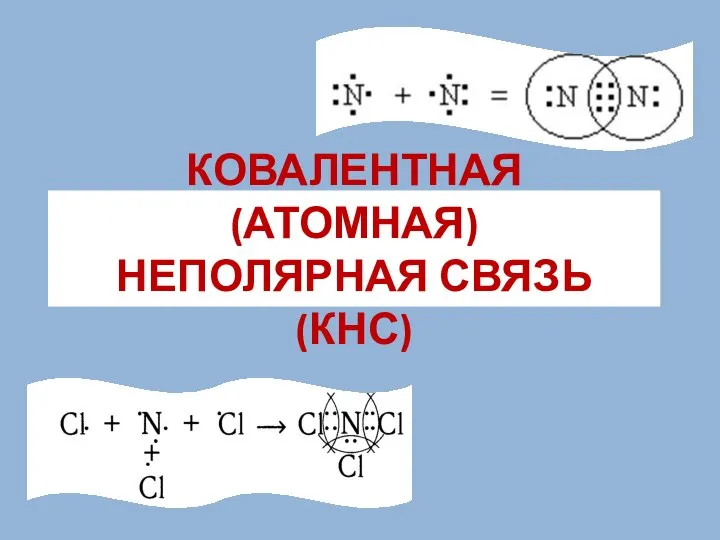 676a1c5e85f2455c9a6d495b8a94b9f9
676a1c5e85f2455c9a6d495b8a94b9f9 ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области
ФБОУ- Раздольненская средняя общеобразовательная школа №19 Новосибирского района Новосибирской области Материаловедение
Материаловедение Карбоновые кислоты. Сложные эфиры. Жиры
Карбоновые кислоты. Сложные эфиры. Жиры Пространственное строение органических соединений
Пространственное строение органических соединений Оксиды. Кварц (SiO2). Корунд (Al2O3)
Оксиды. Кварц (SiO2). Корунд (Al2O3) Bool-doser team
Bool-doser team Дифференциальный термический анализ
Дифференциальный термический анализ Неметалічні елементи
Неметалічні елементи Органическая химия
Органическая химия Углеводороды (УВ)
Углеводороды (УВ) Получение металлов
Получение металлов Study of short peptide adsorption on solution dispersed. Inorganic nanoparticles using depletion method
Study of short peptide adsorption on solution dispersed. Inorganic nanoparticles using depletion method Основы квантовой химии
Основы квантовой химии Презентация на тему Жиры (9 класс)
Презентация на тему Жиры (9 класс)  Теория электролитической диссоциации. Контрольный тест
Теория электролитической диссоциации. Контрольный тест Химия вокруг нас
Химия вокруг нас Определение количества этилендиамина в соединении [Gd(en)x][Fe(CN)6]
Определение количества этилендиамина в соединении [Gd(en)x][Fe(CN)6] Алкины
Алкины Основные сведения о металлах и сплавах и их свойства
Основные сведения о металлах и сплавах и их свойства Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Аминокислоты. Белки. Лекция 2
Аминокислоты. Белки. Лекция 2 Гидролиз солей
Гидролиз солей Презентация на тему Химия вокруг нас
Презентация на тему Химия вокруг нас