Содержание
- 2. « Спирты »
- 3. Цели урока: 1) рассмотреть строение и свойства многоатомных спиртов, максимально используя имеющиеся знания о составе, строении
- 4. Устный опрос : Какие вещества называются спиртами?
- 5. Как классифицируют спирты по числу ОН-групп, и по Rad?
- 6. Классификация спиртов
- 7. Работа на местах Написать формулу: 2-метилбутанол 2-метил-пентанол-3 Осуществить превращение: C2 H6 → C2 H4 → C2
- 8. Дать название следующим веществам: CH2—CH—CH2—CH2 — CH2—CH2—OH I CH3 CH3 ⏐ OH--- CH 2—C--- CH3 ⏐
- 9. МОТИВАЦИЯ к восприятию нового материала: Что мы знаем о многоатомных спиртах? Используем ли их в повседневной
- 10. Многоатомные спирты – это органические соединения, в молекулах которых содержатся две или более гидроксильных групп, соединенных
- 12. Названия спиртов Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три-, ...) указывается количество гидроксильных групп.
- 13. Многоатомный спирт -этиленгликоль Этиленгликоль — представитель предельных двухатомных спиртов — гликолей. Название гликоли получили вследствие сладкого
- 14. Многоатомный спирт - глицерин Глицерин – трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая на вкус жидкость.
- 16. Качественной реакцией на многоатомные спирты является их взаимодействие со свежеполученным осадком гидроксида меди( II), который растворяется
- 17. Применение этиленгликоля Важным свойством этиленгликоля является способность понижать температуру замерзания воды, от чего вещество нашло широкое
- 18. Этиленгликоль – яд ! Дозы вызывающие смертельное отравление этиленгликолем варьируются в широких пределах - от 100
- 19. Применение глицерина В производстве взрывчатых веществ, в частности тринитрата глицерина. При обработке кожи, для предотвращения от
- 21. Скачать презентацию


















 смеси
смеси Уравнения диссоциации
Уравнения диссоциации Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Цитология
Цитология Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb
Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb Применение брома
Применение брома Производство органических препаратов ароматического ряда
Производство органических препаратов ароматического ряда Металлы. Группы металлов
Металлы. Группы металлов Реакции ионного обмена
Реакции ионного обмена Неорганическая химия 1 семестра. Растворы
Неорганическая химия 1 семестра. Растворы Теория радиационной деформации в некубических металлах: явление анизотропной диффузии
Теория радиационной деформации в некубических металлах: явление анизотропной диффузии Электролиз
Электролиз Многоядерные Арены
Многоядерные Арены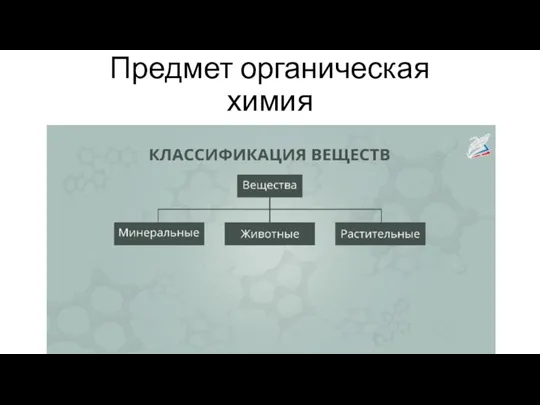 Органическая химия
Органическая химия Фосфор туралы
Фосфор туралы Типы химических реакций. Класс оксиды
Типы химических реакций. Класс оксиды Влияние давления на скорость химических реакций с участием газов
Влияние давления на скорость химических реакций с участием газов Хром
Хром Ионообменная хроматография в разделении белков
Ионообменная хроматография в разделении белков Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Метаболизм триацилглицеринов
Метаболизм триацилглицеринов Витамины. Классификация витаминов
Витамины. Классификация витаминов Комплексные соединения
Комплексные соединения Мифы и реальность о суперклее
Мифы и реальность о суперклее Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Амины. Номенклатура
Амины. Номенклатура Теория электролитической диссоциации. Контрольный тест
Теория электролитической диссоциации. Контрольный тест Физика полимеров Ч1
Физика полимеров Ч1