Содержание
- 2. Едва ли найдётся другое, искусственно добываемое, вещество, столь часто применяемое в технике, как серная кислота. Там,
- 3. Реакции разбавленной серной кислоты с активными металлами 2Li + H2 SO4 = Li2SO4 + H2 ↑
- 4. Реакции разбавленной серной кислоты с металлами средней активности Zn + H2SO4 = ZnSO4 + H2 ↑
- 5. Реакции разбавленной серной кислоты с алюминием и железом 2Al + 3H2 SO4 = Al2(SO4)3+3H2 ↑ Al0
- 6. Реакции разбавленной серной кислоты с малоактивными металлами Cu + H2SO4 - не взаимодействует
- 7. Реакции концентрированной серной кислоты с активными металлами 8Na + 5H2 SO4 (k) = H2S + 4Na2SO4
- 8. Реакции концентрированной серной кислоты с металлами средней активности Zn + 2H2 SO4 = ZnSO4 + 2H2O
- 9. Реакции концентрированной серной кислоты с алюминием и железом На холоде концентрированная серная кислота пассивирует многие металлы,
- 10. Реакции концентрированной серной кислоты с малоактивными металлами Cu + 2H2 SO4 = CuSO4 + 2H2O +
- 11. Реакции концентрированной серной кислоты с неметаллами S + 2H2 SO4 = 2H2O + 3SO2 S 0
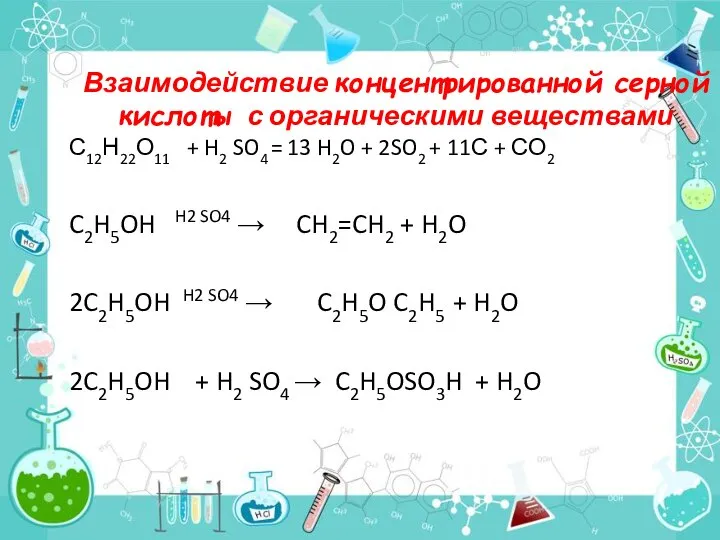
- 12. Взаимодействие концентрированной серной кислоты с органическими веществами С12Н22О11 + H2 SO4 = 13 H2O + 2SO2
- 14. Скачать презентацию










 Поверхность потенциальной энергии и расчет сил, действующих на ионы
Поверхность потенциальной энергии и расчет сил, действующих на ионы Ковалентная химическая связь
Ковалентная химическая связь Нафтены и арены
Нафтены и арены Кремний и его соединения
Кремний и его соединения Коррозионно-активное воздействие на РЭС. Оценка коррозионной стойкости. Лекция №11
Коррозионно-активное воздействие на РЭС. Оценка коррозионной стойкости. Лекция №11 Презентация для заочников
Презентация для заочников Ацилирование. Лекция 4
Ацилирование. Лекция 4 Любовь и химия
Любовь и химия Պոլիմերներ
Պոլիմերներ Нефть и способы её переработки
Нефть и способы её переработки Растворимость веществ. Кристаллогидраты
Растворимость веществ. Кристаллогидраты Эффект растворителя при определении пространственной структуры сложных гетероциклических соединений
Эффект растворителя при определении пространственной структуры сложных гетероциклических соединений Химическая связь 8 класс - Презентация_
Химическая связь 8 класс - Презентация_ Взаимодействие карбонатов с разбавленными кислотами
Взаимодействие карбонатов с разбавленными кислотами Кинетика химических реакций
Кинетика химических реакций Вода - это жизнь
Вода - это жизнь Химия 11 класс
Химия 11 класс Презентация на тему Ионы и ионная химическая связь
Презентация на тему Ионы и ионная химическая связь  Металлы
Металлы Предмет органической химии. Строение атома углерода
Предмет органической химии. Строение атома углерода Выберите вещества
Выберите вещества Алкины. Строение алкинов
Алкины. Строение алкинов Энергетический обмен
Энергетический обмен alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1
alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1 Углеводы. Дисахариды. Полисахариды. Лекция 6
Углеводы. Дисахариды. Полисахариды. Лекция 6 Подготовка к итоговой контрольной работе
Подготовка к итоговой контрольной работе Вермикулит. Технические характеристики
Вермикулит. Технические характеристики Стекло. Определение стекла
Стекло. Определение стекла