Содержание
- 2. Физические свойства При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха.
- 3. Разбавленная серная кислота обладает общими свойствами, характерными для всех кислот.
- 4. Водный раствор изменяет окраску индикаторов : - лакмус - красный, - метилоранж - красный, - фенолфталеин
- 5. Разбавленная серная кислота реагирует с металлами, стоящими в ряду активности металлов до водорода: H2SO4+Zn=ZnSO4+H2
- 6. Реагирует с основными и амфотерными оксидами: H2SO4+MgO=MgSO4+H2O H2SO4 +ZnO=ZnSO4+H2O
- 7. Взаимодействует с основаниями: H2SO4+2KOH=K2SO4+2H2O
- 8. Если кислота взята в избытке, то образуется кислая соль: H2SO4+NaOH=NaHSO4+H2O
- 9. Реагирует с солями, вытесняя из них другие кислоты: H2SO4+Na2CO3 =Na2SO4+H2O +CO2
- 10. Свойства концентрированной серной кислоты
- 11. Концентрированная серная кислота энергично реагирует с водой с образованием гидратов: H2SO4+nH2O=H2SO4·nH2O+Q
- 12. -при нагревании она реагирует со всеми металлами ( исключение Au, Pt и нек. др.). В этих
- 13. Взаимодействие концентрированной серной кислоты с металлами: H2SO4 + МЕ0 = соль-сульфат + H2O + ? Ряд
- 14. Характерной реакцией на серную кислоту и её соли является взаимодействие с растворимыми солями бария: H2SO4+BaCl2=BaSO4↓+2HCl Выпадает
- 15. Применение серной кислоты в производстве минеральных удобрений; как электролит в свинцовых аккумуляторах; для получения различных минеральных
- 17. Скачать презентацию














 Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Химия и сельское хозяйство Пестициды
Презентация на тему Химия и сельское хозяйство Пестициды  Высокоэффективная жидкостная препаративная хроиматография
Высокоэффективная жидкостная препаративная хроиматография Строение и свойства предельных и непредельных углеводородов. . Обобщающий урок по химии 10 класс
Строение и свойства предельных и непредельных углеводородов. . Обобщающий урок по химии 10 класс Химическая реакция
Химическая реакция Качественные реакции в химии
Качественные реакции в химии Вермикулитовый концентрат
Вермикулитовый концентрат Физические свойства металлов
Физические свойства металлов Эмульсии
Эмульсии Презентация на тему Основные законы науки химии
Презентация на тему Основные законы науки химии  Активные формы кислорода (АФК) Reactive Oxygen Species (ROS)
Активные формы кислорода (АФК) Reactive Oxygen Species (ROS) Классификация органических веществ
Классификация органических веществ Презентация на тему Коррозия металлов (11 класс)
Презентация на тему Коррозия металлов (11 класс)  Составитель: Денисова В.Г.
Составитель: Денисова В.Г. Основные положения МКТ
Основные положения МКТ Сравнение свойств неорганических и органических веществ
Сравнение свойств неорганических и органических веществ Якісні реакції органічних речовин
Якісні реакції органічних речовин Номенклатура органических веществ
Номенклатура органических веществ Расчет псевдокритических свойств конденсатного газа и пластовых газоконденсатных жидкостей. Анализ рекомбинированных проб
Расчет псевдокритических свойств конденсатного газа и пластовых газоконденсатных жидкостей. Анализ рекомбинированных проб Производство чугуна и стали
Производство чугуна и стали Амилаза. Строение амилазы
Амилаза. Строение амилазы Поделочный камень родонит
Поделочный камень родонит Чистые вещества и смеси
Чистые вещества и смеси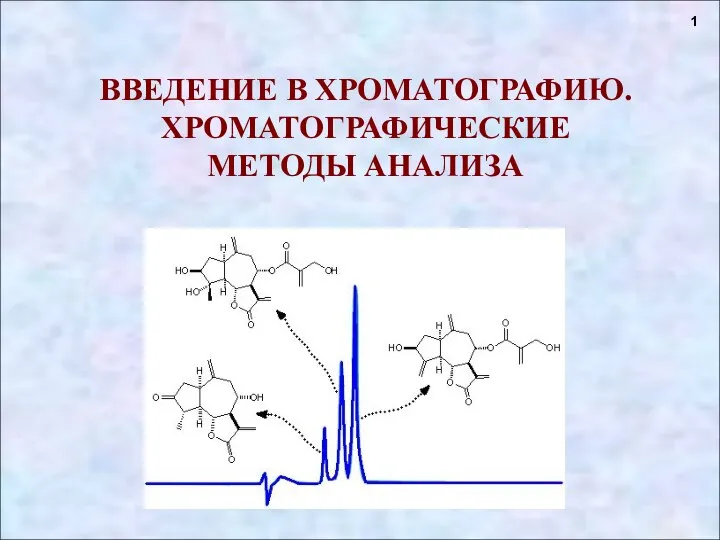 Введение в хроматографию. Хроматографические методы анализа
Введение в хроматографию. Хроматографические методы анализа Основания, их состав и название
Основания, их состав и название Сераорганические соединения
Сераорганические соединения Углеводороды. Алкены, этилен
Углеводороды. Алкены, этилен Физические и химические свойства воды
Физические и химические свойства воды