Содержание
- 2. Т1 Строение атома и ПСХЭ
- 3. А1 Строение атома 13Al +13 2,8,3 3 период 2+8+3=13 Р (е)=13 N = 27-13=14 27 K
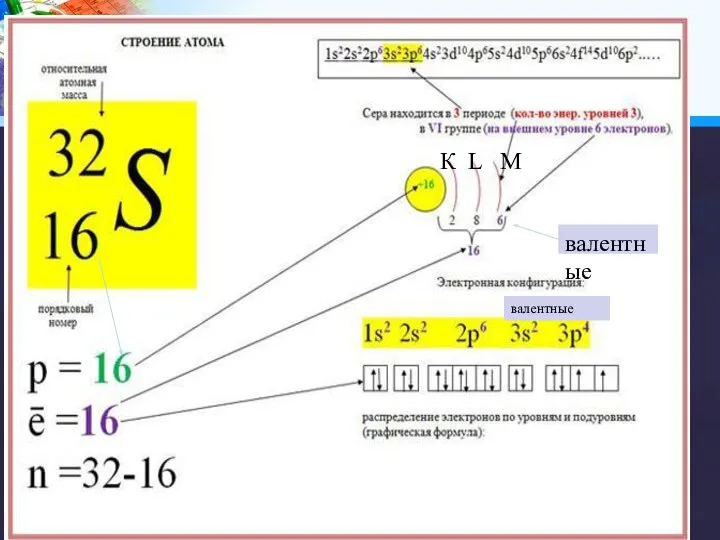
- 4. К L М валентные валентные
- 5. 4 период 6 группа главная подгруппа 34Se +34 2, 8, 18, 6 4период 7 группа побочная
- 8. №1 Ответ 1-бор Ответ -2
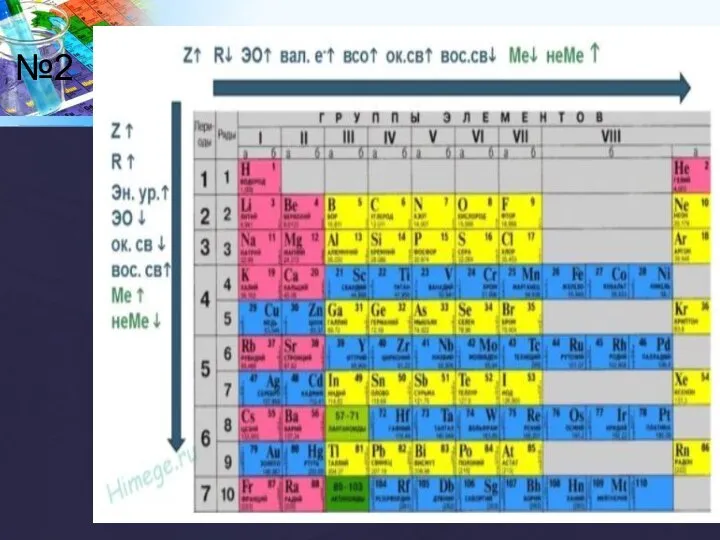
- 9. Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Необходимо запомнить: Физический смысл
- 10. №2
- 11. Ответ 3 Ответ 1
- 13. Ответ 34
- 14. 1. Учебный тренажер содержит 20 заданий В-1 с кратким ответом. 2. Задание считается выполненным верно, если
- 15. 1. В ряду химических элементов О → S → Sе: уменьшается радиус атома уменьшается электроотрицательность усиливаются
- 16. 2. В ряду химических элементов Na → Al → P происходит увеличение (усиление): числа нейтронов в
- 17. 3. В ряду химических элементов Cl → Si → Al: уменьшаются заряды ядер атомов возрастают кислотные
- 18. 4. В ряду химических элементов Sе → S → О: уменьшается валентность в высших оксидах возрастают
- 19. 5. В ряду химических элементов Si → Р → S: уменьшается число протонов в ядре уменьшается
- 20. 6. В ряду химических элементов Ве → Мg → Са: уменьшается радиус атомов возрастает способность атомов
- 21. 7. В ряду химических элементов N → Р → Аs: уменьшается электроотрицательность уменьшаются радиусы атомов ослабевают
- 22. 8. В порядке ослабевания металлических свойств расположены элементы в рядах: Be → Mg → Ca Na
- 23. 9. Способность отдавать электроны возрастает у элементов следующих рядов: уменьшается число протонов в ядре уменьшается электроотрицательность
- 24. 10. В ряду химических элементов Al → Mg →Na: усиливается электроотрицательность усиливаются металлические свойства усиливается основный
- 25. 11. В ряду химических элементов N → С → В: увеличивается число протонов в ядре увеличивается
- 26. 12. В порядке уменьшения числа электронов во внешнем слое расположены элементы следующих рядов: N → O
- 27. 13. В ряду химических элементов Si → Ge → Sn: увеличивается радиус атома ослабевают металлические свойства
- 28. 14. В ряду химических элементов Cl → S → P → Si: увеличиваются неметаллические свойства уменьшается
- 29. 15. В ряду химических элементов Si → Аl → Мg: уменьшается электроотрицательность увеличиваются заряды ядер атомов
- 30. 16. В ряду химических элементов Cl → P → Si: уменьшаются заряды ядер атомов уменьшается число
- 31. 17. В ряду химических элементов I → Вr → Сl: увеличивается степень окисления в высших оксидах
- 32. 18. В ряду химических элементов F → О → N: увеличивается число электронных слоев уменьшаются заряды
- 33. 19. В ряду химических элементов Аl → Р → Сl: увеличивается электроотрицательность уменьшаются заряды ядер атомов
- 35. Скачать презентацию






























 Основания
Основания Электролитическая диссоциация
Электролитическая диссоциация Алканы. Этан
Алканы. Этан Пиримидин. Пиримидиновые основания
Пиримидин. Пиримидиновые основания Аллотропия Аллотропные видоизменения (модификации)
Аллотропия Аллотропные видоизменения (модификации) Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1 Тест по теме Альдегиды и кетоны
Тест по теме Альдегиды и кетоны Химический анализ
Химический анализ Общая химия, понятия
Общая химия, понятия Study of short peptide adsorption on solution dispersed. Inorganic nanoparticles using depletion method
Study of short peptide adsorption on solution dispersed. Inorganic nanoparticles using depletion method Сера, значение и применение
Сера, значение и применение Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1)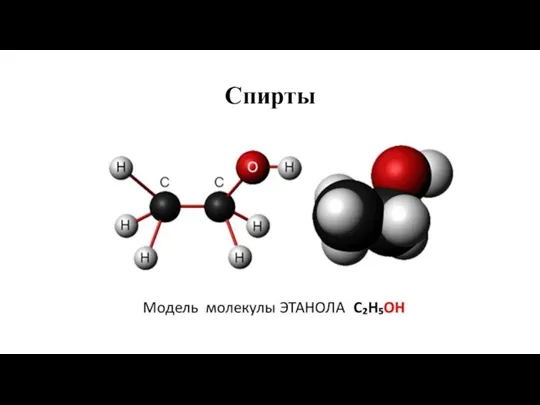 Спирты
Спирты История химии
История химии Презентация на тему Фосфор. Соединения фосфора
Презентация на тему Фосфор. Соединения фосфора  Ферменты
Ферменты Исследовательская работа по химии на тему: Интегративные проблемные ситуации
Исследовательская работа по химии на тему: Интегративные проблемные ситуации Периодический закон и строение атома
Периодический закон и строение атома Пусть имя Д.И. Менделеева будет нашей путеводной звездой
Пусть имя Д.И. Менделеева будет нашей путеводной звездой Азотсодержащие органические соединения
Азотсодержащие органические соединения Разбор заданий на амины
Разбор заданий на амины Химический состав клетки
Химический состав клетки Альдегиды. Кетоны
Альдегиды. Кетоны СРО № 3-4 ТБХ (2)
СРО № 3-4 ТБХ (2) Комплексные соли. 11 класс
Комплексные соли. 11 класс Презентация на тему Эфиры и жиры
Презентация на тему Эфиры и жиры  Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ)
Физическая химия тугоплавких неметаллических и силикатных материалов (ТНСМ) Соединения алюминия
Соединения алюминия