Содержание
- 2. Неорганическая биохимия (в 2 томах) Ред. Эйхгорн Гюнтер, 1978 Основы химии живого Слесарев В.И., 2000 Биометаллоорганическая
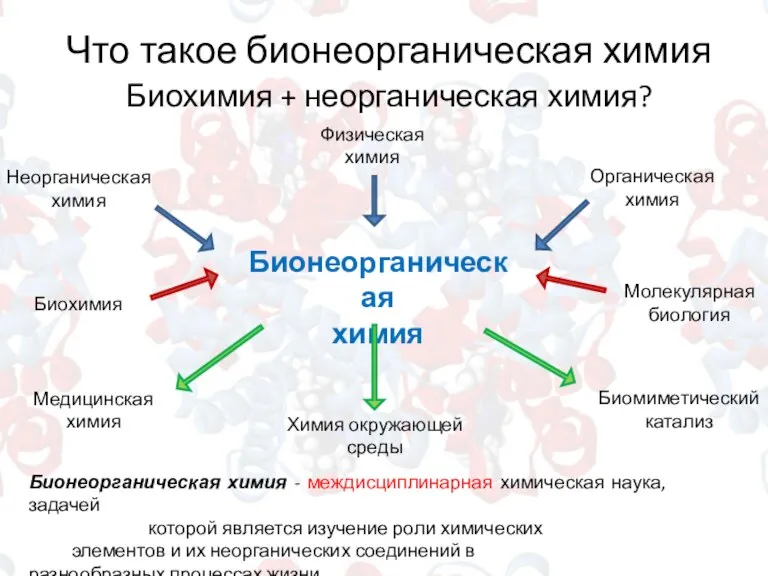
- 3. Что такое бионеорганическая химия Биохимия + неорганическая химия? Бионеорганическая химия Неорганическая химия Физическая химия Биохимия Органическая
- 4. Что такое бионеорганическая химия Задачи бионеорганической химии Изучение роли металлов и их соединений в живых организмах
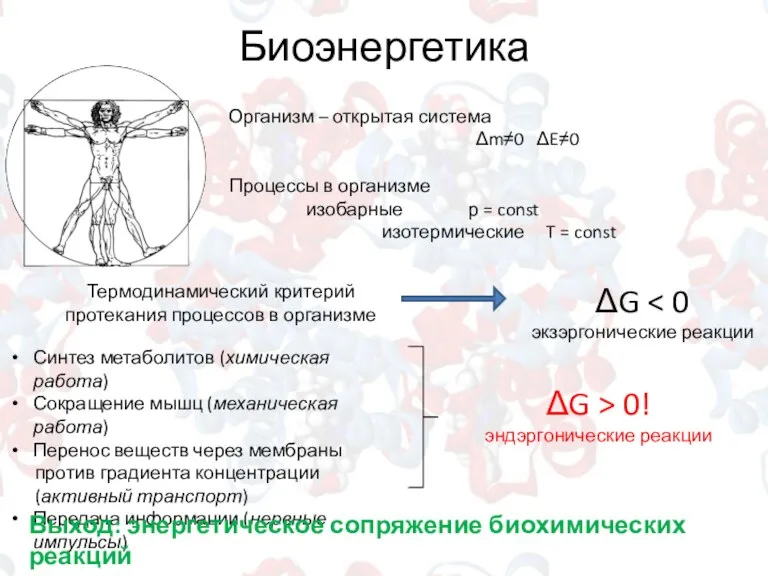
- 5. Биоэнергетика Организм – открытая система Δm≠0 ΔE≠0 Процессы в организме изобарные р = const изотермические T
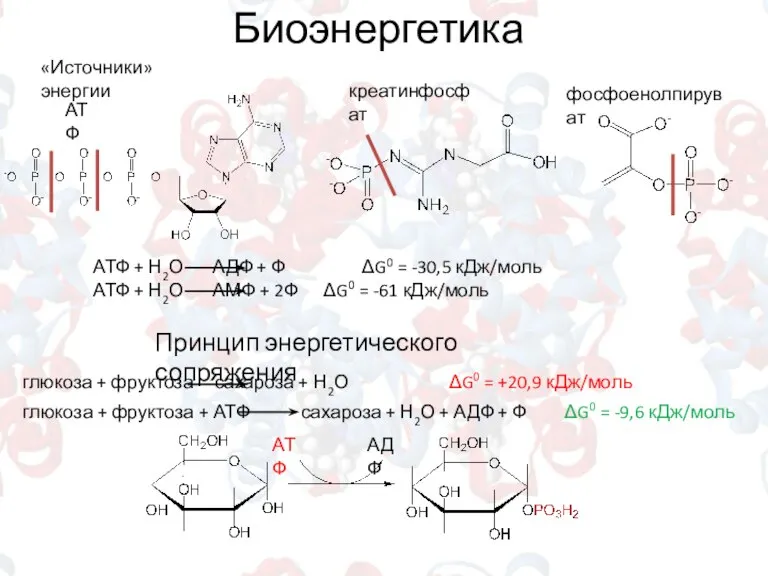
- 6. Биоэнергетика Принцип энергетического сопряжения «Источники» энергии АТФ креатинфосфат фосфоенолпируват
- 7. Биоэнергетика Химическое равновесие и стационарное состояние ΔG = 0 Химическое равновесие Процессы не протекают Джозайя Гиббс
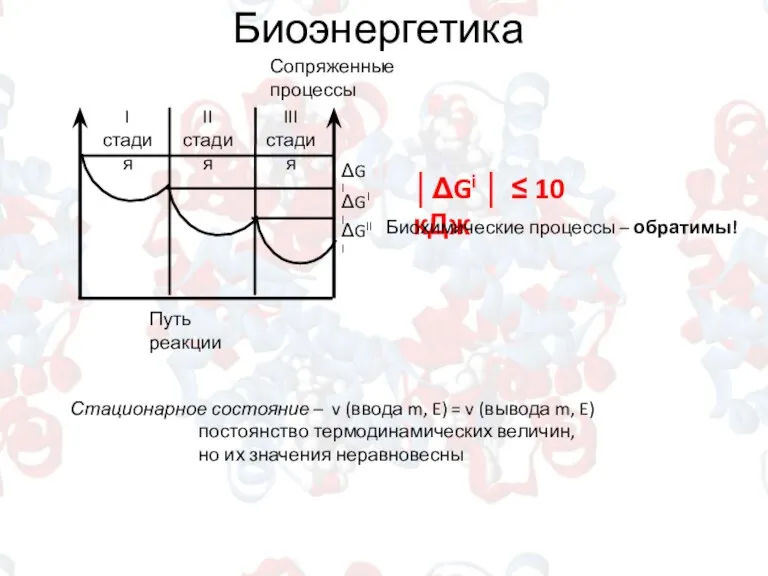
- 8. Биоэнергетика │ΔGi │ ≤ 10 кДж Биохимические процессы – обратимы! Стационарное состояние – v (ввода m,
- 9. Биоэнергетика Теорема Пригожина (1947) – стационарному состоянию системы в условиях, препятствующих достижению равновесия, соответствует минимальное значение
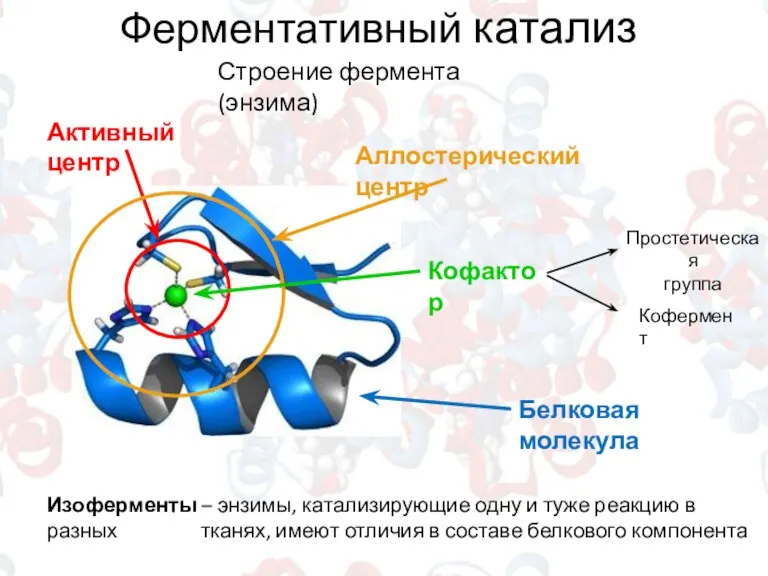
- 10. Ферментативный катализ Активный центр Аллостерический центр Кофактор Простетическая группа Кофермент Строение фермента (энзима) Белковая молекула Изоферменты
- 11. Ферментативный катализ Особенности ферментативного катализа Размер. М(фермента) = 105÷107 г/моль → коллоидные системы, микрогетерогенность Высокая каталитическая
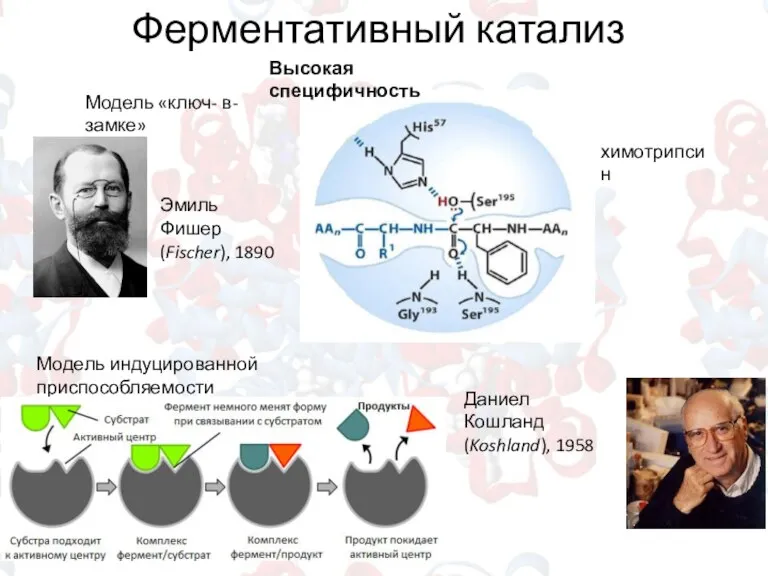
- 12. Ферментативный катализ Высокая специфичность Модель индуцированной приспособляемости Эмиль Фишер (Fischer), 1890 Даниел Кошланд (Koshland), 1958 химотрипсин
- 13. Ферментативный катализ Уравнение Михаэлиса-Ментен Леонор Михаэлис (Michaelis) Мод Ментен (Menten)
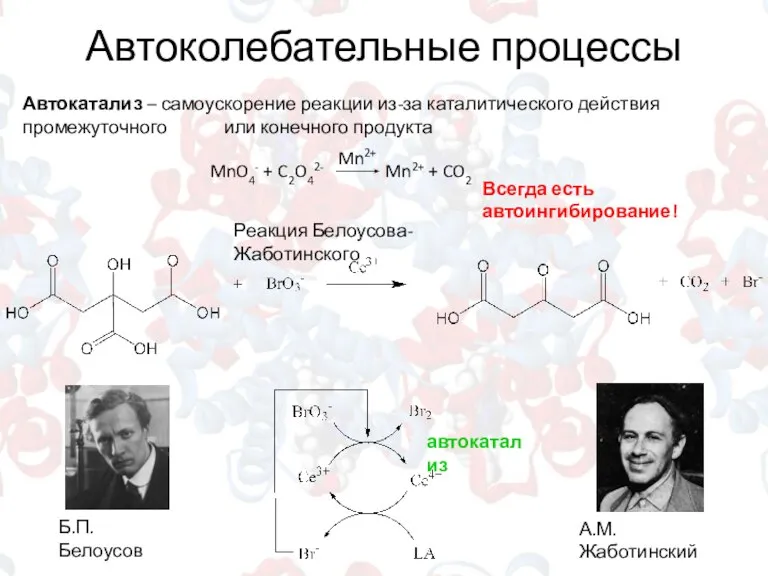
- 14. Автоколебательные процессы Автокатализ – самоускорение реакции из-за каталитического действия промежуточного или конечного продукта Всегда есть автоингибирование!
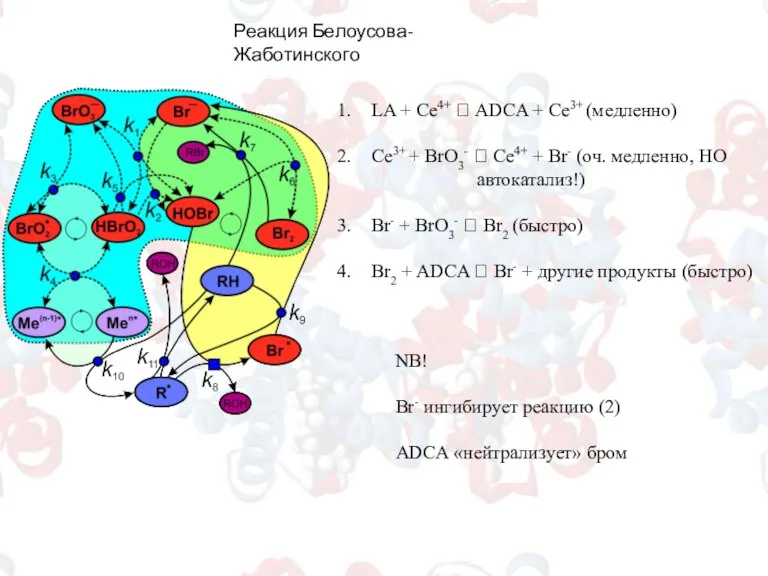
- 15. Реакция Белоусова-Жаботинского LA + Ce4+ ? ADCA + Ce3+ (медленно) Сe3+ + BrO3- ? Ce4+ +
- 17. Скачать презентацию






 Опорно-двигательная система
Опорно-двигательная система Кто такие рыбы? (1 класс)
Кто такие рыбы? (1 класс) Строение растения картофеля. Картофельное поле
Строение растения картофеля. Картофельное поле Животный мир леса. (2 класс)
Животный мир леса. (2 класс) Цікаве про тритонів
Цікаве про тритонів Индивидуальное развитие организма
Индивидуальное развитие организма Побег. Строение и значение побега
Побег. Строение и значение побега Домашние животные
Домашние животные Физиология нервов и мышц
Физиология нервов и мышц Эпителии. Железы
Эпителии. Железы Уровни организации живых систем
Уровни организации живых систем Кто живет на дне морском? Загадки для самых сообразительных
Кто живет на дне морском? Загадки для самых сообразительных Разнообразен и прекрасен мир растений
Разнообразен и прекрасен мир растений Фотосинтез. Этапы его развития
Фотосинтез. Этапы его развития Млекопитающие. Урок-экскурсия
Млекопитающие. Урок-экскурсия Сокровища Деметры
Сокровища Деметры Мутагенные факторы среды
Мутагенные факторы среды Методы исследования генетики человека (число и тема в тетрадь)
Методы исследования генетики человека (число и тема в тетрадь) Презентация на тему Биогеоценоз, как особый уровень организации жизни
Презентация на тему Биогеоценоз, как особый уровень организации жизни  Фотосинтез. Образование органического вещества
Фотосинтез. Образование органического вещества Декоративные птицы
Декоративные птицы Краткая история развития зоологии 7 класс Зоология 4 урок
Краткая история развития зоологии 7 класс Зоология 4 урок Углы в краниометрии. (Тема 4)
Углы в краниометрии. (Тема 4) Презентация на тему РАСТЕНИЯ-СИМВОЛЫ
Презентация на тему РАСТЕНИЯ-СИМВОЛЫ  Викторина по биологии
Викторина по биологии Понятие витаминов
Понятие витаминов Протисты (protista)
Протисты (protista) Науки об организме человека
Науки об организме человека