Содержание
- 4. «Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимется, столько
- 5. Ключ к тесту
- 6. Цель урока помочь обучающимся сформировать знания о химическом уравнении как об условной записи химической реакции с
- 7. Химические реакции. Составление уравнений химических реакций Тема урока
- 8. Проблема Является ли закон сохранения массы веществ основой для составления уравнений химических реакций
- 10. Железо + сера → сульфид железа (II ) Fe + S → FeS
- 12. Al + O2 → Al O Al + O2 → Al+3 O-2 Al + O2 →
- 14. Fe(OH)3→ Fe2O3 + H2O 2Fe(OH)3 → Fe2O3 + H2O 2Fe(OH)3 → Fe2O3 + 3H2O 2Fe(OH)3 =
- 15. Алгоритмом расстановки коэффициентов в уравнениях химических реакций Подсчитать количество атомов каждого элемента в правой и левой
- 17. 2P + 5Cl2 →2PCl5 2Na + S → Na2S 2HCl + Mg →MgCl2 + H2 N2
- 18. Проблема Является ли закон сохранения массы веществ основой для составления уравнений химических реакций
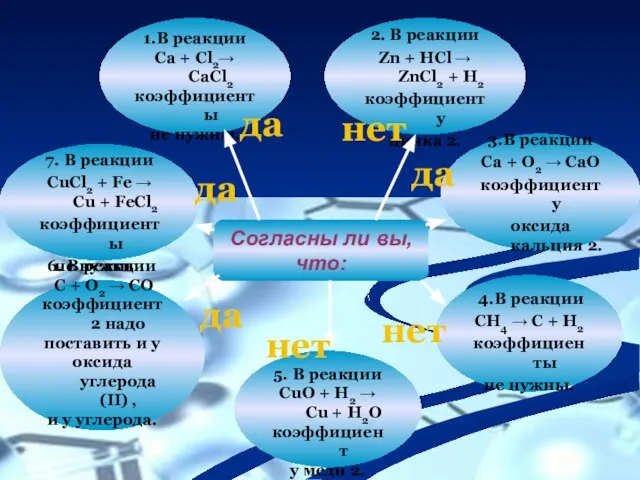
- 19. Согласны ли вы, что: 1.В реакции Ca + Cl2→ CaCl2 коэффициенты не нужны. 2. В реакции
- 20. Оценка за урок Если вы набрали: 20-21 балл – оценка«5» 17-19 баллов – оценка«4» 13-16 баллов
- 21. Домашнее задание §14, упр. 1 – для тех, кто получил оценку «3» упр. 2,4– для тех,
- 23. Скачать презентацию

















 Экономика
Экономика Какое слово склевали цыплята?
Какое слово склевали цыплята? Детское объединение Клуб общения
Детское объединение Клуб общения body parts
body parts ВКР: Алгоритм поиска неисправностей схемы питания главной платы smart-led-телевизора LG на шасси LA31R
ВКР: Алгоритм поиска неисправностей схемы питания главной платы smart-led-телевизора LG на шасси LA31R Pancakes day
Pancakes day  Перевод чисел из десятичной системы счисления в двоичную, восьмеричную и шестнадцатеричную
Перевод чисел из десятичной системы счисления в двоичную, восьмеричную и шестнадцатеричную Деловая игра для учащихся Притобольной средней школы
Деловая игра для учащихся Притобольной средней школы Правила проведения делового разговора по телефону
Правила проведения делового разговора по телефону Формулировка и комментарий основной проблемы текста
Формулировка и комментарий основной проблемы текста Новые инновационные композиционные материалы
Новые инновационные композиционные материалы Портрет Натюрморт Пейзаж Описание
Портрет Натюрморт Пейзаж Описание Происхождение Вселенной 11 класс
Происхождение Вселенной 11 класс Лудомания
Лудомания Повышение эффективности системы солнечного теплоснабженияА. Жамалов КазГос ЖенПИ
Повышение эффективности системы солнечного теплоснабженияА. Жамалов КазГос ЖенПИ Развитие координационных способностей у юных борцов вольного стиля
Развитие координационных способностей у юных борцов вольного стиля My holidays
My holidays Презентация
Презентация Презентация на тему Первые русские князья Олег, Игорь, Ольга
Презентация на тему Первые русские князья Олег, Игорь, Ольга  Гатчинский педагогический колледж имени К.Д. Ушинского
Гатчинский педагогический колледж имени К.Д. Ушинского Объект. Предмет
Объект. Предмет Покинут счастьем будет тот, Кого ребёнком плохо воспитали. Побег зелёный выпрямить легко, Сухую ветвь один огонь исправит.
Покинут счастьем будет тот, Кого ребёнком плохо воспитали. Побег зелёный выпрямить легко, Сухую ветвь один огонь исправит.  Научная химическая лаборатория Ломоносова
Научная химическая лаборатория Ломоносова Вы блестящий учитель, у Вас прекрасные ученики!
Вы блестящий учитель, у Вас прекрасные ученики! Среды обитания организмов. Приспособленность к среде обитания
Среды обитания организмов. Приспособленность к среде обитания Киото Сангё Университет
Киото Сангё Университет Звезда по имени Саломея Крушельницкая
Звезда по имени Саломея Крушельницкая «Создание условий в ДОУ комбинированного вида для комплексной поддержки детей с ограниченными возможностями здоровья»
«Создание условий в ДОУ комбинированного вида для комплексной поддержки детей с ограниченными возможностями здоровья»