Содержание
- 2. Содержание : 1. Определение сущности процесса электролиза 2. Электролиз в расплавах: а) процессы на катоде б)
- 3. Электролиз – это окислительно-восстановительный процесс, протекающий на электродах в растворах или расплавах электролитов при пропускании электрического
- 4. Электролиз в расплавах На катоде происходит процесс восстановления • В расплавах катионы металла восстанавливаются до свободного
- 5. Электролиз в расплавах На аноде происходит процесс окисления • В расплавах анионы бескислородных кислот (кроме фторидов)
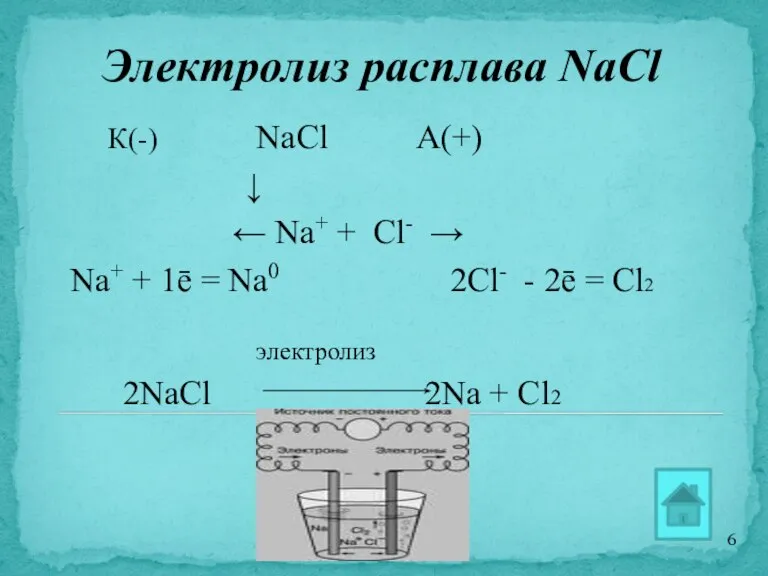
- 6. Электролиз расплава NaCl К(-) NaCl А(+) ↓ ← Na+ + Cl- → Na+ + 1ē =
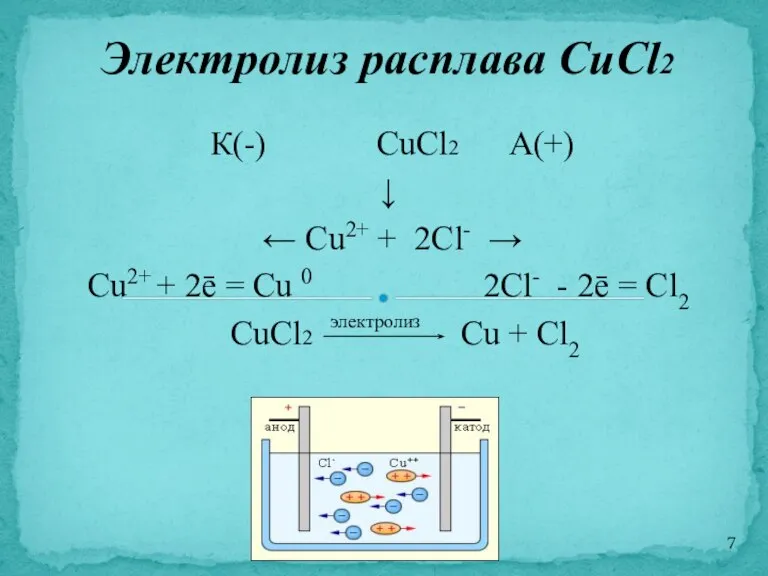
- 7. К(-) CuCl2 А(+) ↓ ← Cu2+ + 2Cl- → Cu2+ + 2ē = Cu 0 2Cl-
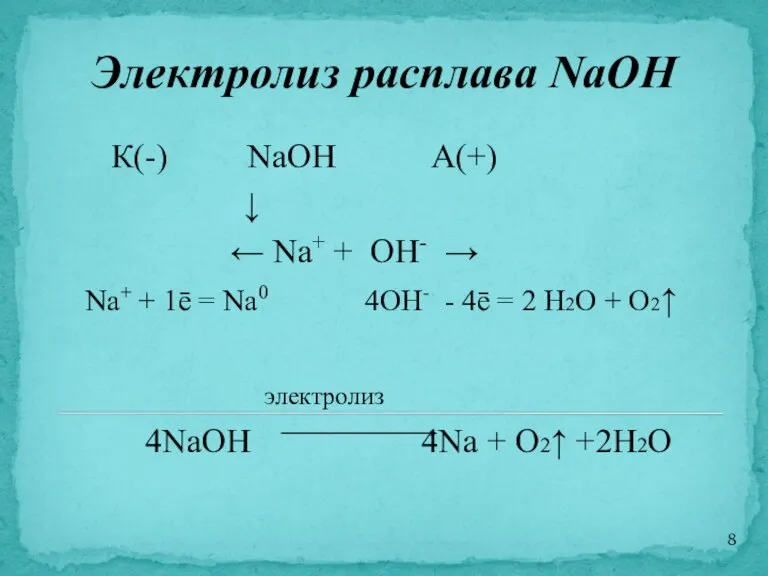
- 8. Электролиз расплава NaOH К(-) NaOH А(+) ↓ ← Na+ + OH- → Na+ + 1ē =
- 9. Электролиз в растворах (процесс на катоде) В растворах процесс на катоде не зависит от материала катода,
- 10. Электролиз в растворах (процесс на катоде) б) Если металл расположен в ряду напряжений между Al и
- 11. Процесс на аноде В растворах процесс на аноде зависит от материала анода и от природы аниона.
- 12. Процесс на аноде б) Если анод инертный, то в случае бескислородных анионов (кроме фторидов) идет окисление
- 13. Электролиз раствора NaCl на инертном аноде К(-) NaCl А(+) ↓ ← Na+ + Cl- → 2Н2О
- 14. Электролиз раствора CuSO4 на инертном аноде К(-) CuSO4 А(+) ↓ ← Cu2+ + SO42- → Cu2+
- 15. Электролиз раствора NaCl на растворимом аноде К(-) NaCl А(+) ↓ (Cu) ← Na+ + Cl- →
- 16. Применение электролиза: получение чистых металлов (Алюминий, магний, натрий, кадмий получают только электролизом)
- 17. очистка металлов
- 18. получение щелочей, хлора, водорода
- 19. защита металлов от коррозии (При этом на поверхности металлических изделий электрохимическим методом наносят тонкий слой другого
- 20. копирование рельефных изделий из металлов и других материалов. Гальванопластика позволяет создавать документально точные копии барельефов, монет,
- 21. применение электролиза в косметологии для электроэпиляции (при удалении волос этим методом используются очень тонкие иголочки, которыми
- 22. Тест по теме "Электролиз" 1. При электролизе раствора сульфата цинка с инертными электродами на аноде выделяется:
- 23. 3. При электролизе расплава гидроксида натрия на аноде выделяется: а) натрий; б) водород; в) кислород; г)
- 24. 5. Процесс на катоде при электролизе растворов солей зависит от: а) природы катода; б) активности металла;
- 25. 7. При электролизе 240 г 15%-го раствора гидроксида натрия на аноде выделилось 89,6 л (н.у.) кислорода.
- 26. А теперь проверим ваши ответы! 1-б 2-б 3-в, г 4-а, г 5-б 6- в 7- в
- 27. Домашнее задание: Учебник О.С.Габриеляна Химия 11 класс § 18 (стр.217 - 222), упр. 22,23,25.
- 28. Список использованной литературы: 1. О.С.Габриелян Учебник химии для 11 класса, М., Дрофа, 2004г. Интернет – ресурсы:
- 30. Скачать презентацию























 Oatmeal cookies with honey
Oatmeal cookies with honey Их имена у всех на устах
Их имена у всех на устах Когда изобрели велосипед
Когда изобрели велосипед Пособия семьям, имеющим детей: ближайшие перспективы и текущая ситуация
Пособия семьям, имеющим детей: ближайшие перспективы и текущая ситуация Аттестационная работа. Классификация рисунков Александра Сергеевича Пушкина
Аттестационная работа. Классификация рисунков Александра Сергеевича Пушкина Вопрос №6Системы сертификации, требования к аккредитации. Типовая структура построения системы. Органы по сертификации, испытате
Вопрос №6Системы сертификации, требования к аккредитации. Типовая структура построения системы. Органы по сертификации, испытате Физика в космосе
Физика в космосе Великая Отечественная война
Великая Отечественная война Презентация дидактического материала для работы с одарёнными детьми на уроках литературного чтения ( развитие творческого вообр
Презентация дидактического материала для работы с одарёнными детьми на уроках литературного чтения ( развитие творческого вообр Презентация на тему Самопознание и развитие личности
Презентация на тему Самопознание и развитие личности ЭТОТ ДЕНЬ МЫ НЕ ЗАБУДЕМ НИКОГДА! Посвящается моему прапрадеду, ветерану Великой Отечественной войны Логачеву Алексею Стефанович
ЭТОТ ДЕНЬ МЫ НЕ ЗАБУДЕМ НИКОГДА! Посвящается моему прапрадеду, ветерану Великой Отечественной войны Логачеву Алексею Стефанович Граждане как субъекты гражданских прав
Граждане как субъекты гражданских прав Шакирова Фарида Фаритовна и её любимый 4 «В» класс Торопись, ведь дни проходят: Ты у времени в гостях Не рассчитывай на помощь, Помни
Шакирова Фарида Фаритовна и её любимый 4 «В» класс Торопись, ведь дни проходят: Ты у времени в гостях Не рассчитывай на помощь, Помни Предпринимательский проект по производству резиновой плитки
Предпринимательский проект по производству резиновой плитки Макс срсп
Макс срсп ПОРТРЕТЫ И ПЕЙЗАЖИ АРМЕНИИ
ПОРТРЕТЫ И ПЕЙЗАЖИ АРМЕНИИ Прайс-лист на размещение рекламы
Прайс-лист на размещение рекламы Тесты по баскетболу
Тесты по баскетболу Передача информации 5 класс
Передача информации 5 класс Внешнее дыхание
Внешнее дыхание  УЗ «Гродненская областная инфекционная клиническая больница» - единственный областной инфекционный стационар, оказывающий специ
УЗ «Гродненская областная инфекционная клиническая больница» - единственный областной инфекционный стационар, оказывающий специ С литературой по Московскому тракту через Сибирь
С литературой по Московскому тракту через Сибирь Презентация на тему Сжатое изложение
Презентация на тему Сжатое изложение  «БРЕНД “РОССИЯ”» БРЕНДИНГ СТРАНЫ: ВЫЗОВ или ОБЕЩАНИЕ? Второй этап исследования журнала «Со-Общение» Итоги первого этапа (2006-2008
«БРЕНД “РОССИЯ”» БРЕНДИНГ СТРАНЫ: ВЫЗОВ или ОБЕЩАНИЕ? Второй этап исследования журнала «Со-Общение» Итоги первого этапа (2006-2008  Информационно-правоваябаза данных«ТорговыйЛоцман»
Информационно-правоваябаза данных«ТорговыйЛоцман» Дипломное проектирование - важный этап подготовки специалистов
Дипломное проектирование - важный этап подготовки специалистов Presentation 4
Presentation 4 Помада абсолютный поцелуй
Помада абсолютный поцелуй