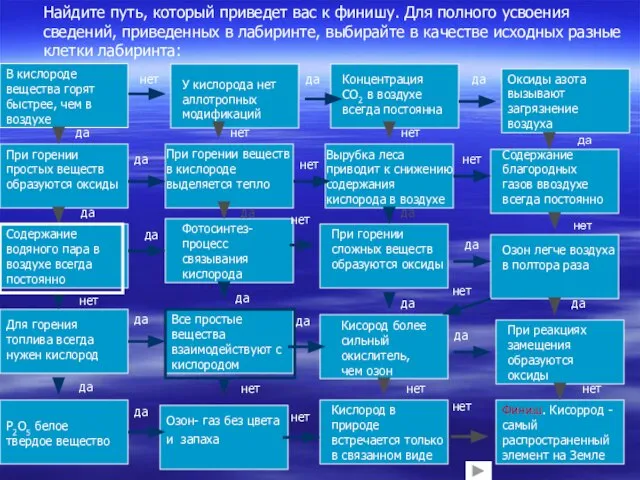
в лабиринте, выбирайте в качестве исходных разные клетки лабиринта:
В кислороде вещества горят быстрее, чем в воздухе
У кислорода нет аллотропных модификаций
При горении простых веществ образуются оксиды
При горении веществ в кислороде выделяется тепло
Концентрация СО2 в воздухе всегда постоянна
Оксиды азота вызывают загрязнение воздуха
Содержание благородных газов ввоздухе всегда постоянно
Вырубка леса приводит к снижению содержания кислорода в воздухе
нет
да
да
да
Содержание водяного пара в воздухе всегда постоянно
Фотосинтез- процесс связывания кислорода
При горении сложных веществ образуются оксиды
Озон легче воздуха в полтора раза
Для горения топлива всегда нужен кислород
Все простые вещества взаимодействуют с кислородом
Кисород более сильный окислитель, чем озон
При реакциях замещения образуются оксиды
P2O5 белое твердое вещество
Озон- газ без цвета и запаха
Кислород в природе встречается только в связанном виде
Финиш. Кисоррод - самый распространенный элемент на Земле
нет
нет
нет
да
нет
да
нет
нет
да
нет
да
да
да
да
да
нет
да
нет
да
да
нет
да
да
нет
да
нет
да
нет













 Предложения по формированию в структуре Правительства РФ Департамента стратегического развития
Предложения по формированию в структуре Правительства РФ Департамента стратегического развития Правовая природа ЕС
Правовая природа ЕС Electrical generator
Electrical generator 22
22 Управление договорами - 5
Управление договорами - 5 Памятник Североморцам
Памятник Североморцам Инвестиционная составляющая лесопромышленного комплекса Иркутской области
Инвестиционная составляющая лесопромышленного комплекса Иркутской области Виды научно-исследовательских работ
Виды научно-исследовательских работ Методы развития памяти
Методы развития памяти «Особенности и проблемы развития рынка услуг связи Московской области» Владимир Демчишин – генеральный директор, (
«Особенности и проблемы развития рынка услуг связи Московской области» Владимир Демчишин – генеральный директор, ( Понимание свободы подростками на примере обучающихся средней образовательной школы
Понимание свободы подростками на примере обучающихся средней образовательной школы Роль содружества «Могучая кучка» в русской культуре
Роль содружества «Могучая кучка» в русской культуре Храм Василия Блаженного
Храм Василия Блаженного Новый мир начинается с тебя
Новый мир начинается с тебя НАНОТЕХНОЛОГИИ В БИОЛОГИИ И МЕДИЦИНЕ
НАНОТЕХНОЛОГИИ В БИОЛОГИИ И МЕДИЦИНЕ Предложение партнерства с Теле2
Предложение партнерства с Теле2 Стиральная машина WF0702WKE/YLP
Стиральная машина WF0702WKE/YLP Getting you there.. Bancassurance @ Fortis | November 2007 | 2 При различных структурах собственности могут применяться различные брэндинговые стратегии.
Getting you there.. Bancassurance @ Fortis | November 2007 | 2 При различных структурах собственности могут применяться различные брэндинговые стратегии. Части речи
Части речи Муниципальное дошкольное образовательное учреждение «Центр развития ребенка – детский сад № 9» Проект «В поисках лета»
Муниципальное дошкольное образовательное учреждение «Центр развития ребенка – детский сад № 9» Проект «В поисках лета» Символ Ростех - Мягкоступов Р.О. (Филиал ПАО ОДК-Сатурн - ОМКБ (1)
Символ Ростех - Мягкоступов Р.О. (Филиал ПАО ОДК-Сатурн - ОМКБ (1) Механические волны
Механические волны Products
Products Дачный дом (фотографии)
Дачный дом (фотографии) Эффективные модели обновления систем повышения квалификации и аттестации педагогических кадров
Эффективные модели обновления систем повышения квалификации и аттестации педагогических кадров London is the capital of Great Britain
London is the capital of Great Britain ПРОГРАММА РАЗВИТИЯ КАФЕДРЫ МЕНЕДЖМЕНТА ИНСТИТУТА ЭКОНОМИКИ С(А)ФУ НА 2011-2015 ГГ.
ПРОГРАММА РАЗВИТИЯ КАФЕДРЫ МЕНЕДЖМЕНТА ИНСТИТУТА ЭКОНОМИКИ С(А)ФУ НА 2011-2015 ГГ. Пресмыкающиеся Тульской области
Пресмыкающиеся Тульской области