Слайд 2Цель урока:
Установить взаимосвязь между макроскопическими и микроскопическими параметрами
Научиться решать вычислительные задачи с

использованием основного уравнения МКТ
Слайд 3Макроскопические – параметры, которые можно измерить с помощью приборов.
Микроскопические – параметры, которые

измеряются косвенным путем.
Слайд 4m – масса газа
V – объем газа
t – температура газа
p –
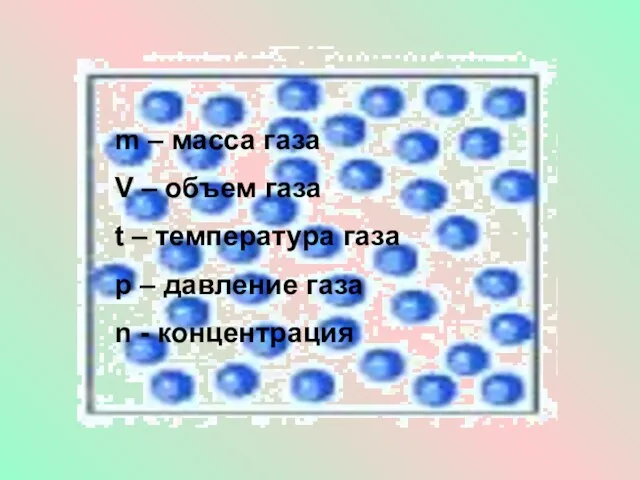
давление газа
n - концентрация
Слайд 6Модель идеального газа
1. Межмолекулярные силы притяжения отсутствуют (можно пренебречь потенциальной энергией)
2. Взаимодействия

молекул газа происходят только при их соударениях и являются упругими
3. Молекулы газа не имеют объема - рассматриваются как материальные точки
Слайд 8Это уравнение, выведенное впервые немецким физиком Р. Клаузиусом, называется основным уравнением молекулярно-кинетической

теории идеального газа. Оно устанавливает связь между микроскопическими параметрами и макроскопическими (измеряемыми) величинами.
Слайд 9Учитывая, что - средняя кинетическая энергия молекулы газа,
получим:

Слайд 10Давление идеального газа прямо пропорционально средней кинетической энергии поступательного движения молекул, содержащихся

в единице объема газа.
Слайд 12Задача №1.
Каково давление азота, если средняя
квадратичная скорость его молекул
500 м/с, а

его плотность 1,36 кг/м3 ?
Слайд 14Задача №2.
Имеются два одинаковых сосуда. В одном из них находится кислород,

а в другом азот. Число молекул каждого газа и средние квадраты их скоростей одинаковы. Давление кислорода равно 32 кПа. Чему равно давление азота?








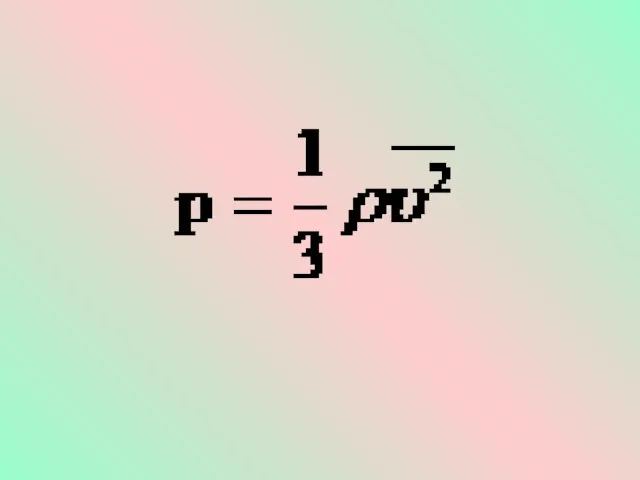



 ПРЕЗЕНТАЦИЯ О ПРЕЗЕНТАЦИЯХ
ПРЕЗЕНТАЦИЯ О ПРЕЗЕНТАЦИЯХ Ручная аргонодуговая сварка
Ручная аргонодуговая сварка Катанын үстүндө иштөө. 8 класс
Катанын үстүндө иштөө. 8 класс Дорога к трем п: понимание, прозрачность, повышение эффективности
Дорога к трем п: понимание, прозрачность, повышение эффективности Презентация на тему Форма государственного устройства, ее виды
Презентация на тему Форма государственного устройства, ее виды  Ballroom Dance: a sport or an art?
Ballroom Dance: a sport or an art? ПСИХОЛОГИЯ ПОЗНАВАТЕЛЬНЫХ ПРОЦЕССОВ
ПСИХОЛОГИЯ ПОЗНАВАТЕЛЬНЫХ ПРОЦЕССОВ ТИТБИТ (Товарищество Информационных Технологий БИТ)г. Киев, (044) 2712452, 2712125,
ТИТБИТ (Товарищество Информационных Технологий БИТ)г. Киев, (044) 2712452, 2712125,  Жили-были динозавры
Жили-были динозавры Презентація урок 2
Презентація урок 2 Строительство аэропортового комплекса «Южный» г. Ростов-на-Дону
Строительство аэропортового комплекса «Южный» г. Ростов-на-Дону Презентация на тему Пагубные привычки
Презентация на тему Пагубные привычки Историко-культурное наследие Молдовы
Историко-культурное наследие Молдовы Виды усилителей. Построение многокаскадных усилителей. Требования к усилительным каскадам
Виды усилителей. Построение многокаскадных усилителей. Требования к усилительным каскадам Кольори. Послідовність кольорів
Кольори. Послідовність кольорів Презентация на тему Исчезающие виды растений
Презентация на тему Исчезающие виды растений Маркировки лидера
Маркировки лидера Мышление – это выбор…
Мышление – это выбор… Комиссионный осмотр обустройств станции
Комиссионный осмотр обустройств станции Презентация на тему Механическая энергия Закон сохранения энергии
Презентация на тему Механическая энергия Закон сохранения энергии  The Germanic languages Alphabets, Vocabulary and semantics
The Germanic languages Alphabets, Vocabulary and semantics Классный час: «Вред курения»
Классный час: «Вред курения» Соответствие цветов. Цветовые пространства и модели
Соответствие цветов. Цветовые пространства и модели Тема: «Сложение с помощью линейки: прибавление числа 6.
Тема: «Сложение с помощью линейки: прибавление числа 6. Значение имён
Значение имён Земельный участокна поляне Фрунзе 9 линия
Земельный участокна поляне Фрунзе 9 линия Episode 3. Part 1. Vocabulary
Episode 3. Part 1. Vocabulary Дружно в садике живем
Дружно в садике живем