Содержание
- 2. "Жизнь — это открытые саморегулирующиеся и самовоспроизводящиеся системы совокупностей живых организмов, построенные из сложных биологических полимеров
- 3. Белки— высокомолекулярные органические соединения – (ВМС), нерегулярные биополимеры, состоящие из мономеров- аминокислот, соединенных пептидной связью.
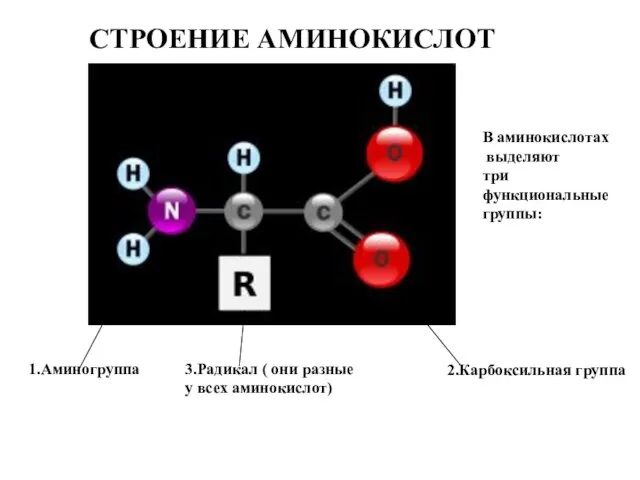
- 4. СТРОЕНИЕ АМИНОКИСЛОТ В аминокислотах выделяют три функциональные группы: 1.Аминогруппа 2.Карбоксильная группа 3.Радикал ( они разные у
- 5. Не могут быть синтезированы в организме. Поэтому их поступление в организм с пищей необходимо. Незаменимыми для
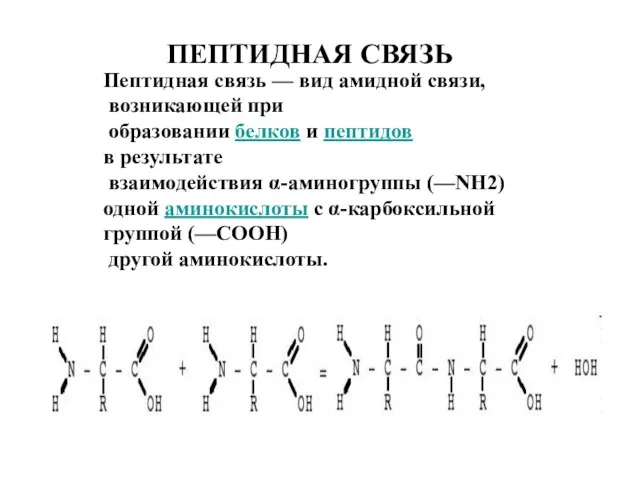
- 6. ПЕПТИДНАЯ СВЯЗЬ Пептидная связь — вид амидной связи, возникающей при образовании белков и пептидов в результате
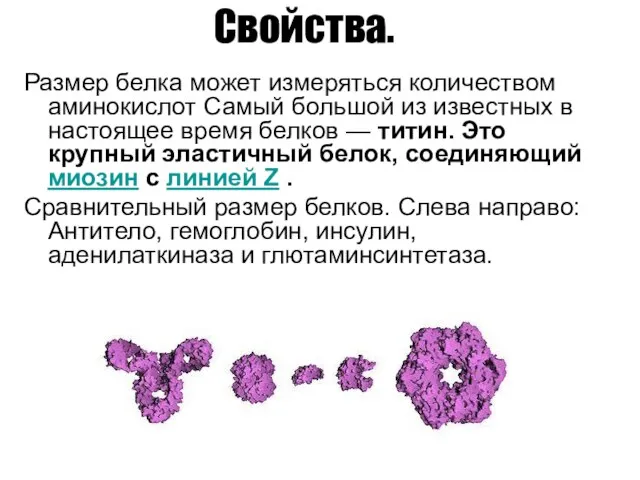
- 7. Свойства. Размер белка может измеряться количеством аминокислот Самый большой из известных в настоящее время белков —
- 8. Денатурация. Резкое изменение условий, например, нагревание или обработка белка кислотой или щёлочью приводит к потере четвертичной,
- 9. Б Е Л К И Простые Состоят только из аминокислотных остатков Сложные могут включать: - ионы
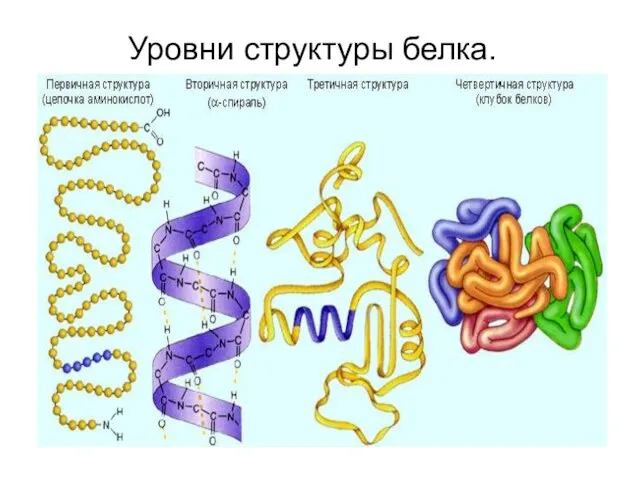
- 10. Уровни структуры белка.
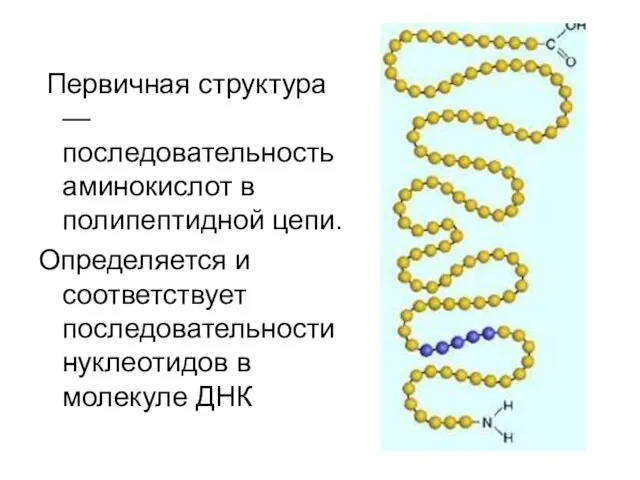
- 11. Первичная структура — последовательность аминокислот в полипептидной цепи. Определяется и соответствует последовательности нуклеотидов в молекуле ДНК
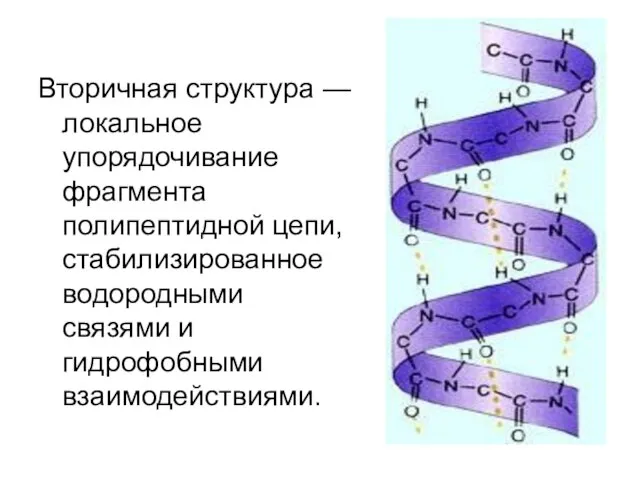
- 12. Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями и гидрофобными взаимодействиями.
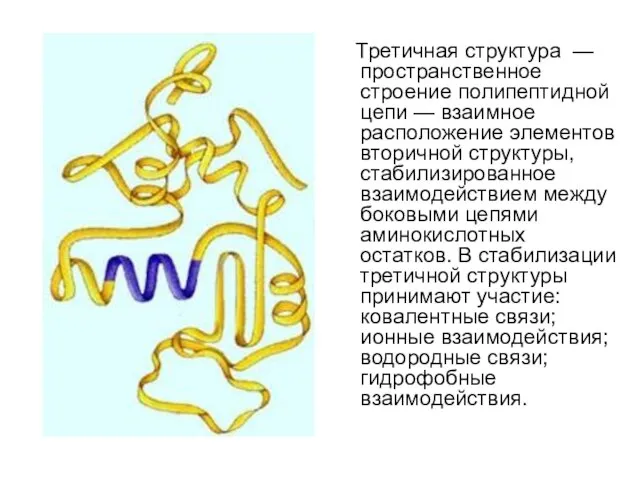
- 13. Третичная структура — пространственное строение полипептидной цепи — взаимное расположение элементов вторичной структуры, стабилизированное взаимодействием между
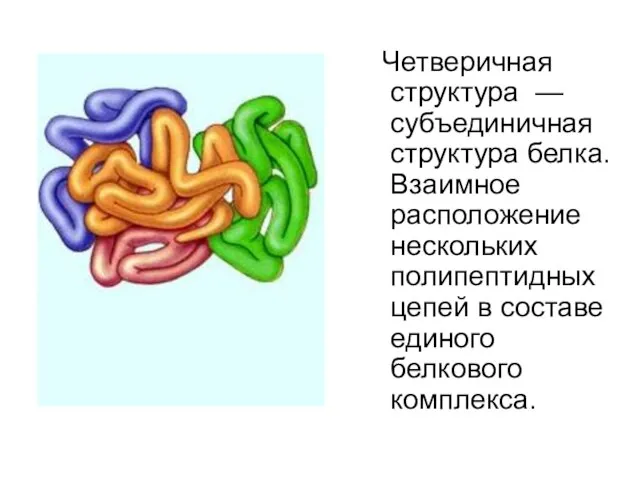
- 14. Четверичная структура — субъединичная структура белка. Взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса.
- 16. Скачать презентацию




 Концепции биологии. Строение живого
Концепции биологии. Строение живого Растения Пензенской области
Растения Пензенской области Історія використання людством біотехнологій
Історія використання людством біотехнологій Методы изучения живых организмов. Многообразие форм живых организмов
Методы изучения живых организмов. Многообразие форм живых организмов Отчет об экскурсии. Разнообразие видов в сообществе
Отчет об экскурсии. Разнообразие видов в сообществе Учение о тканях. Эпителиальные ткани. Лекция 4
Учение о тканях. Эпителиальные ткани. Лекция 4 Класс земноводные (амфибии)
Класс земноводные (амфибии) Комнатные растения
Комнатные растения Зуби ссавців
Зуби ссавців Корень. Корневые системы. Строение корня
Корень. Корневые системы. Строение корня Причины исчезновения динозавров. 1 класс
Причины исчезновения динозавров. 1 класс Анализ экологической устойчивости гороха (pisum sativum l.) в условиях зоны недостаточного увлажнения
Анализ экологической устойчивости гороха (pisum sativum l.) в условиях зоны недостаточного увлажнения Пастушья сумка
Пастушья сумка Распознавание сложных образов
Распознавание сложных образов Эмбриональное развитие дыхательной системы. Аномалии развития
Эмбриональное развитие дыхательной системы. Аномалии развития Алоэ - комнатные растения
Алоэ - комнатные растения Общие закономерности физиологии, основные понятия
Общие закономерности физиологии, основные понятия Вермикомпостирование жиросодержащих отходов и избыточного ила с целью получения биоудобрения
Вермикомпостирование жиросодержащих отходов и избыточного ила с целью получения биоудобрения Общая характеристика класса - Ленточные черви(Cestoda)
Общая характеристика класса - Ленточные черви(Cestoda) Сочные плоды
Сочные плоды Головной мозг
Головной мозг Вода, ее состав, свойства, значение
Вода, ее состав, свойства, значение Уникальная ольфакторная подпись
Уникальная ольфакторная подпись Такие большие, маленькие насекомые
Такие большие, маленькие насекомые 基因表达调控
基因表达调控 Групи риб
Групи риб Плюрализм концепций происхождения жизни на Земле
Плюрализм концепций происхождения жизни на Земле мышцы
мышцы