Содержание
- 3. Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики.
- 4. Цели урока: знать формулировку второго закона термодинамики; объяснять смысл второго закона термодинамики; применять второй закон термодинамики
- 5. Критерии оценивания: знаю формулировку второго закона термодинамики; объясняю смысл второго закона термодинамики; применяю второй закон термодинамики
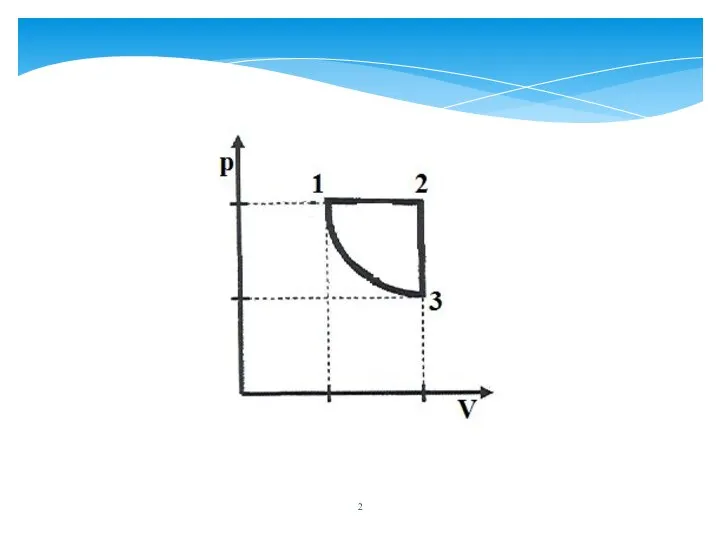
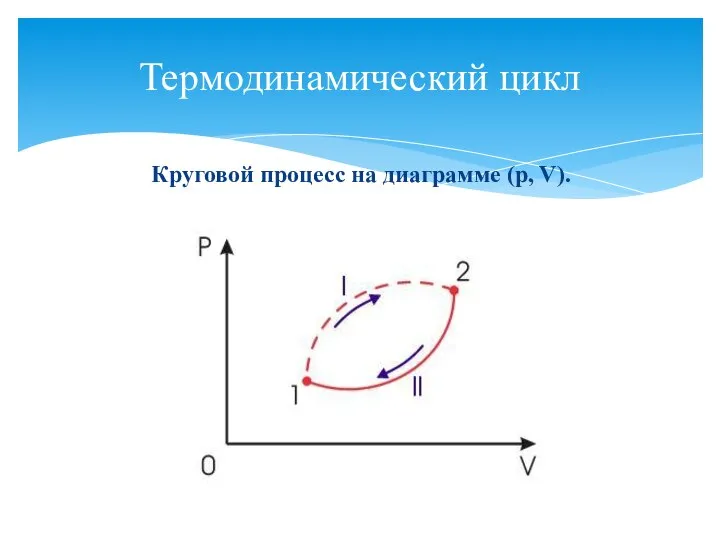
- 6. Термодинамический цикл Круговой процесс на диаграмме (p, V).
- 7. Представьте себе. . . вы ломаете яйцо или случайно разбиваете чашку или тарелку. . .
- 8. . . . Почему нет? . . . Но вы когда-нибудь видели, как сломанное яйцо или
- 9. Энтропия Энтропия определяет неупорядоченность системы - количество различных способов, которыми могут располагаться частицы в системе. У
- 10. Энтропия определяет упорядоченость: Твердые тела имеют низкую энтропию, жидкости имеют более высокую энтропию, чем твердые тела,
- 11. Рассмотрим пример: Горячая чашка кофе охлаждается... Передача тепла ... но холодная чашка кофе никогда самопроизвольно не
- 12. Если бы охлаждение было обратимым, холодный кофе мог бы спонтанно нагреваться, получая тепловую энергию из воздуха
- 13. Второй закон термодинамики Второй з-н термодинамики указывает направление возможных энергетических превращений и тем самым выражает необратимость
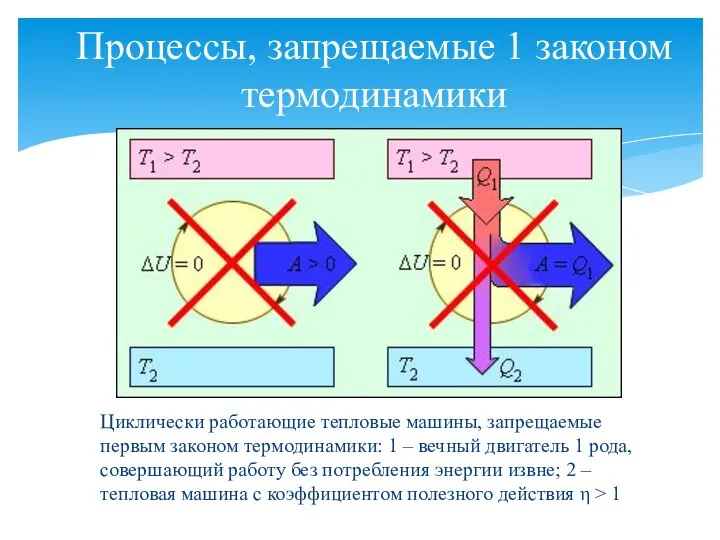
- 14. Процессы, запрещаемые 1 законом термодинамики Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный
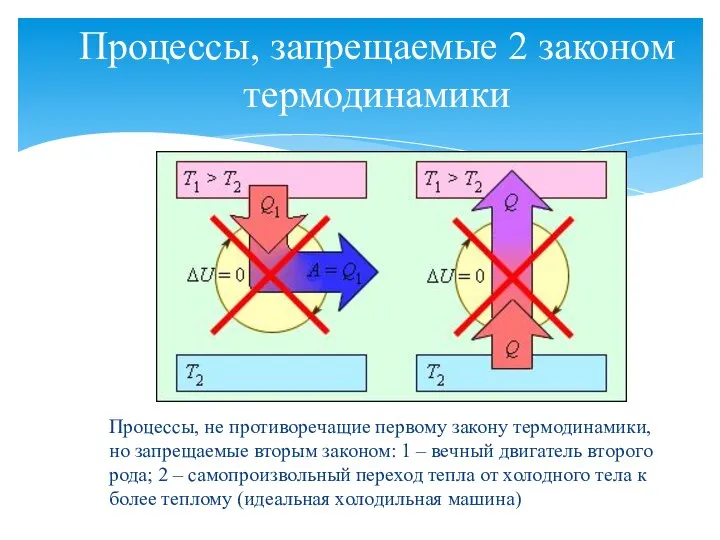
- 15. Процессы, запрещаемые 2 законом термодинамики Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1
- 16. Энтропия всегда увеличивается Это второй закон термодинамики в формулировке Л. Больцмана Полная энтропия замкнутой системы может
- 17. Цели урока: знать формулировку второго закона термодинамики; объяснять смысл второго закона термодинамики; применять второй закон термодинамики
- 18. Критерии оценивания: знаю формулировку второго закона термодинамики; объясняю смысл второго закона термодинамики; применяю второй закон термодинамики
- 20. Скачать презентацию












 Биомеханика. Кинематика. Относительность движения
Биомеханика. Кинематика. Относительность движения Постоянный электрический ток и его характеристики
Постоянный электрический ток и его характеристики Ядерный реактор
Ядерный реактор Презентация на тему Солнце и другие звезды
Презентация на тему Солнце и другие звезды  Презентация на тему Термометр
Презентация на тему Термометр  Уравнение неразрывности. Лекция 5
Уравнение неразрывности. Лекция 5 Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении
Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении Презентация на тему Электрическое поле (8 класс)
Презентация на тему Электрическое поле (8 класс)  Расчет производительности экструдеров
Расчет производительности экструдеров Как уменьшить силу трения
Как уменьшить силу трения Электрическая цепь и её составная часть
Электрическая цепь и её составная часть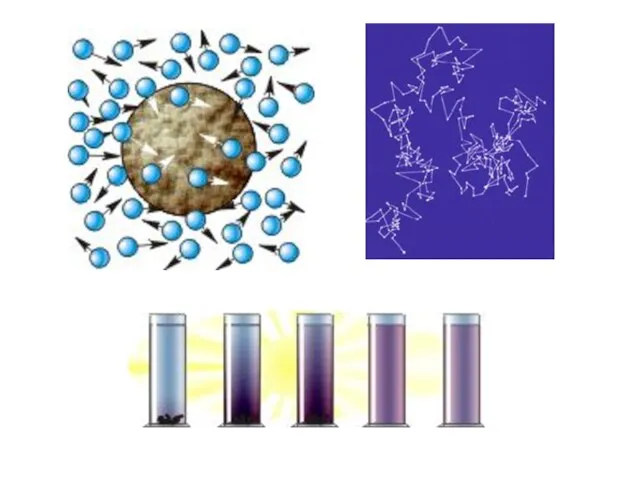 Тепловое движение
Тепловое движение Презентация к уроку _Инерциальные системы отсчета
Презентация к уроку _Инерциальные системы отсчета Видимое и ультрафиолетовое излучение
Видимое и ультрафиолетовое излучение рух по колу
рух по колу Автор: Тараканова Светлана школа № 14, 8 А класс
Автор: Тараканова Светлана школа № 14, 8 А класс Закон Снеллиуса (отражения) для монотипных волн
Закон Снеллиуса (отражения) для монотипных волн Электромагнитная совместимость в электроэнергетике
Электромагнитная совместимость в электроэнергетике Наглядное пособие для изучения шпоночного и штифтового соединений
Наглядное пособие для изучения шпоночного и штифтового соединений Электрический ток. Задачи
Электрический ток. Задачи Электрический ток в различных средах
Электрический ток в различных средах Явление электромагнитной индукции (эми). 11 класс
Явление электромагнитной индукции (эми). 11 класс Солнечная лаборатория
Солнечная лаборатория Результаты измерений. Лабораторная работа №3 по биофизике
Результаты измерений. Лабораторная работа №3 по биофизике Сила
Сила Изменение агрегатных состояний
Изменение агрегатных состояний Основы медицинской и биологической физики. Лекция 4. Часть 1
Основы медицинской и биологической физики. Лекция 4. Часть 1 Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации
Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации