Слайд 3История Алюминия
Родился Алюминий в 1827г.
Ф.Вёлер с помощью металлического калия получил загадочный металл

путём вытеснения его из расплава хлористого алюминия. Но в 1886г. Два химика Поль Эру и Чарльз Холи сделали открытие, которое позволило снизить затраты на производство Алюминия. Они обнаружили что в расплавленном минерале криолите неподатливый глинозем растворяется в горячем чае так же хорошо, как сахар. И если в этот раствор опустить электроды, то Аl начинает кристаллизироваться на катоде, надёжно закрытый от воды и кислорода коркой криолита.
Слайд 4Место жительства.
У каждого жителя ПСХЭ есть свой дом.
Живёт Алюминий в 13 доме

3-й области (3-й ряд) в 3-м районе (3-й период) в 1-ом квартале (1-я подгруппа).
Слайд 5Характеристика
Алюминий самый распространённый на земле металл.
Серебристо-белый, лёгкий, но механически прочный.

Он любит гостить у глин, полевых штапов, слюд и многих других минералов. Послушный: легко поддаётся обработке, легко вытягивается в проволоку, раскатывается в фольгу, отливается. Дружит с электричеством и теплом. Легко может подружиться с другими жителями ПСХЭ. Природный Алюминий состоит из одного изотопа.
Слайд 6Его физ. приметы.
Очень лёгкий. Плотность его равна 2,7кг/м в кубе. Атомный

вес 26,98. Электроотрицательность по Полингу 1,5. Атомный радиус его 0,143нм. По массе от всей Земли 8,8%. При температуре 660 градусов становится хрупким, легко ломается, его можно истолочь в порошок.
Слайд 7Его хим. приметы.
У атома Алюминия на внешнем энергетическом уровне находятся 3

электрона, которые он отдаёт при встрече с другими жителями страны ПСХЭ. При этих встречах он имеет степень окисления +3. Алюминий является сильным восстановителем. Он очень активный металл, но хитрый. Если он не хочет с кем либо встречаться (взаимодействовать), то он на открытом воздухе одевает тонкий, прочный, беспористый плащ. Это объясняет его высокую коррозийную стойкость.





 УРОКАлгебра 8 класс
УРОКАлгебра 8 класс Русский драматический театр
Русский драматический театр Аудитория Autonet.ru Москва, Март 2008
Аудитория Autonet.ru Москва, Март 2008 Искусство и костюм стиля МОДЕРН
Искусство и костюм стиля МОДЕРН Тема урока: Моделирование одежды. Профессия художника – модельера Цель урока: 1. Обобщить знания о приемах моделирования 2. Науч
Тема урока: Моделирование одежды. Профессия художника – модельера Цель урока: 1. Обобщить знания о приемах моделирования 2. Науч ПРАВОВАЯ ОТВЕТСТВЕННОСТЬ МОЛОДЕЖИ
ПРАВОВАЯ ОТВЕТСТВЕННОСТЬ МОЛОДЕЖИ Мастер - класс Вышивка крестом
Мастер - класс Вышивка крестом МАСЛЯНЫЕ РАДИАТОЫ NEOCLIMA 2011
МАСЛЯНЫЕ РАДИАТОЫ NEOCLIMA 2011 Презентация на тему Панда
Презентация на тему Панда Дэнас-вертебра. Принципиально новый способ стимуляции по типу бегущая волна
Дэнас-вертебра. Принципиально новый способ стимуляции по типу бегущая волна Темперамент и характер
Темперамент и характер Что и какие события могут по праву считаться всемирным наследием
Что и какие события могут по праву считаться всемирным наследием Грамматический чай
Грамматический чай primer_prezentatsii_PP_01_SV-97_2022
primer_prezentatsii_PP_01_SV-97_2022 Весна в картинах известных художников
Весна в картинах известных художников Психомоторное развитие детей. Семиотика нарушений психомоторного развития детей
Психомоторное развитие детей. Семиотика нарушений психомоторного развития детей Выбор одежды и поза ведущего во время тренинга
Выбор одежды и поза ведущего во время тренинга Классификация фотоаппаратов
Классификация фотоаппаратов В течение многих лет ученые, строители и производители искали универсальный строительный материал, имеющий необходимую прочность
В течение многих лет ученые, строители и производители искали универсальный строительный материал, имеющий необходимую прочность Презентация на тему Сельское хозяйство развитых и развивающихся стран (10 класс)
Презентация на тему Сельское хозяйство развитых и развивающихся стран (10 класс)  Модель построения предметно-развивающей среды в рамках проектной деятельности
Модель построения предметно-развивающей среды в рамках проектной деятельности Технология и аппаратура флотации. Применение флотации в производстве кормовых дрожжей
Технология и аппаратура флотации. Применение флотации в производстве кормовых дрожжей Анализ представленных субъектами Российской Федерации отчетов о достижении показателей результативности реализации субсидий
Анализ представленных субъектами Российской Федерации отчетов о достижении показателей результативности реализации субсидий Стартап. Поиск мечты
Стартап. Поиск мечты Презентация НИР (Шаблон) (2)
Презентация НИР (Шаблон) (2)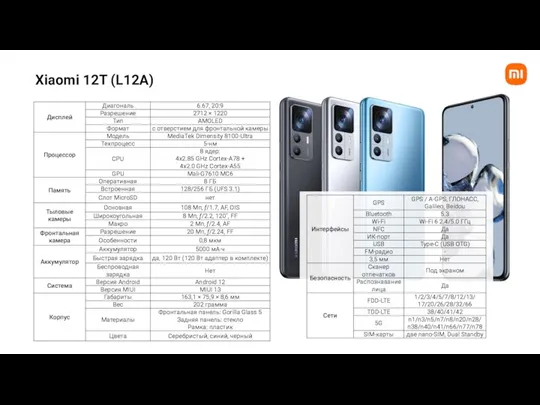 Xiaomi 12T (L12A) specs and KSP (1)[669]
Xiaomi 12T (L12A) specs and KSP (1)[669] Чего ты хочешь…^3^
Чего ты хочешь…^3^ К вопросу агентивности. Эволюция Ориентированного на Решение подхода
К вопросу агентивности. Эволюция Ориентированного на Решение подхода