Содержание
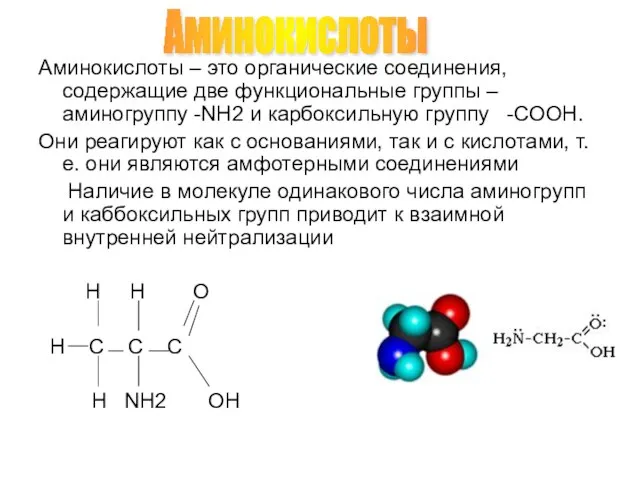
- 2. Аминокислоты – это органические соединения, содержащие две функциональные группы – аминогруппу -NH2 и карбоксильную группу -COOH.
- 3. Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Реагируют
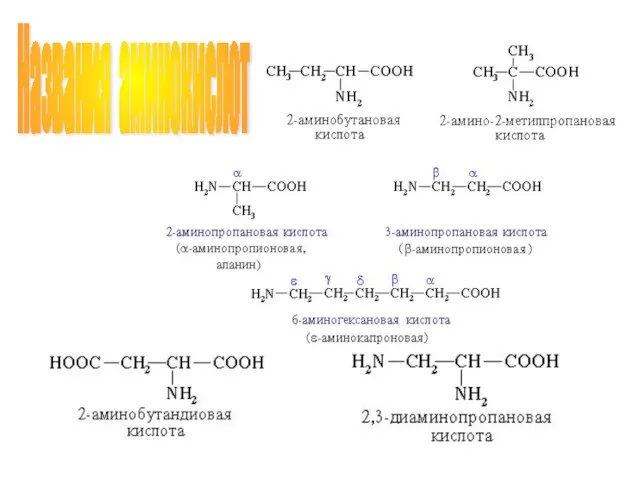
- 4. Названия аминокислот
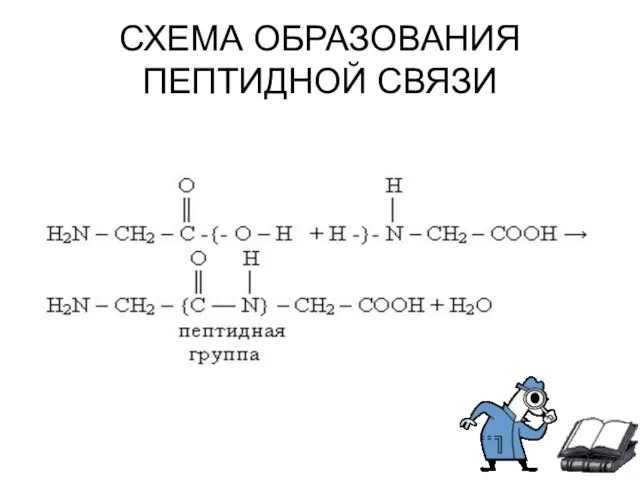
- 5. Аминокислоты могут реагировать друг с другом: карбоксильная группа одной аминокислоты реагирует с аминогруппой другой аминокислоты с
- 6. СХЕМА ОБРАЗОВАНИЯ ПЕПТИДНОЙ СВЯЗИ
- 7. Аминокислоты необходимы для синтеза белков в живых организмах. Главными поставщиками белков служат мясо, рыба, яйца, творог.
- 8. Белок – это высокомолекулярное органическое соединение, представляющее собой биополимер, состоящий из мономеров, которыми являются аминокислоты соединенные
- 9. В состав белка входят химические элементы: углерод C водород H2 кислород O2 азот азот N сера
- 10. По физическим свойствам белки делятся на : растворимые в воде нерастворимые в воде
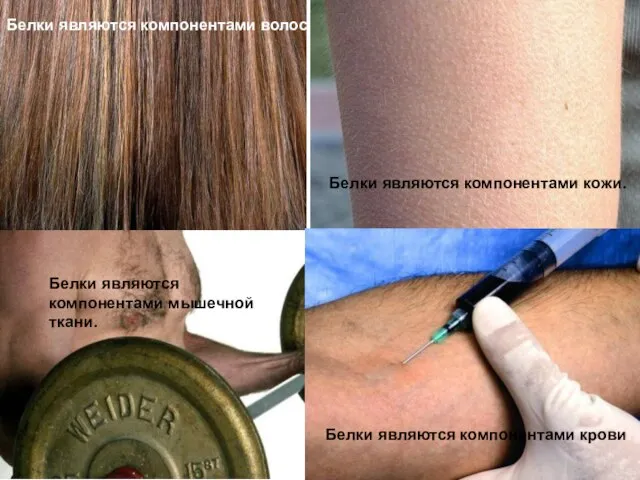
- 11. Белки являются компонентами волос Белки являются компонентами кожи. Белки являются компонентами мышечной ткани. Белки являются компонентами
- 12. В состав белков входят 20 αα - аминокислот, но их остатки могут многократно повторяться в самых
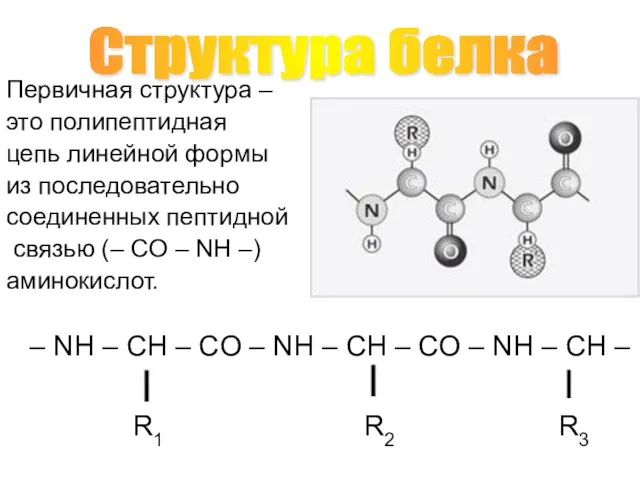
- 13. Первичная структура – это полипептидная цепь линейной формы из последовательно соединенных пептидной связью (– CO –
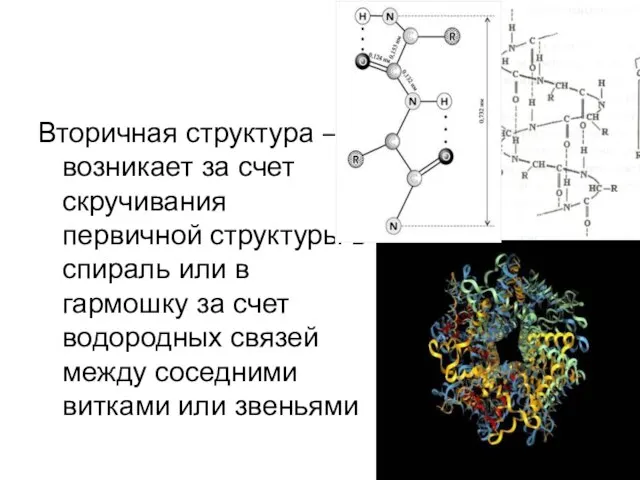
- 14. Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку за счет
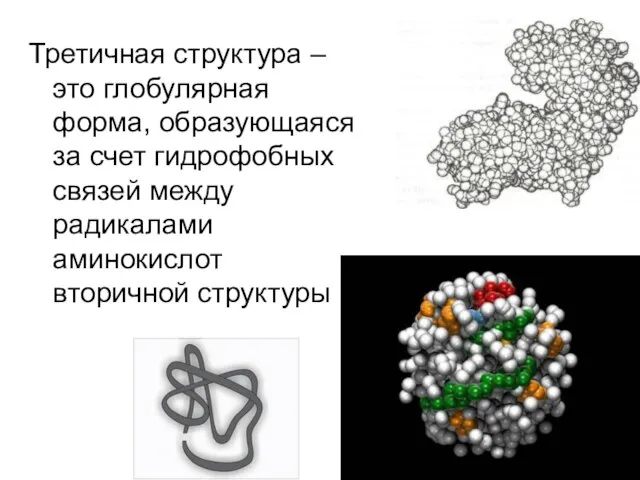
- 15. Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры
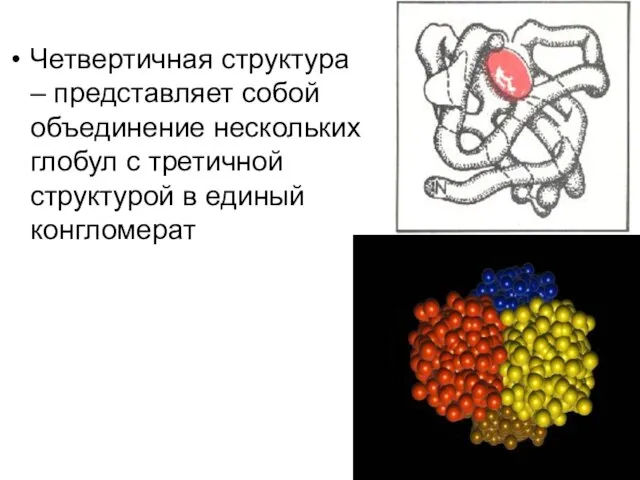
- 16. Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат
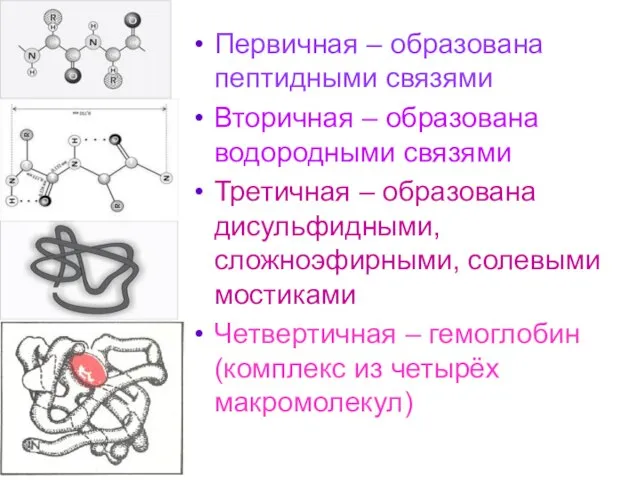
- 17. Первичная – образована пептидными связями Вторичная – образована водородными связями Третичная – образована дисульфидными, сложноэфирными, солевыми
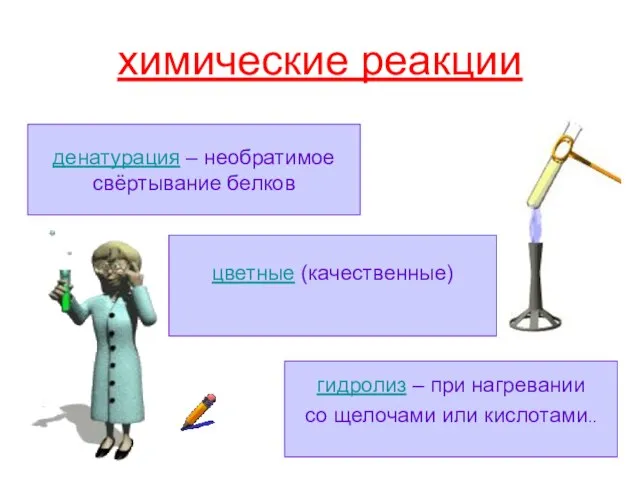
- 18. химические реакции цветные (качественные) денатурация – необратимое свёртывание белков гидролиз – при нагревании со щелочами или
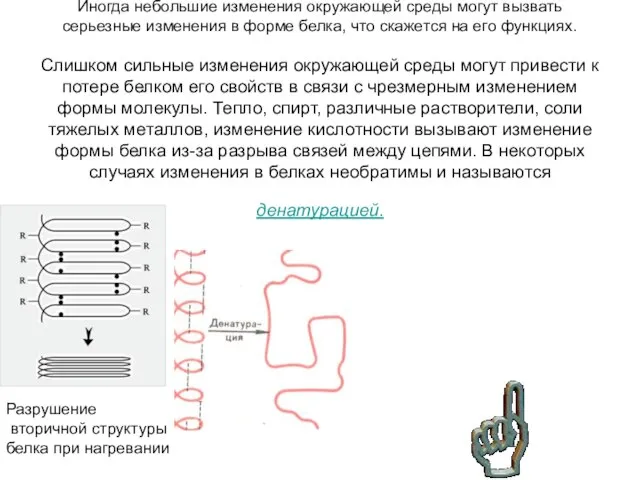
- 19. Иногда небольшие изменения окружающей среды могут вызвать серьезные изменения в форме белка, что скажется на его
- 20. Ксантопротеиновая реакция В пробирку налейте 2 мл раствора белка и добавьте по каплям 0,5 мл концентрированного
- 21. Схема гидролиза трипептида
- 22. Новые понятия: Гидролиз белков – разрушение первичной структуры белка. Денатурация – полное разрушение пространственной структуры белка.
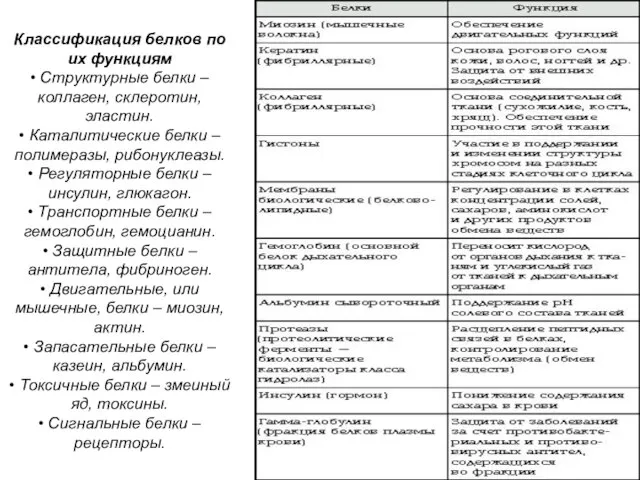
- 23. Классификация белков по их функциям • Структурные белки – коллаген, склеротин, эластин. • Каталитические белки –
- 24. Скорость обмена белковых тел 10 дней - 50 % белков печени и плазмы крови 80 дней
- 25. Норма белка в организме человека
- 26. Самостоятельная работа 1. Какие элементы входят в состав белка? 2. Какие вещества образуются при гидролизе белков?
- 27. Ответы: В состав молекулы белка входят: углерод, водород, кислород, азот, сера, фосфор, железо. При гидролизе белка
- 28. «Жизнь есть способ существования белковых тел…» (Ф.Энгельс)
- 29. Искусственное получение природных полипептидов возможно. Для этого необходимо знать, какие аминокислоты входят в состав молекулы, сколько
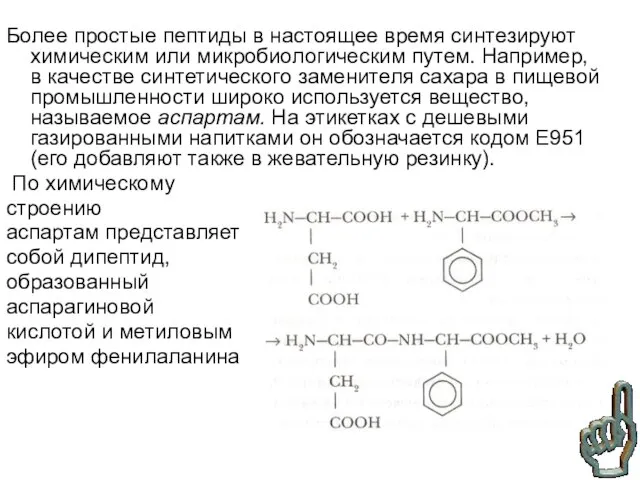
- 30. Более простые пептиды в настоящее время синтезируют химическим или микробиологическим путем. Например, в качестве синтетического заменителя
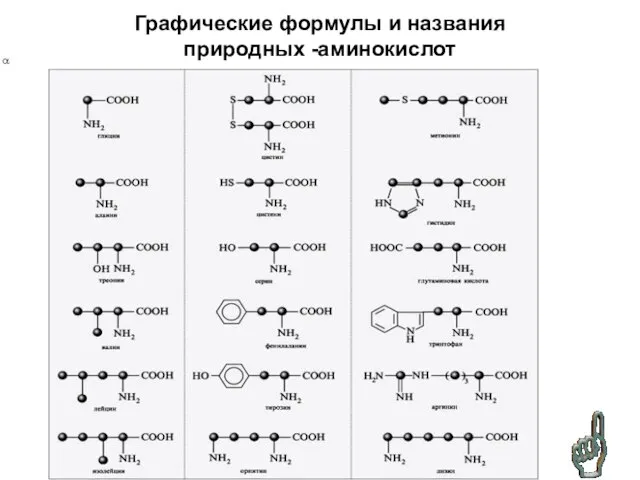
- 31. Графические формулы и названия природных -аминокислот
- 33. Скачать презентацию















 Терроризм
Терроризм  Государственные символы России
Государственные символы России РОССИЯв XVII векеСистема властии управления
РОССИЯв XVII векеСистема властии управления Класс Птицы. СОВООБРАЗНЫЕ
Класс Птицы. СОВООБРАЗНЫЕ Озера Евразии. Онежское озеро
Озера Евразии. Онежское озеро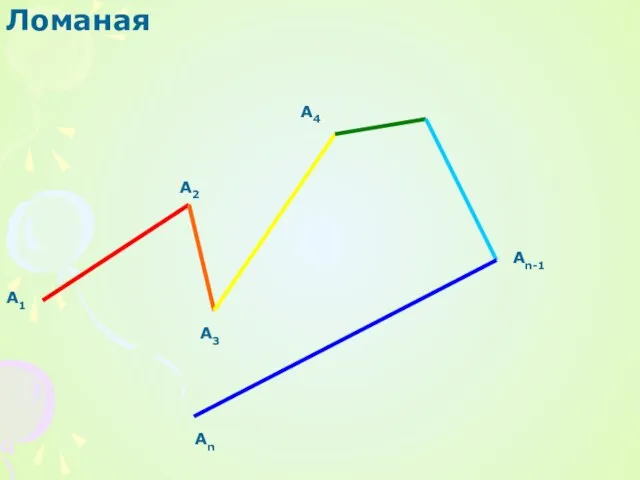 Презентация на тему Ломаная
Презентация на тему Ломаная профессиональноЕ самоопределениЕ молодежи в учреждениях начального и среднего профессионального образования
профессиональноЕ самоопределениЕ молодежи в учреждениях начального и среднего профессионального образования Пожарная безопасность
Пожарная безопасность Нарушения родительско-детских отношений как фактор риска развития патологии у детей
Нарушения родительско-детских отношений как фактор риска развития патологии у детей Traficante de drogas. Жанр игры: RPG, драма
Traficante de drogas. Жанр игры: RPG, драма Умножение вектора на число
Умножение вектора на число Народы Юго-Восточной Азии
Народы Юго-Восточной Азии Способы быстрого набора энергии. Курс Управление карьерой
Способы быстрого набора энергии. Курс Управление карьерой Рождение Иисуса и его версии
Рождение Иисуса и его версии Презентация на тему Саграда Фамилия
Презентация на тему Саграда Фамилия Гололед
Гололед по информатике
по информатике Информация вокруг нас
Информация вокруг нас Исследовательская
Исследовательская яна шапкина и данила гриднев
яна шапкина и данила гриднев Бабочки 3 класс
Бабочки 3 класс Влияние вредных привычек на внутриутробное развитие плода
Влияние вредных привычек на внутриутробное развитие плода Общероссийские антидопинговые правила
Общероссийские антидопинговые правила Медиакультура современного общества
Медиакультура современного общества Всероссийский телевизионный интернет-марафон "Финансовое просвещение из региона в регион" NON STOP
Всероссийский телевизионный интернет-марафон "Финансовое просвещение из региона в регион" NON STOP Анатомия конфликта. Конструктивные и деструктивные конфликты и пути преодаления
Анатомия конфликта. Конструктивные и деструктивные конфликты и пути преодаления Дидактические материалы к обобщающему уроку по курсу «ВОКРУГ ТЕБЯ – МИР…» АВТОР: Воронина Лариса Вячеславовна, учитель русского
Дидактические материалы к обобщающему уроку по курсу «ВОКРУГ ТЕБЯ – МИР…» АВТОР: Воронина Лариса Вячеславовна, учитель русского Концертная фотография
Концертная фотография