Содержание
- 2. Цель урока
- 3. Содержание
- 4. Определение Аминокислоты – бифункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH2 и карбоксильную
- 5. Строение Общая формула (NH2)mR(COOH)n, где m и n чаще всего равны 1 или 2. таким образом,
- 6. Классификация По числу функциональных групп: По взаимному расположению карбоксильной и аминогруппы По строению углеводородного радикала Аминокислоты
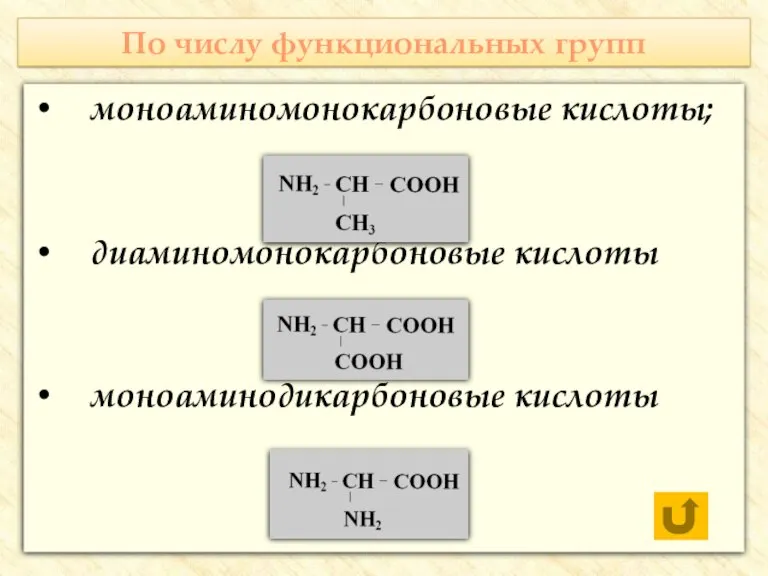
- 7. По числу функциональных групп моноаминомонокарбоновые кислоты; диаминомонокарбоновые кислоты моноаминодикарбоновые кислоты
- 8. По взаимному расположению карбоксильной и аминогруппы α –аминокислоты, β – аминокислоты, γ- аминокислоты, δ – аминокислоты,
- 9. По строению углеводородного радикала Предельные Непредельные Циклические Ароматические
- 10. Аминокислоты делят на: Природные Их около 150, они были обнаружены в живых организмах, около 20 из
- 11. Аминокислоты организма
- 12. Номенклатура Систематическая Рациональная Тривиальное
- 13. Систематическая номенклатура выбрать самую длинную цепь содержащую карбоксильную группу и аминогруппу; пронумеровать начиная с углерода карбоксильной
- 14. Рациональная номенклатура По рациональной номенклатуре положение аминогруппы указывается буквами греческого алфавита, начиная со второго атома углерода
- 15. Тривиальные названия Многие аминокислоты имеют тривиальные названия, например: Аланин
- 16. Изомерия Изомерия углеродного скелета; Изомерия положения функциональных групп; Межклассовая изомерия с нитросоединениями; Оптическая изомерия;
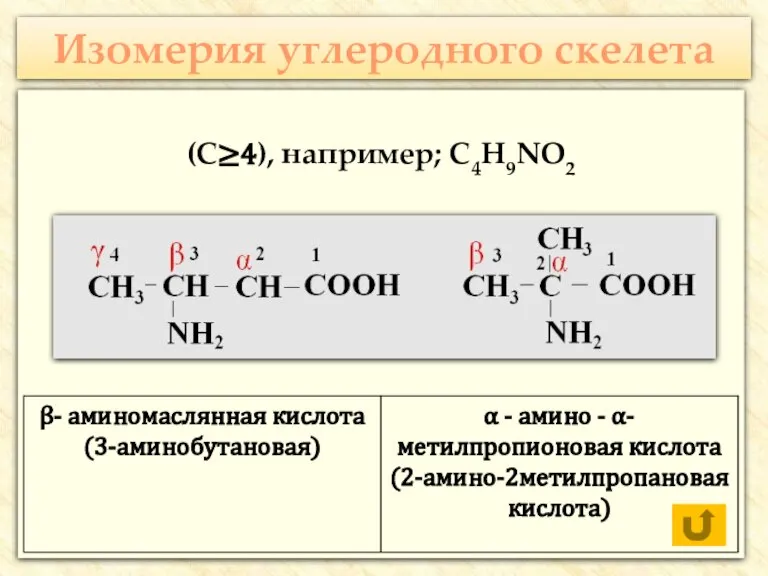
- 17. Изомерия углеродного скелета (С≥4), например; С4H9NO2
- 18. Изомерия положения функциональных групп (С≥3), например; С3H7NO2
- 19. Межклассовая с нитросоединениями (С≥2), например; С3H7NO2
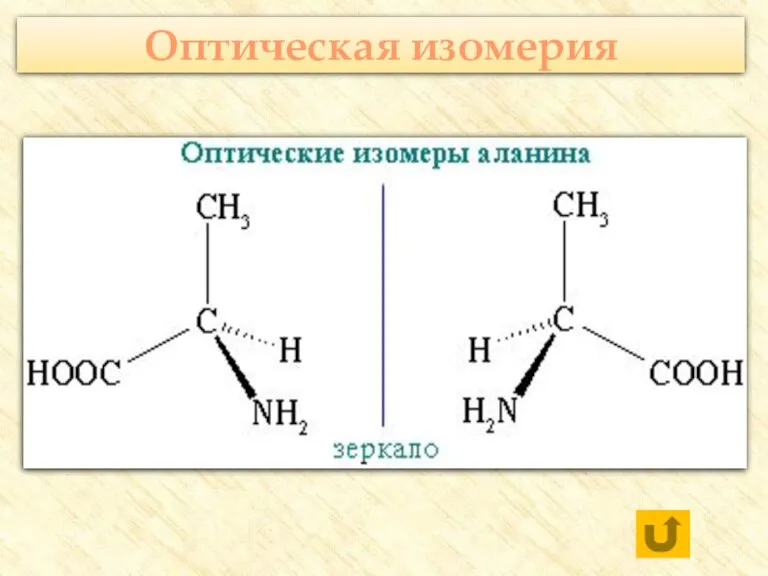
- 20. Оптическая изомерия
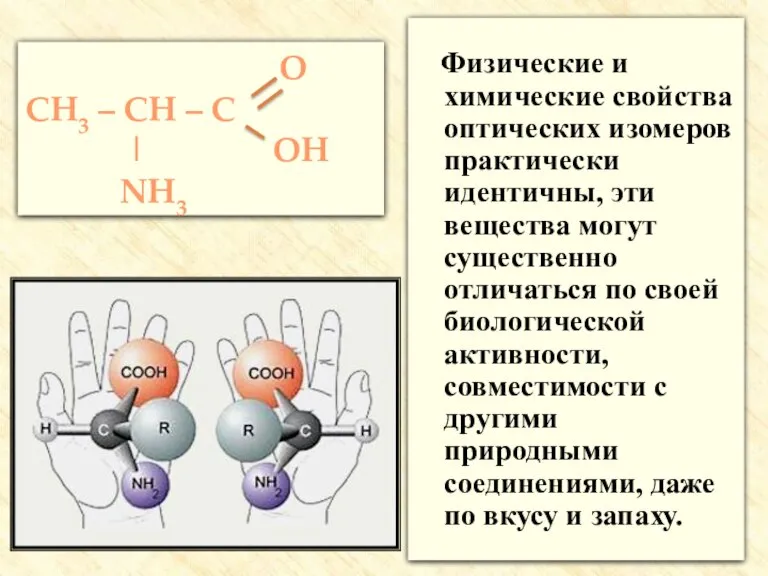
- 21. Физические и химические свойства оптических изомеров практически идентичны, эти вещества могут существенно отличаться по своей биологической
- 22. Физические свойства Аминокислоты – бесцветные кристаллические вещества с высокими температурами плавления. Плавятся с разложением, нелетучие. Хорошо
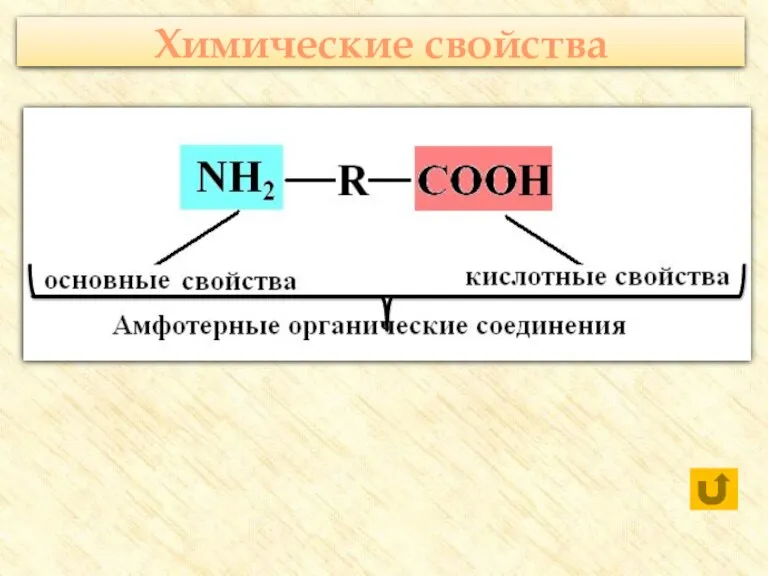
- 23. Химические свойства
- 24. Реакции с участием карбоксильной группы С активными металлами Оксидами металлов Гидроксидами металлов С солями слабых летучих
- 25. 1. Mg + 2NH2 – CH2 – COOH → (NH2 – CH2 – COO)2Mg + H2
- 26. Реакции с участием аминогруппы Взаимодействуют с кислотами: H2N–CH2–COOH + HCl → [H3N+–CH2–COOH] Cl-
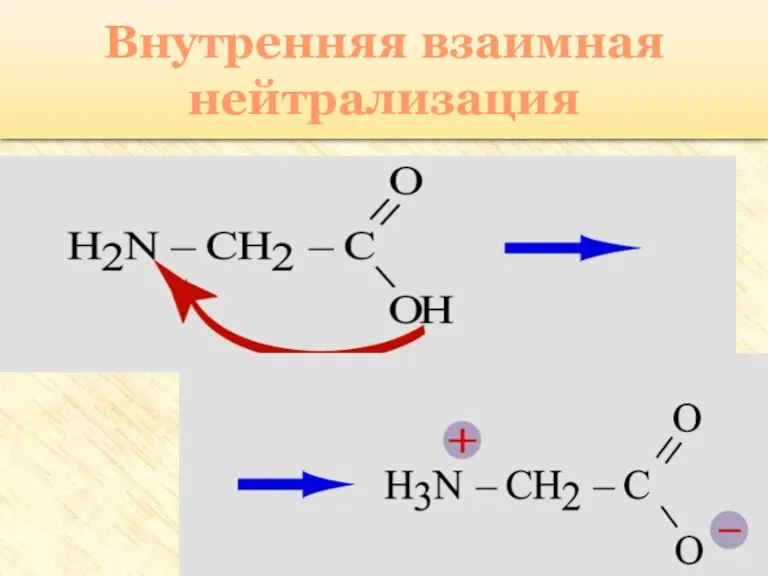
- 27. Особые свойства аминокислот Образование внутренней соли при диссоциации NH2 – CH2 – COOH ⇄ +NH3 –
- 28. Внутренняя взаимная нейтрализация
- 30. Особые свойства аминокислот 3. Декарбоксилирование : NH2 – CH2 – CH2 – COOH → NH2 –
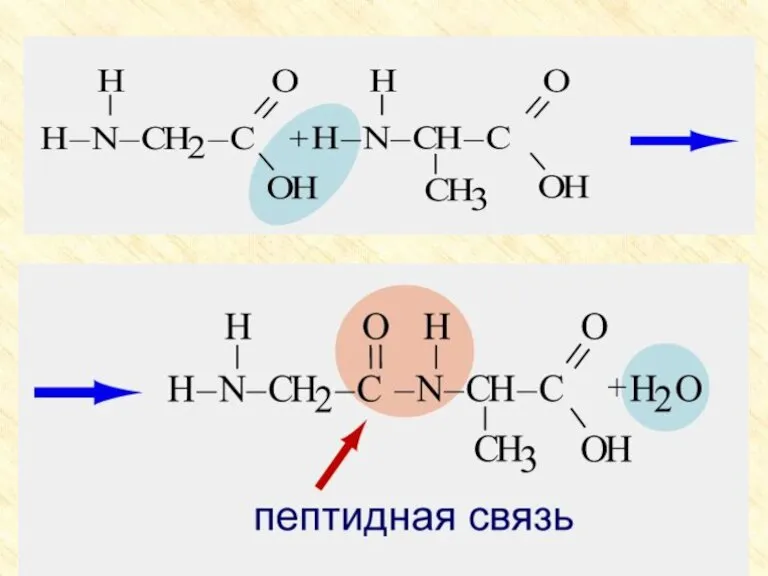
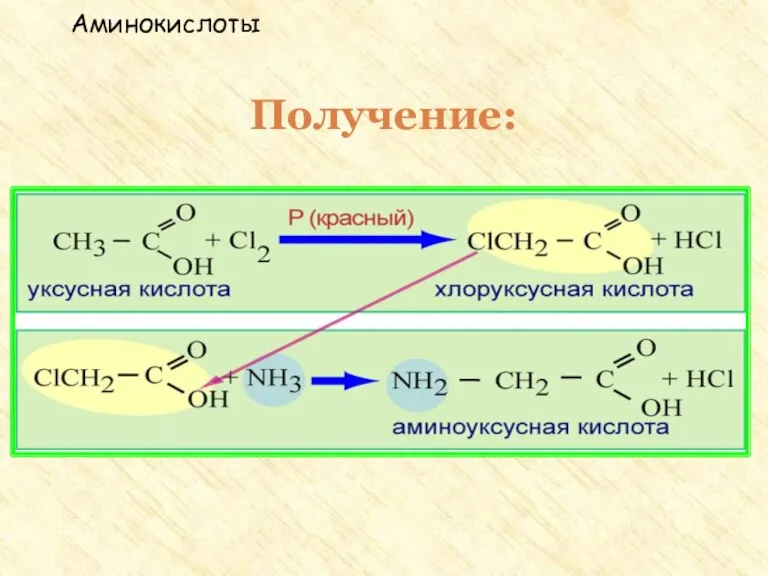
- 31. Получение аминокислот Гидролиз белков под влиянием ферментов, кислот или щелочей. Действие аммиака на хлорзамещенные органические кислоты:
- 32. Получение: 1. Гидролиз белков. Белок – полимер под действием воды распадается на мономеры - аминокислоты Аминокислоты
- 33. Применение аминокислот
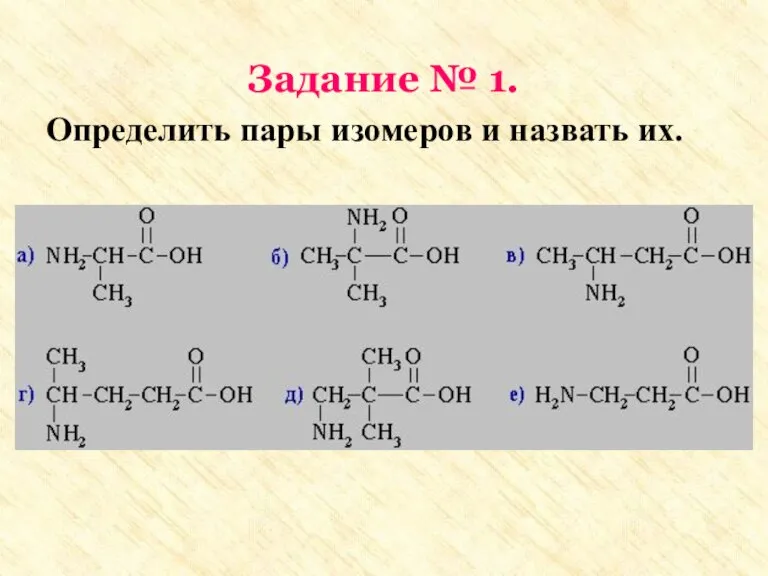
- 34. Задание № 1. Определить пары изомеров и назвать их.
- 35. Задача. Определите формулу аминокислоты, если массовые доли углерода, водорода, кислорода и азота соответственно равны: 48%, 9,34%,
- 37. Скачать презентацию



















![Реакции с участием аминогруппы Взаимодействуют с кислотами: H2N–CH2–COOH + HCl → [H3N+–CH2–COOH] Cl-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/336369/slide-25.jpg)





 Развеем мифы
Развеем мифы Как команда показывает, что проект опаздывает
Как команда показывает, что проект опаздывает Формирование духовно-нравственных ценностей в преподавании МХК
Формирование духовно-нравственных ценностей в преподавании МХК Федеральная налоговая служба приступила к исчислению налога на доходы физических лиц с применением штрафных санкций
Федеральная налоговая служба приступила к исчислению налога на доходы физических лиц с применением штрафных санкций Риск-менеджмент в системе экономической безопасности предприятия
Риск-менеджмент в системе экономической безопасности предприятия Склонение слов
Склонение слов Вини пух и пчелы
Вини пух и пчелы Упрочнение пород
Упрочнение пород Политические режимы
Политические режимы Презентация на тему Основы административного права
Презентация на тему Основы административного права  Межрегиональный образовательный форум «Открытое образовательное пространство: живая праКтика тьюторства»
Межрегиональный образовательный форум «Открытое образовательное пространство: живая праКтика тьюторства» Дистанционное обучение в рамках Moodle
Дистанционное обучение в рамках Moodle Понятие о деепричастии как особой форме глагола
Понятие о деепричастии как особой форме глагола Mentos Ascania Racing назаставке раллийной игры WRC
Mentos Ascania Racing назаставке раллийной игры WRC Город Псков
Город Псков Презентация на тему Сказка мудростью богата
Презентация на тему Сказка мудростью богата  Презентация на тему Борьба белорусского народа против германских оккупантов
Презентация на тему Борьба белорусского народа против германских оккупантов  Е. Чарушин "Страшный рассказ"
Е. Чарушин "Страшный рассказ" Создание музея школьных принадлежностей
Создание музея школьных принадлежностей Как играли наши бабушки
Как играли наши бабушки Метод разнополых дизиготных близнецовых пар как способ исследования пренатальных факторов формирования индивидуальных различий
Метод разнополых дизиготных близнецовых пар как способ исследования пренатальных факторов формирования индивидуальных различий Исполнение федерального бюджета Минрегионом России в 2011 году и бюджетные ассигнования на 2012 -2014 годы
Исполнение федерального бюджета Минрегионом России в 2011 году и бюджетные ассигнования на 2012 -2014 годы Краткие сведения о Сергее Александровиче Есение. «Песнь о собаке»
Краткие сведения о Сергее Александровиче Есение. «Песнь о собаке» День профессии
День профессии «Оценка ситуации по выявлению немедицинского употребления психоактивных веществ (ПАВ) среди учащихся средних образовательных шк
«Оценка ситуации по выявлению немедицинского употребления психоактивных веществ (ПАВ) среди учащихся средних образовательных шк ОПЕРАЦИОННЫЕ СИСТЕМЫ, СРЕДЫ И ОБОЛОЧКИ
ОПЕРАЦИОННЫЕ СИСТЕМЫ, СРЕДЫ И ОБОЛОЧКИ Презентация на тему Логистика и Интернет
Презентация на тему Логистика и Интернет ИПОТЕКА ТРАНШАМИ
ИПОТЕКА ТРАНШАМИ