Содержание
- 2. Цель проекта изучить процесс коррозии металлов в различных средах на примере железа.
- 3. Задачи Изучить литературу и другие источники информации по теме исследования 2. Определить экспериментальным путём влияние различных
- 4. Содержание Введение 1. Литературный обзор. 1.1. Понятие коррозии 1.2. Классификация коррозионных процессов. 1.2.1. По типу разрушений.
- 5. Понятие коррозии. Коррозия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического
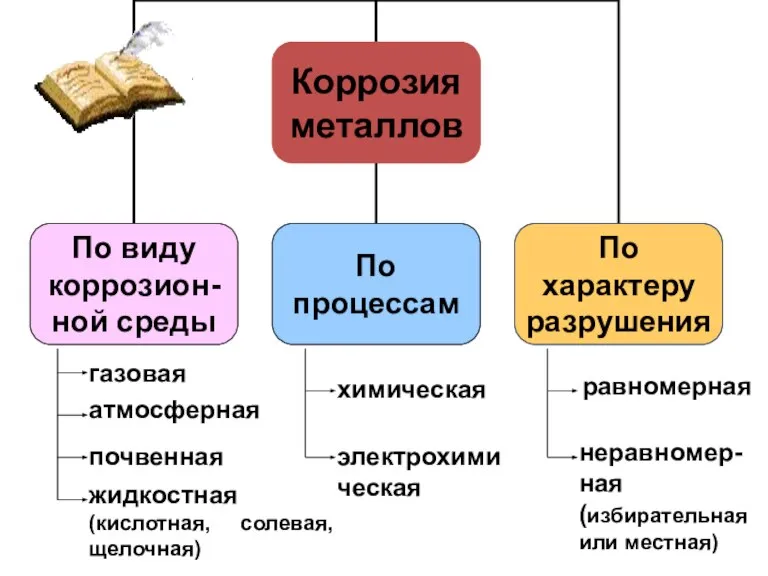
- 6. газовая атмосферная почвенная жидкостная (кислотная, солевая, щелочная) химическая электрохимическая равномерная неравномер- ная (избирательная или местная)
- 7. Коррозия металла. Ржавчина, самый распространенный вид коррозии.
- 8. Учёные, занимавшиеся изучением процессов коррозии. Якоби Б.С.-открытие гальванопластики. Бекетов Н.Н.-основоположник физической химии , академик Петербугской АН
- 9. Практическая часть Для исследования было взято 7 железных пластинок примерно одинакового размера и формы.
- 10. Все пластинки были помещены в стаканы с различной средой: 1.Вода 2.Слабый раствор KOH 3. Слабый раствор
- 11. Результаты 1. Водный раствор
- 12. Результаты 2.Слабый щелочной раствор
- 13. Результаты 3. Раствор фосфорной кислоты
- 14. Результаты 4. Раствор фосфорной кислоты более концентрированый
- 15. Результаты 5.Раствор поваренной соли
- 16. Результаты опытов 6.Слабокислый раствор соляной кислоты
- 17. Выводы Результаты исследования показали, что самой агрессивной средой для железа стала вода, раствор соляной кислоты и
- 18. Необходимость осуществления мероприятий по защите от коррозии диктуется тем обстоятельством, что потери от коррозии приносят чрезвычайно
- 19. СПОСОБЫ ЗАЩИТЫ ОТ КОРРОЗИИ Нанесение защитных покрытий (лаки, краски, эмали); Покрытие другим металлом (позолота, серебрение, хромирование,
- 20. Классификация коррозионных процессов. По типу разрушений. По типу разрушений коррозия бывает сплошной и местной. При равномерном
- 21. Химическая коррозия: Химическая коррозия: Химическая коррозия — взаимодействие поверхности металла с (коррозионно-активной) средой, В этом случае
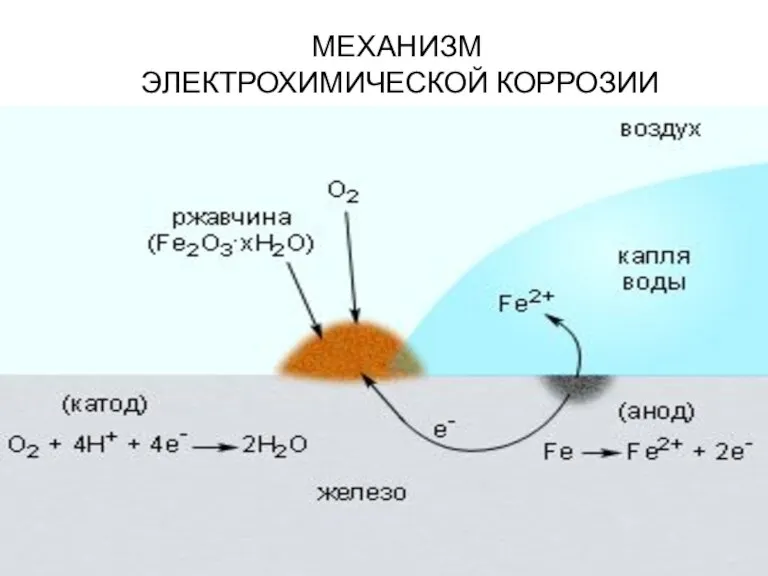
- 22. МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ
- 23. Электрохимическая коррозия: Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. В
- 24. Особенно разнообразные процессы химической коррозии встречаются в различных химических производствах. В атмосфере водорода, метана и других
- 25. Водородная и кислородная коррозия Если происходит восстановление ионов H3O+ или молекул воды H2O, говорят о водородной
- 27. Скачать презентацию






















 Презентация на тему Мировые природные ресурсы
Презентация на тему Мировые природные ресурсы  Карта желаний
Карта желаний Разработка высоконагруженных проектов(например – сайтов для сообществ)
Разработка высоконагруженных проектов(например – сайтов для сообществ) Финансовые бюджеты: особенности разработки
Финансовые бюджеты: особенности разработки «Восславим женщину-мать, чья любовь не знает преград, чьей грудью вскормлен весь мир! Всё прекрасное в человеке от лучей солнца и
«Восславим женщину-мать, чья любовь не знает преград, чьей грудью вскормлен весь мир! Всё прекрасное в человеке от лучей солнца и Новые решения для превосходного кондиционирования с дополнительным преимуществом мультифункционального загущения передовых ПА
Новые решения для превосходного кондиционирования с дополнительным преимуществом мультифункционального загущения передовых ПА Звук [Ш]
Звук [Ш] ПОРТФОЛИО
ПОРТФОЛИО Презентация
Презентация 2 Университет Прикладных Наук Аванс /Avans University of Applied Sciences Летняя школа /Summer course 2012 An exciting challenge for young internationals.
2 Университет Прикладных Наук Аванс /Avans University of Applied Sciences Летняя школа /Summer course 2012 An exciting challenge for young internationals. Подобные слагаемые
Подобные слагаемые История развития информационных технологий
История развития информационных технологий Способности и мотивация
Способности и мотивация ПРЕЗЕНТАЦИЯ к внеклассному мероприятию по русскому языку Учителя русского языка и литературы Власовой М.В.
ПРЕЗЕНТАЦИЯ к внеклассному мероприятию по русскому языку Учителя русского языка и литературы Власовой М.В. Опыт функционирования сайта www.fsb.ru в кризисных ситуациях полковник Правиков Д.И.
Опыт функционирования сайта www.fsb.ru в кризисных ситуациях полковник Правиков Д.И. Перспективы развития нефтеперерабатывающего комплексаОАО АНК «Башнефть»
Перспективы развития нефтеперерабатывающего комплексаОАО АНК «Башнефть» Презентация на тему Радиоактивность. Ядерные реакции
Презентация на тему Радиоактивность. Ядерные реакции Птицеград
Птицеград Информационные компьютерные технологии в практике логопеда
Информационные компьютерные технологии в практике логопеда Всероссийский налоговый диктант: участвуем вместе!
Всероссийский налоговый диктант: участвуем вместе! USA Etiquette
USA Etiquette Приложение № 4 к ВХ.3196 от 02.07.2020 09_35_35 (58638459 v1)
Приложение № 4 к ВХ.3196 от 02.07.2020 09_35_35 (58638459 v1) Видеонаблюдение (1)
Видеонаблюдение (1) Мастера Сысольского района на юбилейной республиканской выставке декоративно-прикладного искусства и художественных промыслов
Мастера Сысольского района на юбилейной республиканской выставке декоративно-прикладного искусства и художественных промыслов "Времена года на Дону".
"Времена года на Дону". Самый прибыльный бизнес
Самый прибыльный бизнес Моё увлечение кошки и черепахи!
Моё увлечение кошки и черепахи! Формирование социальной среды и развитие внешних связей.
Формирование социальной среды и развитие внешних связей.