Слайд 2ОПРЕДЕЛЕНИЕ
Раствор – это термодинамически устойчивая гомогенная система (фаза) переменного состава

Слайд 3СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ
Мольная доля – отношение числа молей i-го компонента раствора

к общему числу молей:
ВОПРОС: чему равна сумма мольных долей всех компонентов?
Молярная концентрация (молярность) – число молей растворенного вещества в одном литре (кубическом дециметре) раствора:
ВОПРОС: какова размерность молярности раствора?
Слайд 4СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ
Моляльность – число молей i-го компонента, приходящееся на 1000

г растворителя:
ВОПРОС: какова размерность моляльности раствора?
Слайд 5ИДЕАЛЬНЫЙ РАСТВОР
раствор, в котором молекулы растворителя взаимодействуют с растворенным веществом так же,

как взаимодействуют между собой молекулы растворителя и между собой - молекулы растворенного вещества
энергия взаимодействия разнородных молекул равна средней энергии взаимодействия однородных молекул:
Слайд 6ОБРАЗОВАНИЕ ИДЕАЛЬНОГО РАСТВОРА
не сопровождается тепловым эффектом
ΔHсмеш=0
не сопровождается изменением объема
ΔVсмеш=0
изменение энтропии равно

изменению энтропии при смешении идеальных газов
ΔSсмеш=ΔSид
Слайд 7МОДЕЛИ НЕИДЕАЛЬНЫХ РАСТВОРОВ
предельно разбавленный раствор, в котором растворитель подчиняется законам идеальных растворов,

а растворенное вещество не подчиняется
регулярный раствор, в котором взаимодействие частиц приводит к изменению энтальпии и объема системы, в то время как изменение энтропии соответствует изменению при смешении идеальных газов
Слайд 8МОДЕЛИ НЕИДЕАЛЬНЫХ РАСТВОРОВ
атермальный раствор, в котором взаимодействие частиц приводит к изменению объема,

к изменени энтропии, не отвечающему смешению идеальных газов, в то время как тепловой эффект смешения равен нулю
ассоциированный раствор, в котором наряду с ван-дер-ваальсовыми межмолекулярными взаимодействиями имеются специфические, близкие по характеру к слабой химической связи
Слайд 9КОЛЛИГАТИВНЫЕ СВОЙСТВА ИДЕАЛЬНЫХ И НЕИДЕАЛЬНЫХ РАСТВОРОВ
1. Давление пара летучего компонента (например, растворителя)

над идеальным раствором пропорционально мольной доле этого компонента в растворе (закон Рауля)
ЗАДАНИЕ. Запишите уравнение закона Рауля и рассчитайте давление пара растворителя над раствором, в котором мольная доля растворенного вещества равна 0,01, а давление пара чистого растворителя равно 6000 Па.
Слайд 101А. ОТКЛОНЕНИЯ ОТ ЗАКОНА РАУЛЯ
Положительные: давление пара летучего компонента превышает рассчитанное по

закону Рауля
ВОПРОС: каким тепловым эффектом сопровождается образование неидеального раствора с положительными отклонениями от идеальности? Почему?
Отрицательные: давление пара летучего компонента ниже рассчитанного по закону Рауля
ВОПРОС: каким тепловым эффектом сопровождается образование неидеального раствора с положительными отклонениями от идеальности? Почему?
Слайд 112. ДАВЛЕНИЕ ПАРА РАСТВОРЕННОГО ВЕЩЕСТВА
Растворимость двухатомных газов в металлах пропорциональна корню квадратному

из их парциального давления (закон Сивертса)
ЗАДАНИЕ: Выведите уравнение закона Сивертса.
Растворимость газа в жидкости пропорциональна его парциальному давлению (закон Генри)
ЗАДАНИЕ: Объясните, как меняется растворимость газа в воде при повышении температуры
Слайд 123. ПОНИЖЕНИЕ ТЕМПЕРАТУРЫ ЗАМЕРЗАНИЯ И ПОВЫШЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ РАСТВОРА
Изменение химического потенциала растворителя
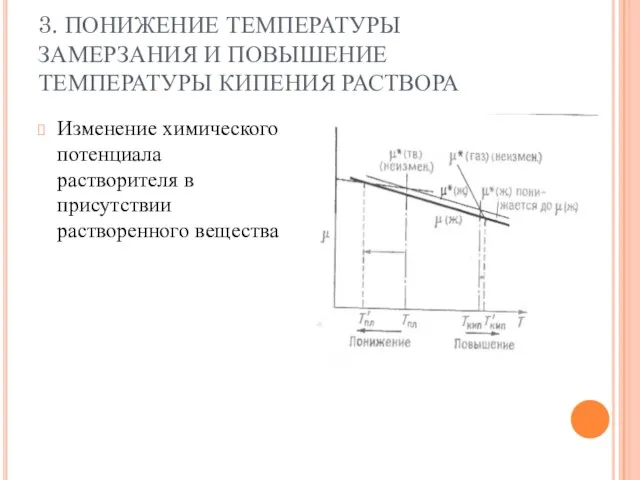
в присутствии растворенного вещества
Слайд 133А. КРИОСКОПИЧЕСКИЙ И ЭБУЛИОСКОПИЧЕСКИЙ ЭФФЕКТЫ
ΔТ(замерзания) = Кm
К – криоскопическая константа (зависит только

от свойств растворителя)
m – моляльность раствора
ΔТ(кипения) = Еm
Е – эбулиоскопическая константа (зависит только от свойств растворителя)
m – моляльность раствора
ВОПРОС: каково практическое значение этих эффектов? Приведите два-три примера.












 Сложение и вычитание смешанных чисел
Сложение и вычитание смешанных чисел Агентам по продаже услуг ООО «АТОН»
Агентам по продаже услуг ООО «АТОН» Трудовые права молодежи
Трудовые права молодежи Цветок ветренницы - праобраз колеса
Цветок ветренницы - праобраз колеса Как читать книгу
Как читать книгу Правописание НЕ
Правописание НЕ Презентация на тему Биологические особенности раннецветущих растений
Презентация на тему Биологические особенности раннецветущих растений  Презентация на тему С огнем не играй - пожар не затевай!
Презентация на тему С огнем не играй - пожар не затевай! Планирование расходов в период подготовки и проведения выборов в единый день голосования
Планирование расходов в период подготовки и проведения выборов в единый день голосования Номинация Рукоделие
Номинация Рукоделие Казахский университет международных отношений и мировых языков имени Абылай хана
Казахский университет международных отношений и мировых языков имени Абылай хана Оптический принцип записи и считывания информации
Оптический принцип записи и считывания информации Presentation Title
Presentation Title  Психолого-педагогическая характеристика и развивающие занятия для детей раннего возраста
Психолого-педагогическая характеристика и развивающие занятия для детей раннего возраста ИСПОЛНЕНИЕ БЮДЖЕТА МО ТЮМЕНСКИЙ МУНИЦИПАЛЬНЫЙ РАЙОН за 1 полугодие 2011 года
ИСПОЛНЕНИЕ БЮДЖЕТА МО ТЮМЕНСКИЙ МУНИЦИПАЛЬНЫЙ РАЙОН за 1 полугодие 2011 года Практикум по проектной деятельности в социальных организациях (в рамках стажёрской практики студентов)
Практикум по проектной деятельности в социальных организациях (в рамках стажёрской практики студентов) Совет по профориентации УГНТУ
Совет по профориентации УГНТУ Организация технического обслуживания и ремонта высоковольтных выключателей
Организация технического обслуживания и ремонта высоковольтных выключателей Стипендиальные программы
Стипендиальные программы 5 причин, почему для Вашего бренда будет полезно выиграть 500 000 грн на медиа-размещение в соцсетиОдноклассники
5 причин, почему для Вашего бренда будет полезно выиграть 500 000 грн на медиа-размещение в соцсетиОдноклассники Повторение
Повторение Монтаж соединения проводов с помощью сварки
Монтаж соединения проводов с помощью сварки Распространение ППО в системе образования Варгашинского района как ресурс развития учительского потенциала
Распространение ППО в системе образования Варгашинского района как ресурс развития учительского потенциала Создание цветочного салона
Создание цветочного салона Поход за грибами
Поход за грибами Развитие познавательной активности на уроках «Человек и мир»
Развитие познавательной активности на уроках «Человек и мир» Олеиновая кислота
Олеиновая кислота SMM, SEO, Баннеры – в чем отличие?
SMM, SEO, Баннеры – в чем отличие?