Содержание
- 2. Непредельные – углеводороды, содержащие между атомами углерода одну или несколько π- связей Непредельные углеводороды Алкены С=С
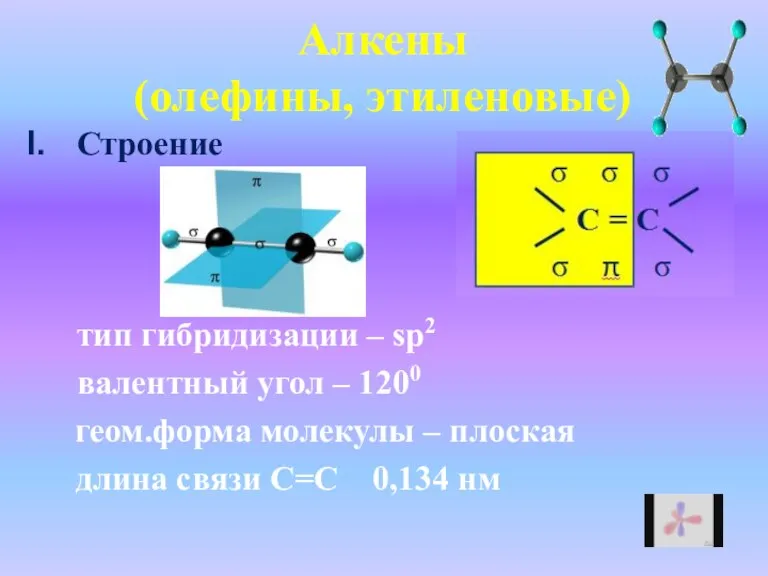
- 3. Алкены (олефины, этиленовые) Строение тип гибридизации – sp2 валентный угол – 1200 геом.форма молекулы – плоская
- 4. II. Гомологический ряд алкенов Составьте структурные и молекулярные формулы первых 3-х гомологов алкенов и, пользуясь Справочной
- 5. Контроль:
- 6. �Какова общая формула алкенов? СnH2n �
- 7. III.Изомерия и номенклатура алкенов. Просмотрите видеоролик о номенклатуре алкенов. Какой вид изомерии присущ как алканам, так
- 8. 4. Что ещё можно изменить в строении алкенов помимо углеродного скелета? 5.Какое минимальное количество атомов углерода
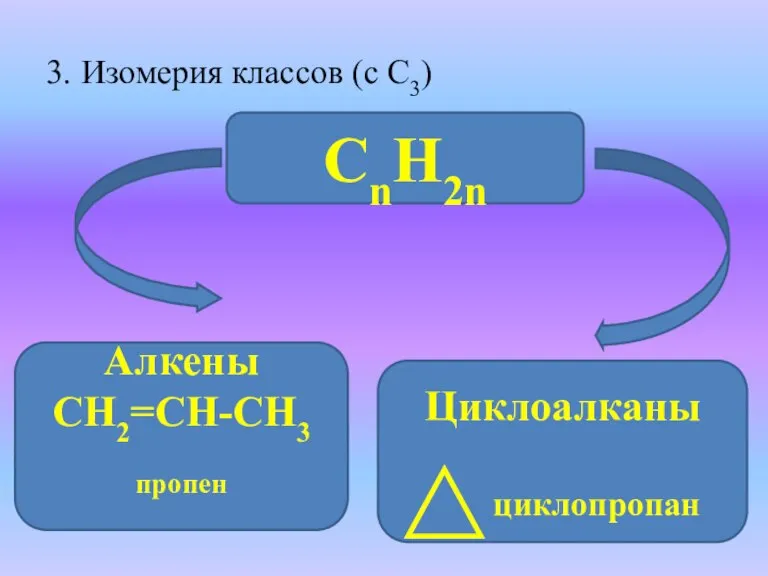
- 9. 3. Изомерия классов (с С3) СnH2n Алкены СН2=СН-СН3 пропен Циклоалканы циклопропан
- 10. Изомерия №№1-3 относится к структурной изомерии (положение атомов в пространстве не меняется)
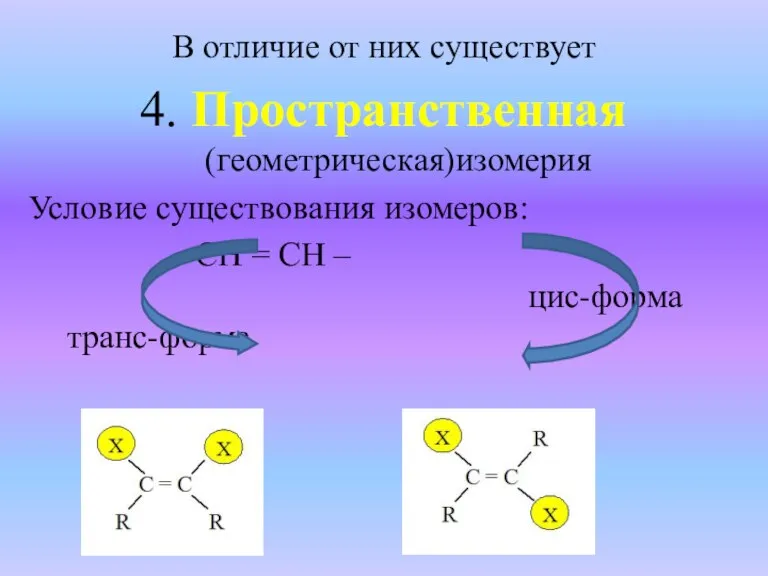
- 11. В отличие от них существует 4. Пространственная (геометрическая)изомерия Условие существования изомеров: – СН = СН –
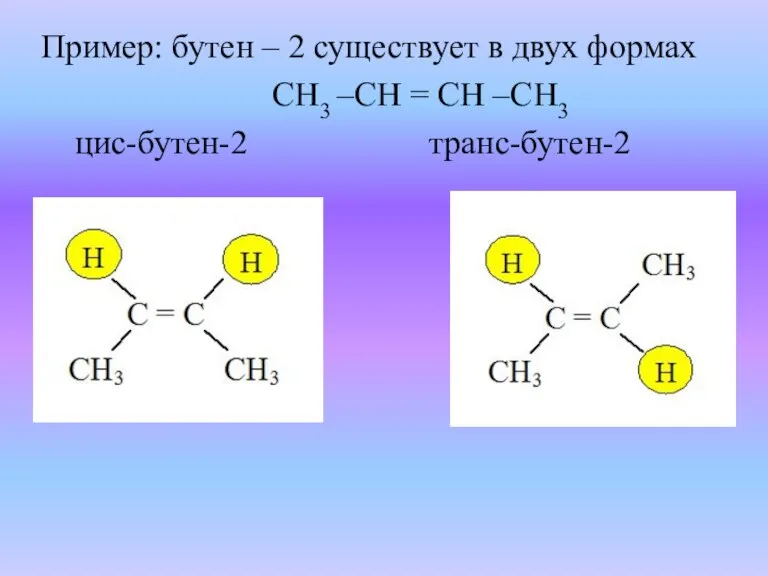
- 12. Пример: бутен – 2 существует в двух формах СН3 –СН = СН –СН3 цис-бутен-2 транс-бутен-2
- 13. Домашнее задание: § 9, стр.43 упр.2,4,8,9
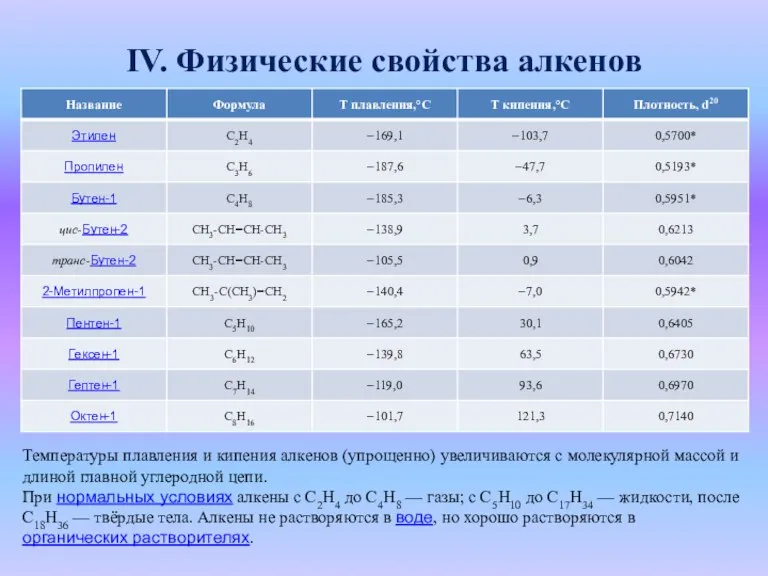
- 14. IV. Физические свойства алкенов Температуры плавления и кипения алкенов (упрощенно) увеличиваются с молекулярной массой и длиной
- 15. V. Химические свойства алкенов Какой тип химических свойств, связанный с составом, будет характерен для алкенов? ГОРЕНИЕ
- 16. Вопрос: Какой тип реакции, связанный со строением, будет характерен для всех непредельных углеводородов? Реакция присоединения Что
- 17. 2.1.Присоединение водорода (гидрирование) Составьте уравнение гидрирования пропилена (при нагревании, в присутствии катализатора). Назовите продукт реакции. СН3-СН=СН2
- 18. 2.3.Присоединение галогенводородов (гидрогалогенирование) Присоединение галогенводородов к гомологам этилена идет по правилу В.В.Марковникова: при обычных условиях водород
- 19. Составьте уравнение гидробромирования пропилена. Назовите продукт реакции. СН3-СН=СН2 + НBr ? СН3-СНBr - СН3 2.4.Присоединение воды
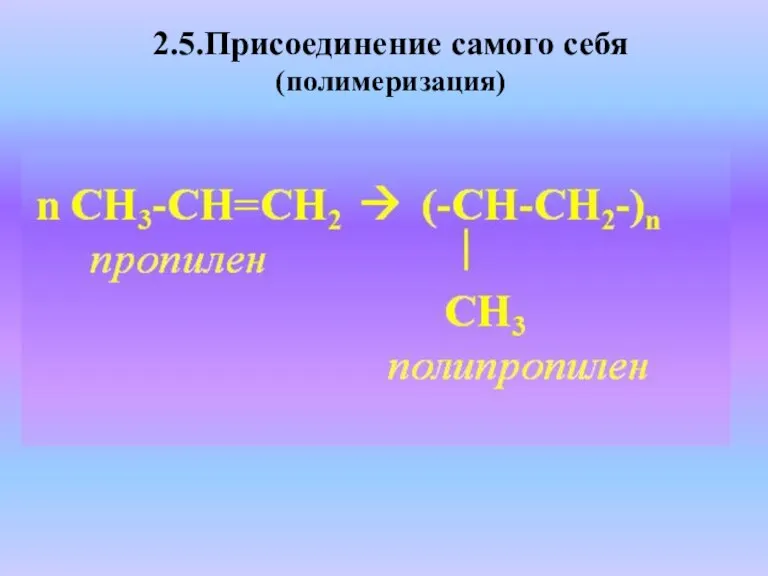
- 20. 2.5.Присоединение самого себя (полимеризация)
- 21. Вопрос: А возможны реакции разложения для этиленовых? Почему? 3. Реакции разложения (дегидрирования) Составьте уравнение дегидрирования пропилена.
- 22. Из природного газа и нефти Разложение(дегидрирование) алканов СnH2n+2? СnH2n + H2 (to, кат-р) 3. Разложение галогенпроизводных:
- 24. Скачать презентацию














 Об организации отдыха и оздоровления учащихся
Об организации отдыха и оздоровления учащихся Использование методов педагогической квалиметрии как средства оценки качества образования
Использование методов педагогической квалиметрии как средства оценки качества образования Порядок организации оздоровления и отдыха детей города Перми в 2012 году
Порядок организации оздоровления и отдыха детей города Перми в 2012 году П п
П п Готовимся к сочинению на лингвистическую тему
Готовимся к сочинению на лингвистическую тему 3 июля 2009 Тула Зона отдыха «Петушки» Пролетарский район
3 июля 2009 Тула Зона отдыха «Петушки» Пролетарский район Методика оценки дебиторской задолженности Национальной коллегии оценщиков
Методика оценки дебиторской задолженности Национальной коллегии оценщиков Presentation
Presentation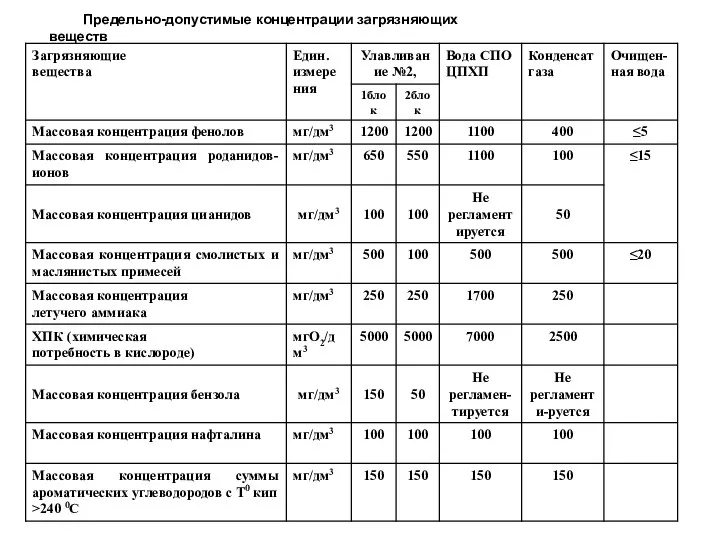 Предельно-допустимые концентрации загрязняющих веществ. Технологическая схема биохимической очистки сточных вод КХП
Предельно-допустимые концентрации загрязняющих веществ. Технологическая схема биохимической очистки сточных вод КХП Определение оптимального режима работы парогенератора АЭС с ВВЭР-1000
Определение оптимального режима работы парогенератора АЭС с ВВЭР-1000 Язык современной Интернет - субкультуры
Язык современной Интернет - субкультуры Сравнение интернета как рекламоносителя с другими медиа
Сравнение интернета как рекламоносителя с другими медиа Политическая деятельность
Политическая деятельность Портфоліо дізайнера
Портфоліо дізайнера Реализация федерального закона от 05.05.2014 №116-ФЗ О внесении изменений в отдельные законодательные акты РФ
Реализация федерального закона от 05.05.2014 №116-ФЗ О внесении изменений в отдельные законодательные акты РФ Участие граждан в решении проблем местных сообществ.Центры Активных Людей
Участие граждан в решении проблем местных сообществ.Центры Активных Людей Почему в России не будет работать закон о коррупции И.И. Елисеева, член-корреспондент РАН Социологический институт РАН
Почему в России не будет работать закон о коррупции И.И. Елисеева, член-корреспондент РАН Социологический институт РАН Правописание согласных в корне слова
Правописание согласных в корне слова Презентация на тему Знание и понимание
Презентация на тему Знание и понимание Теория справедливости Адамса
Теория справедливости Адамса Особенности истории информатики
Особенности истории информатики Отражение моего внутреннего мира в творчестве. Галичина Мария
Отражение моего внутреннего мира в творчестве. Галичина Мария Натуральное число
Натуральное число Система комплексной автоматизации Globus Professional v2.3.
Система комплексной автоматизации Globus Professional v2.3. «Готовность младших школьников к обучению в среднем звене»
«Готовность младших школьников к обучению в среднем звене» Республике Карелия
Республике Карелия Этюды о природе. Зима
Этюды о природе. Зима Генетика. Основные закономерности наследственности
Генетика. Основные закономерности наследственности