Слайд 2Бензол С6Н6 – родоначальник ароматических углеводородов.
Каждый из шести атомов углерода в его
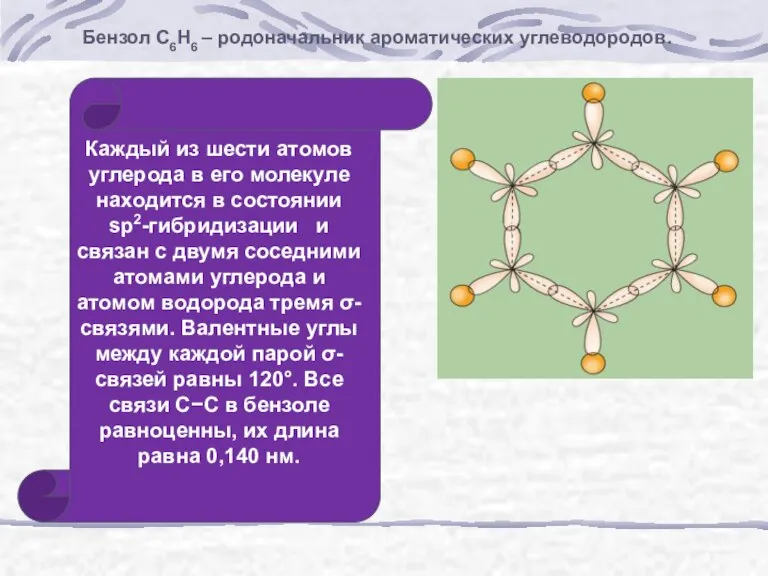
молекуле находится в состоянии sp2-гибридизации и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. Валентные углы между каждой парой σ-связей равны 120°. Все связи С−С в бензоле равноценны, их длина равна 0,140 нм.
Слайд 3р-электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2р-АО,
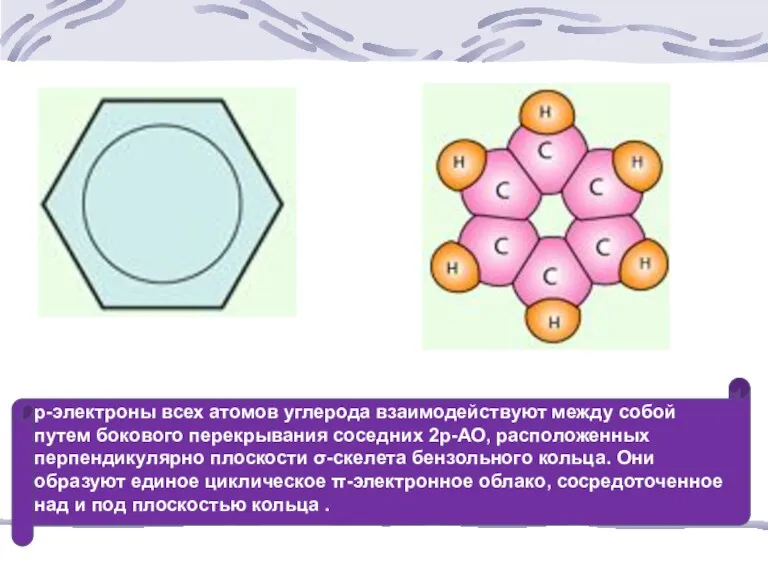
расположенных перпендикулярно плоскости σ-скелета бензольного кольца. Они образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца .
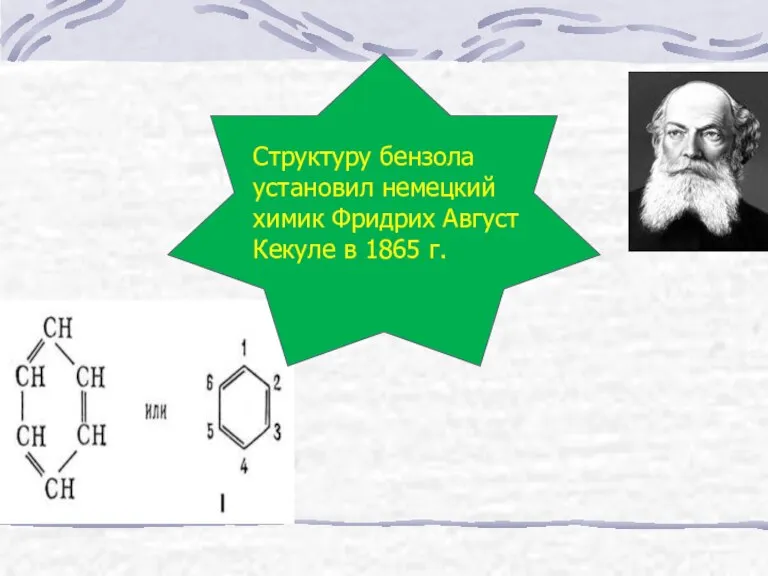
Слайд 4Структуру бензола установил немецкий химик Фридрих Август Кекуле в 1865 г.
Слайд 5Электронное строение бензола
Современное представление об электронной природе связей в бензоле основывается на
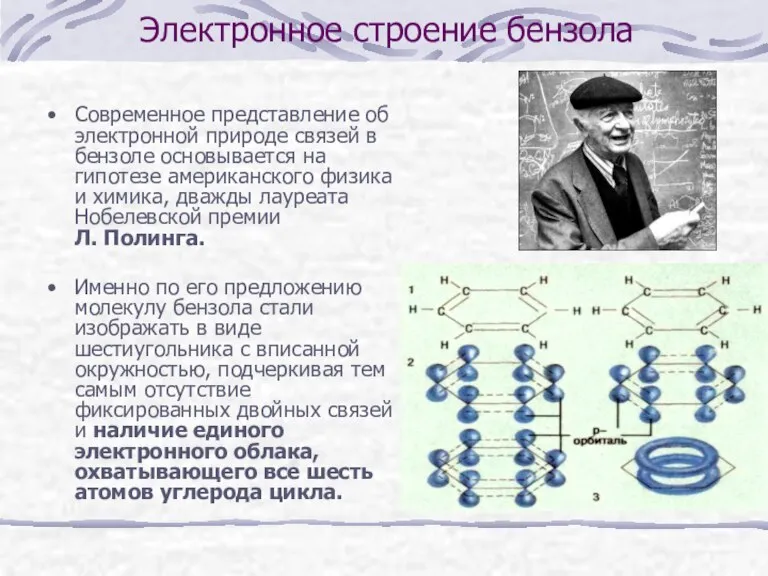
гипотезе американского физика и химика, дважды лауреата Нобелевской премии
Л. Полинга.
Именно по его предложению молекулу бензола стали изображать в виде шестиугольника с вписанной окружностью, подчеркивая тем самым отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла.
Слайд 6У Бензола изомеров нет.
У Метилбензола изомеров нет.
А у Этилбензола есть изомеры.
И у

Пропилбензола тоже есть изомеры
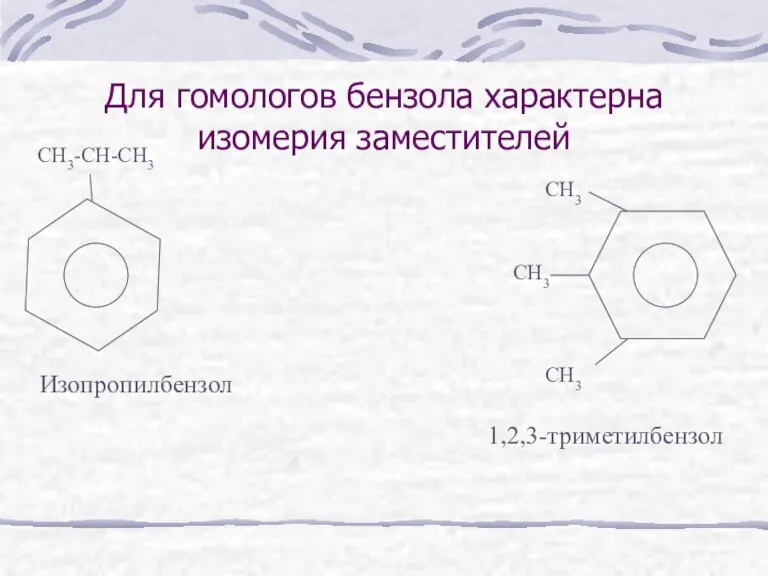
Слайд 7Для гомологов бензола характерна изомерия заместителей
CH3-CH-CH3
Изопропилбензол
CH3
CH3
CH3
1,2,3-триметилбензол
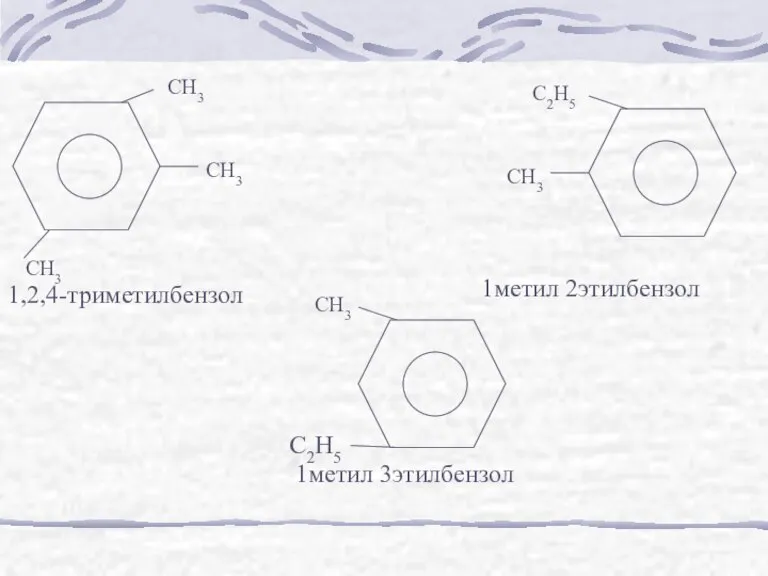
Слайд 8CH3
CH3
CH3
1,2,4-триметилбензол
CH3
C2H5
1метил 2этилбензол
CH3
1метил 3этилбензол
C2H5
Слайд 9Структурная изомерия в гомологическом ряду бензола обусловлена взаимным расположением заместителей в ядре.

Монозамещенные производные бензола не имеют изомеров положения, так как все атомы в бензольном ядре равноценны. Дизамещенные производные существуют в виде трех изомеров








 Инвестиционный проект гостиничного комплекса
Инвестиционный проект гостиничного комплекса Презентация на тему Мир нашего аквариума. Красивые рыбы. Урок изобразительного искусства (1 класс)
Презентация на тему Мир нашего аквариума. Красивые рыбы. Урок изобразительного искусства (1 класс) Education system in Ireland
Education system in Ireland Контрольно-измерительные приборы автомобиля
Контрольно-измерительные приборы автомобиля Презентация на тему территориально-структурное деление таможенных органов
Презентация на тему территориально-структурное деление таможенных органов  Социальная психология
Социальная психология Основы семиотики
Основы семиотики Продвижение гостиницы. Повышение преданности клиентов
Продвижение гостиницы. Повышение преданности клиентов Чем меня привлёк фокс Микки, или жизнь и творчество Саши Черного
Чем меня привлёк фокс Микки, или жизнь и творчество Саши Черного Архитектура Древнего Рима
Архитектура Древнего Рима Проектная задачакак средство формирования и оценки основ ключевых компетентностей младших школьников
Проектная задачакак средство формирования и оценки основ ключевых компетентностей младших школьников Учитель математикиСОШ №3 г. Баймака
Учитель математикиСОШ №3 г. Баймака Презентация на тему Императоры Российской империи
Презентация на тему Императоры Российской империи  Храмы 12-13 в
Храмы 12-13 в Царь Саломон.
Царь Саломон. Физиологическая составляющая мотивации и стимулирования
Физиологическая составляющая мотивации и стимулирования Три среды обитания организмов. Приспособленность организмов к среде обитания
Три среды обитания организмов. Приспособленность организмов к среде обитания 139 Ближе, Господь, к Тебе
139 Ближе, Господь, к Тебе Подготовка к диагностическим исследованиям: сдача мочи, кала, спермы Октябрь 2011
Подготовка к диагностическим исследованиям: сдача мочи, кала, спермы Октябрь 2011 Акробатические элементы. Упражнения на гибкость, растяжка, координация
Акробатические элементы. Упражнения на гибкость, растяжка, координация Предупреждение речевых нарушений у детей раннего возраста
Предупреждение речевых нарушений у детей раннего возраста ПРОДЛЁНКА
ПРОДЛЁНКА Королевство франков. Правление Хлодвига
Королевство франков. Правление Хлодвига Техническое регулирование деятельности предприятий и организаций нефтегазового комплекса
Техническое регулирование деятельности предприятий и организаций нефтегазового комплекса СРО 1. Устное народное творчество и музыкальное исскуство казахов. Казахские пословицы и поговорки
СРО 1. Устное народное творчество и музыкальное исскуство казахов. Казахские пословицы и поговорки Новые стандарты – первые шаги в начальной школе
Новые стандарты – первые шаги в начальной школе История
История На морском дне
На морском дне