Содержание
- 2. Окислительно-восстановительные реакции (ОВР) – реакции, сопровождающиеся изменением степени окисления элементов (атомов). Степень окисления (СО) – условный
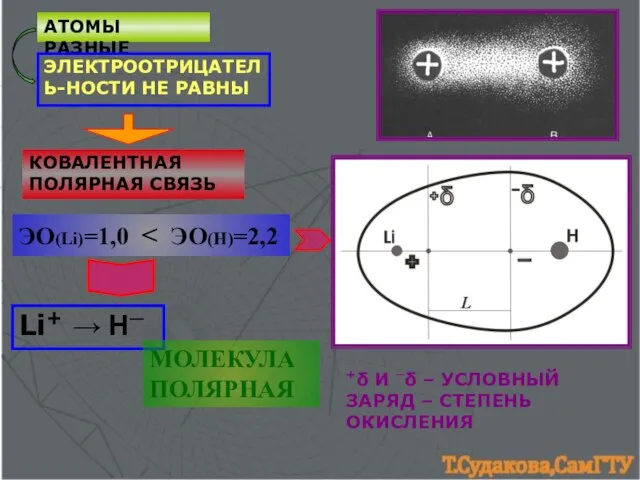
- 3. АТОМЫ РАЗНЫЕ ЭЛЕКТРООТРИЦАТЕЛЬ-НОСТИ НЕ РАВНЫ КОВАЛЕНТНАЯ ПОЛЯРНАЯ СВЯЗЬ +δ И ─δ – УСЛОВНЫЙ ЗАРЯД – СТЕПЕНЬ
- 4. Mg0 + Ag+N+5O─23 → → Mg+2O + N02 + O2 + Ag0 1) Mg0 + 2Ag+NO3
- 5. Элементы с постоянной СО: H+, Li+, Na+, K+, Rb+, Cs+, Be+2, Mg+2, Ca+2, Sr+2, Zn+2, Ag+,
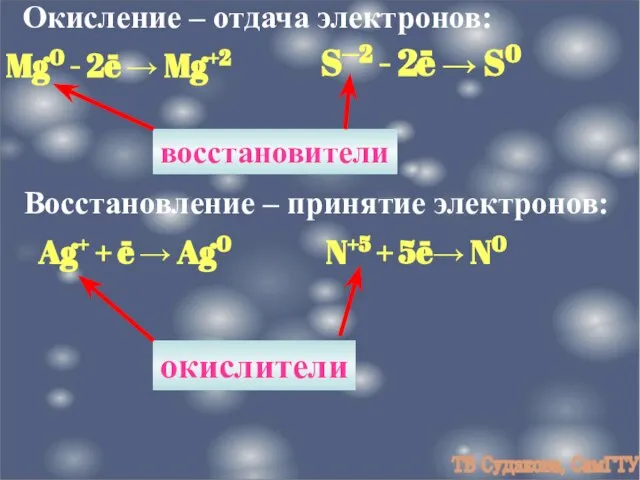
- 6. Окисление – отдача электронов: Mg0 - 2ē → Mg+2 S─2 - 2ē → S0 Восстановление –
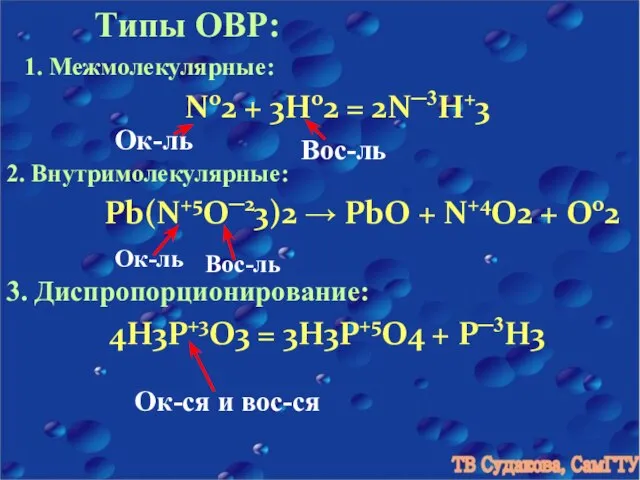
- 7. Типы ОВР: 1. Межмолекулярные: N02 + 3H02 = 2N─3H+3 Ок-ль Вос-ль 2. Внутримолекулярные: Pb(N+5O─23)2 → PbO
- 8. «Фараонова змея»: 2Hg(NCS)2 = 2HgS + C3N4 + CS2 CS─22 + 3O02 = CO─22 + 2S+4O2
- 9. Для окисления или восстановления в стандартных условиях: ΔG0 = - nFϕ0 n – кол-во ē; F
- 10. Направление самопроизвольного протекания ОВР: Полуреакция с большим значением ϕ0 – всегда ОКИСЛИТЕЛЬ! Полуреакция с меньшим значением
- 12. Скачать презентацию






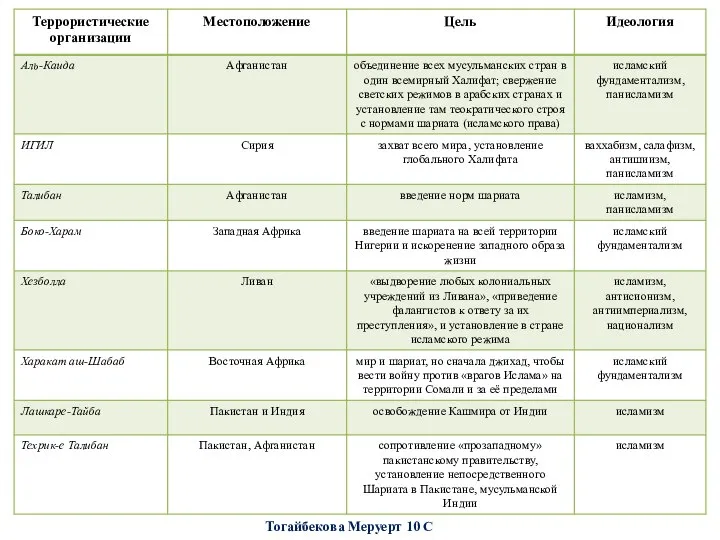 Террористические организации
Террористические организации Викторина по русским народным сказкам и сказкам А.Пушкина
Викторина по русским народным сказкам и сказкам А.Пушкина Какой я
Какой я Развитие психики и сознания
Развитие психики и сознания Рони Ритшель
Рони Ритшель Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия
Концептуальное основание современного В2В маркетинга. Концепция маркетинга взаимодействия Защита информации от несанкционированного доступа
Защита информации от несанкционированного доступа Стратегический менеджмент в условиях спонтанных изменений
Стратегический менеджмент в условиях спонтанных изменений Я - личный помощник. Измени себя и свою жизнь
Я - личный помощник. Измени себя и свою жизнь Зодчество Древней Греции.
Зодчество Древней Греции. Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики
Презентация на тему Сущность и основные понятия этики. Мораль. Типы этики  Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В
Мы познакомимся с чудной страной, Не признающий застой и покой. В этой стране можем деньги вложить И производство свое запустить В  Карликовая игрунка или пальчиковая обезьяна (Finger Monkey)
Карликовая игрунка или пальчиковая обезьяна (Finger Monkey) ТЕМА 3
ТЕМА 3 МАТЕРИНСТВО И ОТЦОВСТВО
МАТЕРИНСТВО И ОТЦОВСТВО Глагол. Урок-обобщение
Глагол. Урок-обобщение Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация
Проект 3: Развитие инновационной деятельности в Технологическом институте, г. Эрдэнэт. - презентация Люблю берёзку русскую
Люблю берёзку русскую Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО
Основные причины психологического бесплодия. Онлайн курс по подготовке к ЭКО Фотоклуб Перспектива
Фотоклуб Перспектива Die Aufgabe “d”
Die Aufgabe “d” Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул
Практика в Горьковской дирекции по ремонту пути, подработка в период летних каникул Основы грузовой и коммерческой работы
Основы грузовой и коммерческой работы Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной
Молодежный инновационный конвент способствует поддержке и повышению престижа молодого ученого в обществе Комитет по молодежной  13 признаков учителя
13 признаков учителя Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев
Тема: Повесть Н.В.Гоголя «Тарас Бульба». Отец и сыновья. Характеры главных героев Термические ожоги (5 класс)
Термические ожоги (5 класс) Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя
Культура Древнего Востока Выполнила ученица 10 класса «В» Коньшина Настя