Содержание
- 2. Важнейшие окислители Сильные F2, O2, O3, H2O2, Cl2 HClO, HClO3, H2SO4, HNO3 Царская водка NO2 KMnO4,
- 3. Сильные Щелочные и щелочно-земельные металлы Mg, Al, H2 HI и йодиды HBr и бромиды H2S и
- 4. Составление уравнений окислительно-восстановительных реакций Метод электронного баланса применяется при рассмотрении ОВР, протекающих при: сплавлении веществ, термическом
- 5. Ионно-электронный метод Достоинства метода В нем применяются не гипотетические ионы, а реально существующие ( не Mn7+,
- 6. Ионно-электронный метод Избыток ионов О2- связывается: в кислой среде – ионами Н+ О2- + 2Н+ →
- 7. Влияние некоторых факторов на характер протекания реакции Степень окисления элемента в продуктах реакции зависит от условия
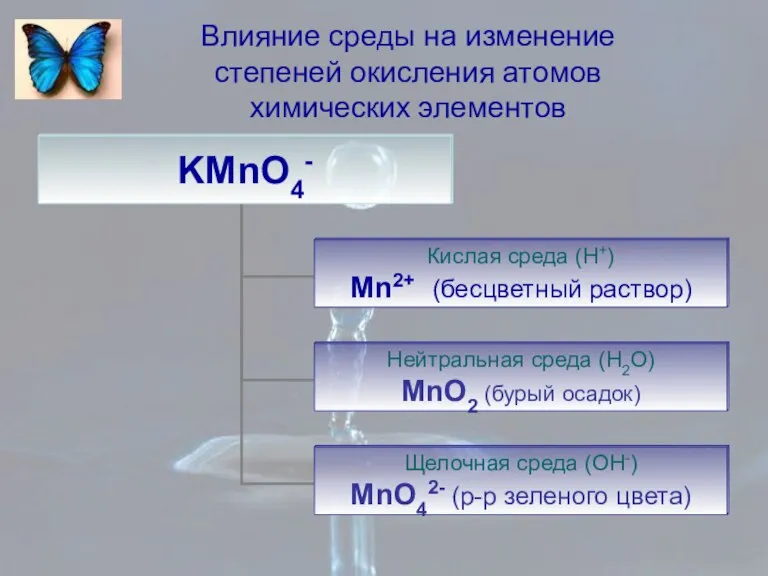
- 8. Влияние среды на изменение степеней окисления атомов химических элементов
- 9. Влияние среды на изменение степеней окисления атомов химических элементов
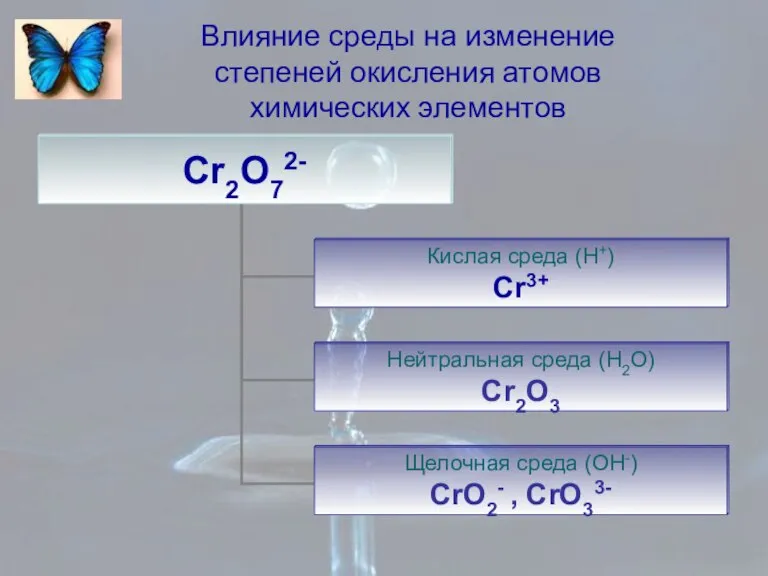
- 10. Влияние среды на изменение степеней окисления атомов химических элементов
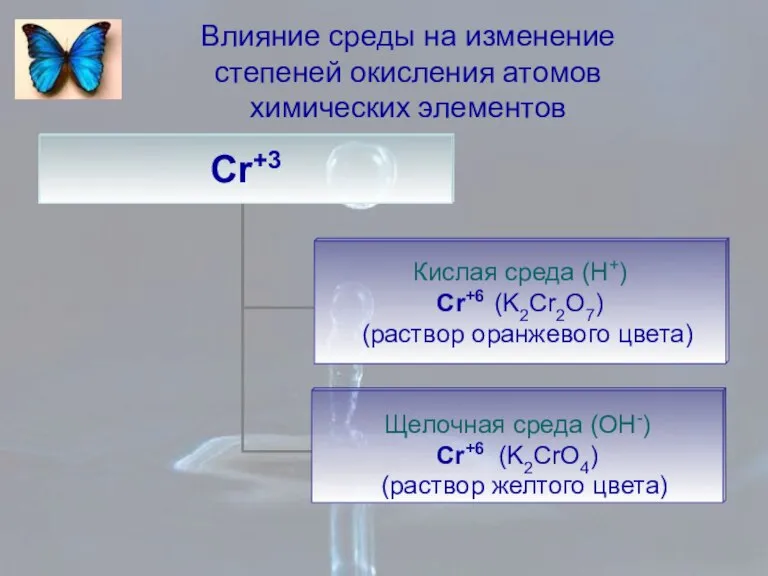
- 11. Влияние среды на изменение степеней окисления атомов химических элементов
- 13. Скачать презентацию







 Найди число в котором 2 ед. 5 разряда и 7 ед. 2 разряда.
Найди число в котором 2 ед. 5 разряда и 7 ед. 2 разряда. Животноводство
Животноводство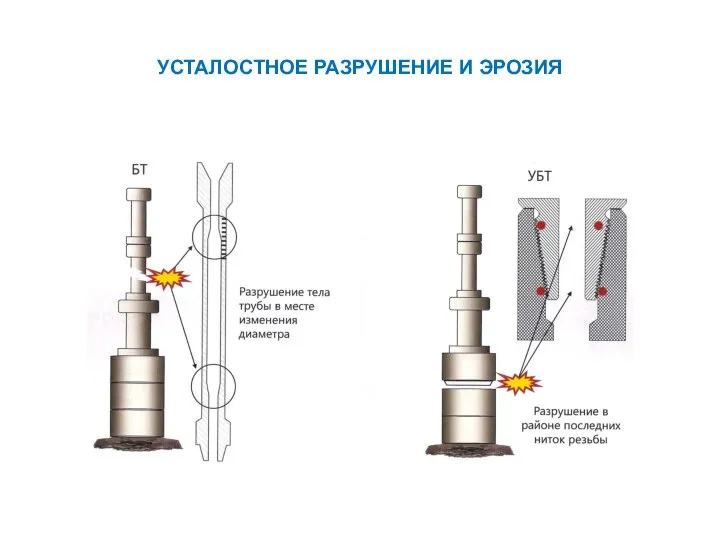 Усталостное разрушение бурильной колонны и эрозия
Усталостное разрушение бурильной колонны и эрозия Презентация на тему Traditions and holidays of Great Britain
Презентация на тему Traditions and holidays of Great Britain  Структура литературного произведения
Структура литературного произведения Кто хочет стать миллионером?
Кто хочет стать миллионером? Презентация на тему Архитектура XVII века
Презентация на тему Архитектура XVII века  ГК Кашемир и Шелк
ГК Кашемир и Шелк Ботель Ривьера. Разработка элементов фирменного стиля моделируемого предприятия
Ботель Ривьера. Разработка элементов фирменного стиля моделируемого предприятия Сила Архимеда 7 класс
Сила Архимеда 7 класс Освоение углеводородных ресурсов полуострова Ямал
Освоение углеводородных ресурсов полуострова Ямал Эстафетный бег
Эстафетный бег Тема урока: Степень с действительным показателем. Вид урока: Обобщение и систематизация. Цели: Обучающие: - обобщение и систематиза
Тема урока: Степень с действительным показателем. Вид урока: Обобщение и систематизация. Цели: Обучающие: - обобщение и систематиза Строевые упражнения
Строевые упражнения Поздравляем с наступающим Новым Годом и Рождеством!
Поздравляем с наступающим Новым Годом и Рождеством! Европа и Россия в Средние века.Развитие феодальной системы.
Европа и Россия в Средние века.Развитие феодальной системы. Конкурс День Народного Единства. Хоккейный клуб Волхов (фото)
Конкурс День Народного Единства. Хоккейный клуб Волхов (фото) Этапы работы над правилом- ступенька к грамотности
Этапы работы над правилом- ступенька к грамотности Современные виды сварки. Их преимущества и недостатки
Современные виды сварки. Их преимущества и недостатки Количественное управление процессом тестирования
Количественное управление процессом тестирования Курганская областьГОУДОД «Курганский областной центр дополнительного образования детей»
Курганская областьГОУДОД «Курганский областной центр дополнительного образования детей» Правильные и неправильные дроби
Правильные и неправильные дроби Прием заявлений в школу в электронном виде
Прием заявлений в школу в электронном виде Оборудование перегрузки топлива на АЭС
Оборудование перегрузки топлива на АЭС Презентация на тему Вводные слова. Вводные предложения. Вставные конструкции
Презентация на тему Вводные слова. Вводные предложения. Вставные конструкции  Кометы 1. Комета Галлея 2. Комета Шумахера-Леви
Кометы 1. Комета Галлея 2. Комета Шумахера-Леви Правописание глаголов
Правописание глаголов "Дистанционные олимпиады и турниры по информатике и ИКТ"
"Дистанционные олимпиады и турниры по информатике и ИКТ"