Содержание
- 2. Химические свойства Гидроксид – ионы (ОН-), образующиеся при диссоциации оснований, обуславливают их химические свойства 1. Действие
- 3. Химические свойства оснований (щелочей и нерастворимых оснований) 2NaOH + H2SO4 → Na2SO4 + 2H2O основание +
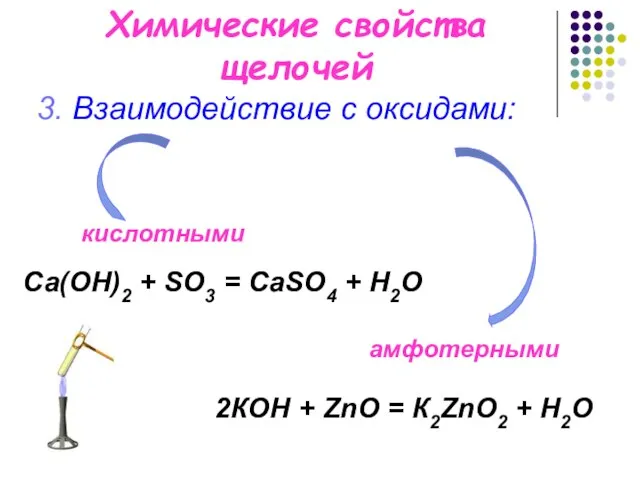
- 4. Химические свойства щелочей 3. Взаимодействие с оксидами: Са(OН)2 + SO3 = СаSO4 + H2O 2КOН +
- 5. Химические свойства щелочей 4. Взаимодействие с растворами солей: 2NaОН + CuSO4 → Cu(OH)2 + Na2SO4
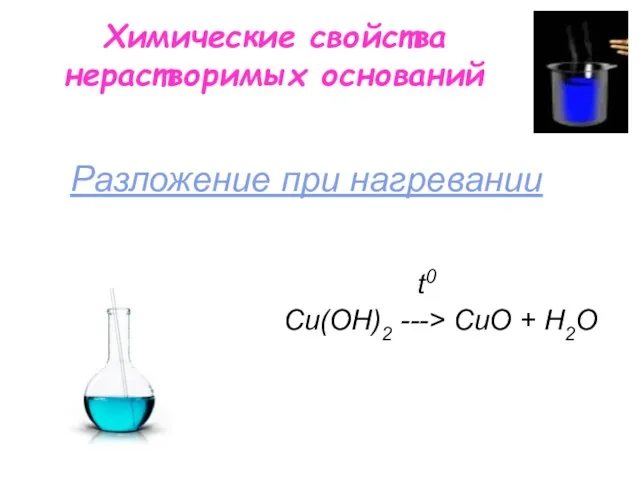
- 6. Химические свойства нерастворимых оснований t0 Сu(OН)2 ---> СuO + H2O Разложение при нагревании
- 7. Способы получения растворимых оснований (щелочей) 1. Взаимодействие щелочных и щелочно-земельных металлов с водой 2Na + 2H2O
- 9. Скачать презентацию




 Азы перспективы
Азы перспективы Задачи на 2014-2015 учебный год (4 класс) ФГОС
Задачи на 2014-2015 учебный год (4 класс) ФГОС Диагностическая линия NTS 5xx
Диагностическая линия NTS 5xx Пассажирские перевозки и их планирование
Пассажирские перевозки и их планирование Фото-отчёт. Классный час День Конституции 9-11 классы
Фото-отчёт. Классный час День Конституции 9-11 классы Русские народные куклы ( тест )
Русские народные куклы ( тест )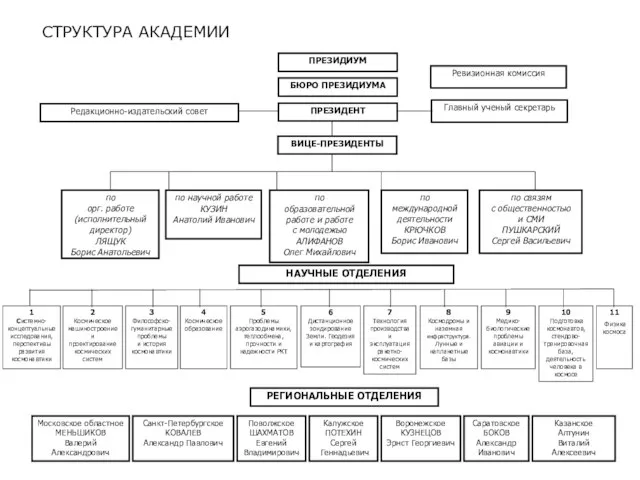 СТРУКТУРА АКАДЕМИИ
СТРУКТУРА АКАДЕМИИ Профессия моих родителей: моя мама -врач Ученица 3Б класса МАОУ «Лицей № 4» г.Перми Савельева Валерия Руководитель: Лунегова Ири
Профессия моих родителей: моя мама -врач Ученица 3Б класса МАОУ «Лицей № 4» г.Перми Савельева Валерия Руководитель: Лунегова Ири Выступление классного руководителя 10 а класса Бессмертных Елены Анатольевны по итогам адаптационного период.
Выступление классного руководителя 10 а класса Бессмертных Елены Анатольевны по итогам адаптационного период. Praktiki_gruppy_TL_44
Praktiki_gruppy_TL_44 Димакс
Димакс Золотое сечение (11 класс)
Золотое сечение (11 класс) Реформы Российской Империи
Реформы Российской Империи Презентация на тему Кайсын Кулиев
Презентация на тему Кайсын Кулиев Игра в футбол. Таблица сложения чисел с переходом через десяток. Интерактивный тренажёр.1 класс
Игра в футбол. Таблица сложения чисел с переходом через десяток. Интерактивный тренажёр.1 класс Метапредметные и личностные результаты в основной школе
Метапредметные и личностные результаты в основной школе С Е М Ь Ч У Д Е С С В Е Т А
С Е М Ь Ч У Д Е С С В Е Т А Деструктивные организации
Деструктивные организации Soonest пункт выдачи заказов
Soonest пункт выдачи заказов В мире профессий (8 класс)
В мире профессий (8 класс) Получение белка в биотехнологическом производстве
Получение белка в биотехнологическом производстве  Знакомство с Латинской Америкой
Знакомство с Латинской Америкой Welcome in the city of the Astrakhan
Welcome in the city of the Astrakhan Свои среди чужих
Свои среди чужих Своя игра русский язык
Своя игра русский язык Нахождение наибольшего и наименьшего значения функции
Нахождение наибольшего и наименьшего значения функции Куница
Куница Презентация на тему основные понятия и определения управления в таможенных органах
Презентация на тему основные понятия и определения управления в таможенных органах