Содержание
- 2. Сафиканов А.Ф. 1. История открытия галогенов 2. Положение в Периодической системе 3. Химические свойства 4. Применение
- 3. Фтор История открытия галогенов Сафиканов А.Ф. Хлор Бром Йод Астат *
- 4. В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры –23°C (в
- 5. В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал
- 6. В 1825 году французский химик А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал
- 7. В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого
- 8. В 1869 г Д.И.Мендеелеев предсказал его существование и возможность открытия в будущем (как «эка-иод»). Впервые астат
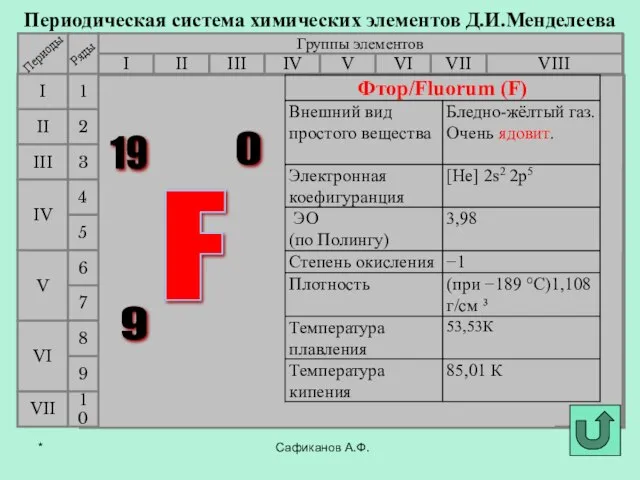
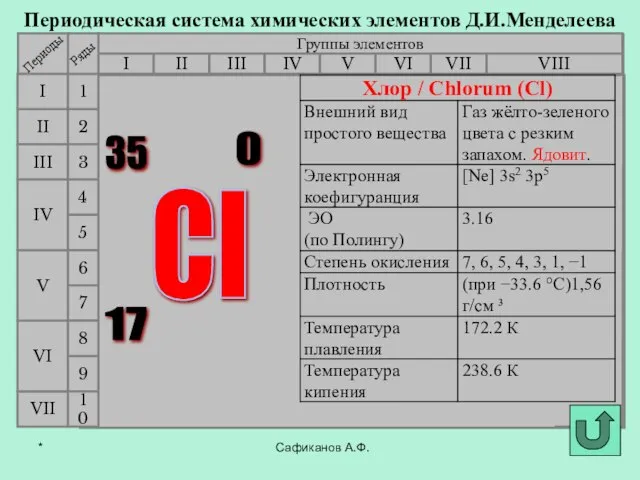
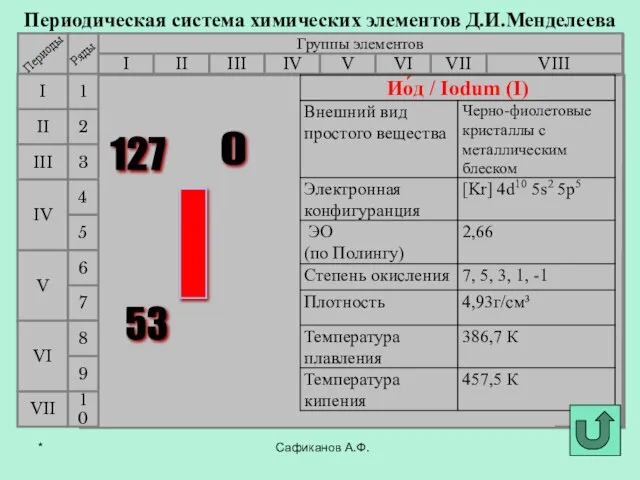
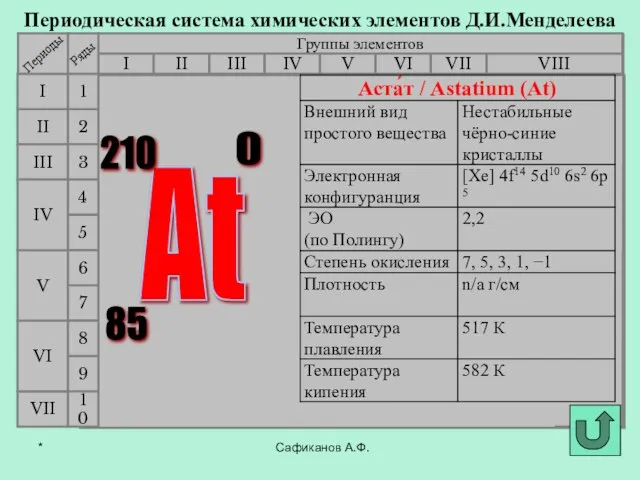
- 9. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 10. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 11. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 12. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 13. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 14. Сафиканов А.Ф. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI
- 15. Химические свойства 45 F2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с
- 16. Химические свойства 45 F2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с
- 17. Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2 и некот. др.) С простыми веществами:
- 18. Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2 и некот. др.) С простыми веществами:
- 19. Химические свойства Br2 - реакционноспособен С простыми веществами: С металлами С неметаллами Al + Br2 →
- 20. Химические свойства Br2 - реакционноспособен С простыми веществами: С металлами С неметаллами 2Al + 3Br2 →
- 21. Химические свойства I2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg +
- 22. Химические свойства I2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg +
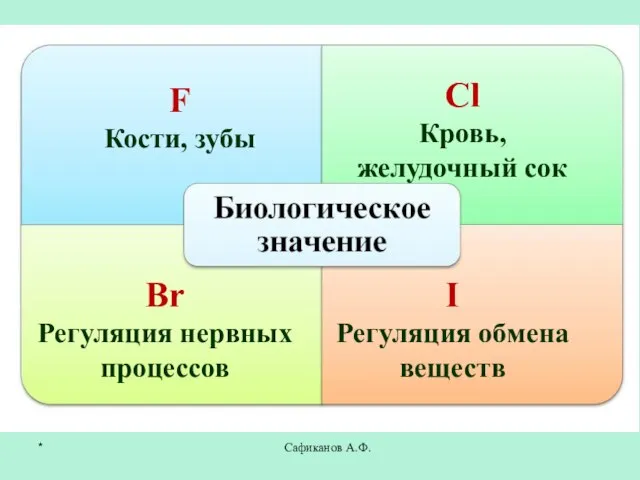
- 23. Сафиканов А.Ф. F Кости, зубы Сl Кровь, желудочный сок Br Регуляция нервных процессов I Регуляция обмена
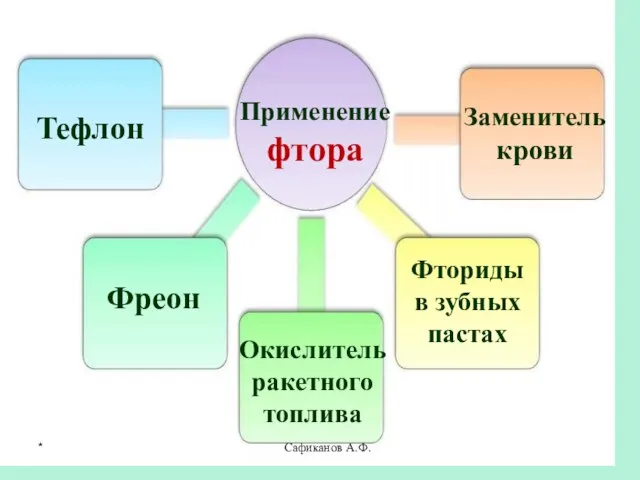
- 24. Сафиканов А.Ф. Применение фтора Тефлон Фреон Окислитель ракетного топлива Заменитель крови Фториды в зубных пастах *
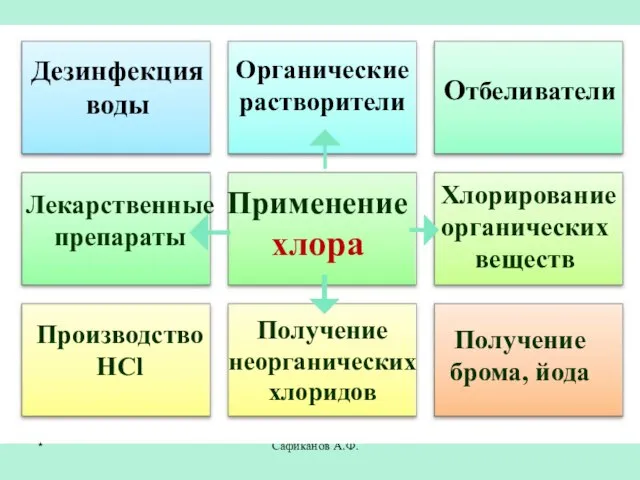
- 25. Сафиканов А.Ф. Применение хлора Отбеливатели Производство HCl Получение брома, йода Дезинфекция воды Органические растворители Лекарственные препараты
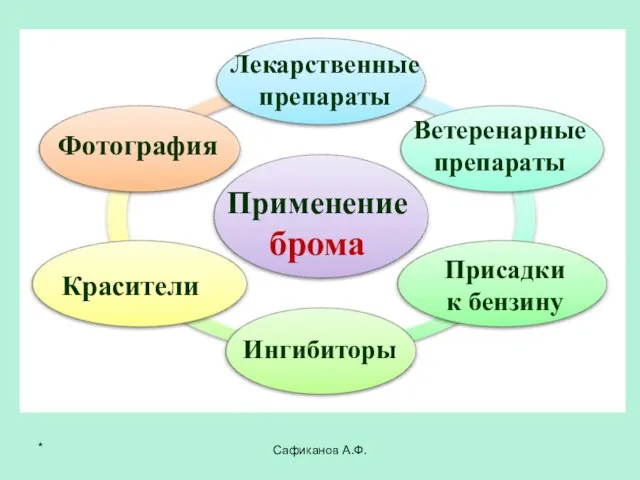
- 26. Сафиканов А.Ф. Применение брома Лекарственные препараты Красители Фотография Ветеренарные препараты Ингибиторы Присадки к бензину *
- 27. Сафиканов А.Ф. Применение йода Лекарственные препараты Фотография Красители Дезинфекция одежды Электролампы *
- 28. Физические свойства галогенов Заполни пропуски Фтор - , в воде , так как интенсивно с ней
- 29. Химические свойства галогенов Поставь коэффициенты Сафиканов А.Ф. Na + Cl2 = NaCl S + F2 =
- 30. Химические свойства галогенов Найди соответствие между исходными веществами и продуктами реакций Сафиканов А.Ф. Xe + 2F2
- 31. Сафиканов А.Ф. § 17, упр.5, 8 стр 63. Дополнительно: ссылка на сайт учителя химии Сафиканова А.Ф.
- 32. Сафиканов А.Ф. Спасибо за урок! Благодарю за сотрудничество. *
- 34. Скачать презентацию






















 Оздоровительные мероприятия с детьми в МОУ Иванковской СОШ Фурмановского района
Оздоровительные мероприятия с детьми в МОУ Иванковской СОШ Фурмановского района Религии мира и их основатели
Религии мира и их основатели The most developed Social Networks
The most developed Social Networks The Law & The Prophets/Profits
The Law & The Prophets/Profits  Шаги DIRECTUM для реализации облачной стратегии
Шаги DIRECTUM для реализации облачной стратегии Корпус с улучшенными тепловыми характеристиками (TAC)?
Корпус с улучшенными тепловыми характеристиками (TAC)? Ада Якушева
Ада Якушева Исполнение налоговой обязанности
Исполнение налоговой обязанности Обзор на персонажа
Обзор на персонажа Виды Москвы с Останкинской башни
Виды Москвы с Останкинской башни Возможности для реализации вариативного изучения истории в 10-11 классе
Возможности для реализации вариативного изучения истории в 10-11 классе Гигиена – залог здоровья
Гигиена – залог здоровья Восточные единоборства
Восточные единоборства С праздником, Горный
С праздником, Горный Выбор аромата. Характер женщины по цвету помады
Выбор аромата. Характер женщины по цвету помады Извлеченные уроки
Извлеченные уроки Технология токарных работ по дереву
Технология токарных работ по дереву Напольное отопление из материалов Rehau
Напольное отопление из материалов Rehau Презентация на тему Угарный газ
Презентация на тему Угарный газ  Движение WorldSkills в России
Движение WorldSkills в России Формула здоровья
Формула здоровья Координационный совет по охране труда при Министерстве экономики Республики Бурятия
Координационный совет по охране труда при Министерстве экономики Республики Бурятия Санкт-Петербург
Санкт-Петербург Современное выставочное искусство (5 класс)
Современное выставочное искусство (5 класс) Аренда в инновационном центре «Инженер»
Аренда в инновационном центре «Инженер» Побег. Строение и значение
Побег. Строение и значение ПОРТФОЛИО 2 КЛАССА «Б»
ПОРТФОЛИО 2 КЛАССА «Б» училище № 19
училище № 19