Содержание
- 2. Сегодня мы с вами должны вспомнить, чем отличаются жидкости от газов, и узнать, почему вода бывает
- 3. Давайте вспомним: 1.Основной закон, описывающий состояние газов называют законом _______. 2.Один моль любого газа занимает объём
- 4. Проверьте друг друга. 1.Авогадро, 2.22,4 л/моль, 3.Азот, кислород, 4.Озон, 5.Водород, 6.Известняка, 7.Синюю. За каждый правильный ответ
- 5. Попробуй реши: 1 вариант. Задача №1. Какой объём ( при н.у.) будут занимать 2 моль углекислого
- 6. Сверьте ответы… 1 Вариант Задача №1. Ответ: 44,8 л (1 Б) Задача №2. Ответ:661,8 л.(2Б) 2
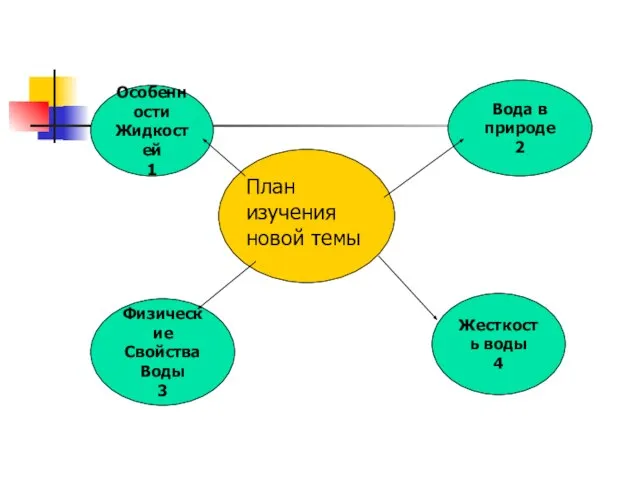
- 7. План изучения новой темы Физические Свойства Воды 3 Особенности Жидкостей 1 Жесткость воды 4 Вода в
- 8. Особенности жидкого состояния вещества. 1.Молекулы находятся непосредственно друг возле друга, поэтому жидкости – малосжимаемы, в отличие
- 9. Вода в природе. Важнейшим жидким веществом является вода, которая покрывает 2/3 поверхности Земли. 97,2 % общего
- 10. Чем уникальна вода? Физические свойства воды обусловлены строением её молекул, а также межмолекулярными связями. Молекулы воды
- 11. Вода имеет аномально высокую температуру плавления и кипения. Сравните молекулярные массы воды и других гидридов элементов
- 12. Ещё одна аномалия воды: Лёд благодаря водо- родным связям имеет ячеистое строение и поэтому легче воды.
- 13. Бывает ли вода «жесткой»? Жесткость природных вод может меняться в зависимости от года: она понижается зимой,
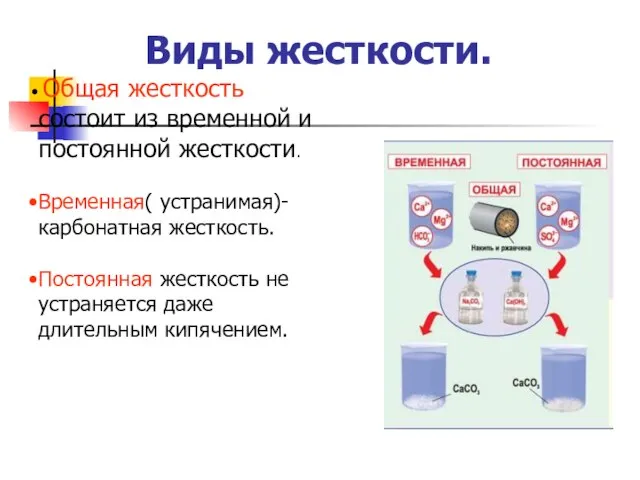
- 14. Виды жесткости. Общая жесткость состоит из временной и постоянной жесткости. Временная( устранимая)- карбонатная жесткость. Постоянная жесткость
- 15. ВИДЫ ЖЕСТКОСТИ. КАРБОНАТНАЯ жесткость зависит от содержания в воде гидрокарбонатов кальция и магния Са(НСО3)2, Mg(HCO3)2. Некарбонатная
- 16. Что такое «жесткая» вода? Жесткая вода- это накипь на деталях бытовой техники , стенках котлов и
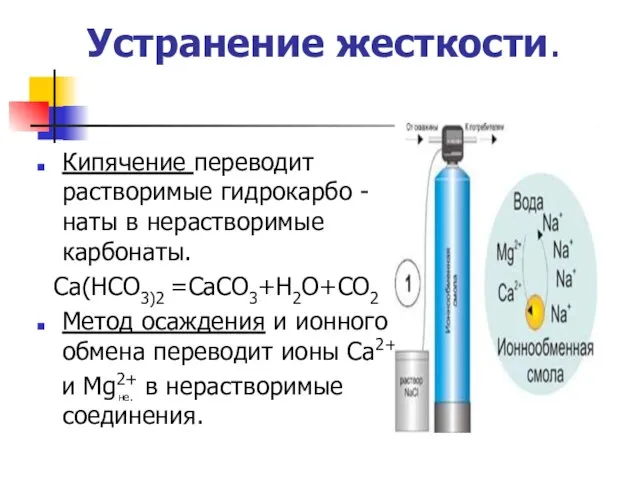
- 17. Устранение жесткости. Кипячение переводит растворимые гидрокарбо -наты в нерастворимые карбонаты. Са(НСО3)2 =СаСО3+Н2О+СО2 Метод осаждения и ионного
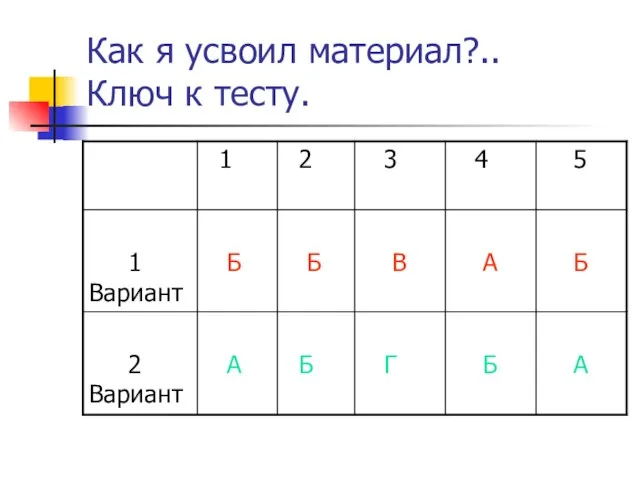
- 18. Как я усвоил материал?.. Ключ к тесту.
- 19. Подведем итоги. Подсчитайте свои баллы (каждый правильный ответ теста- 1балл) Поставьте себе оценку: 12-11 баллов- «пять»
- 20. Если Вы получили: «5»-§ 9, №11, кроссворд; «4»-§ 9, № 7,10; «3»-§ 9, № 1,3, повторить
- 22. Скачать презентацию















 Европейский день соседей
Европейский день соседей Present simple (простое настоящее время)
Present simple (простое настоящее время) Мода-2014
Мода-2014 Программирование
Программирование  Роль филологических дисциплин в формировании стратегий смыслового чтения и работы с текстом в контексте ФГОС
Роль филологических дисциплин в формировании стратегий смыслового чтения и работы с текстом в контексте ФГОС Искитимский центр профессионального обучения
Искитимский центр профессионального обучения «ОСОБЕННОСТИ СЕМЕЙНОГО ВОСПИТАНИЯ»
«ОСОБЕННОСТИ СЕМЕЙНОГО ВОСПИТАНИЯ» Карта для первокурсника. Защита проекта
Карта для первокурсника. Защита проекта Как определить окончание по вопросу?
Как определить окончание по вопросу? Приоритетные направления деятельности ФАС России. Национальные ориентиры и международные проекты
Приоритетные направления деятельности ФАС России. Национальные ориентиры и международные проекты Программа «Участник молодежного научно-инновационного конкурса» («У.М.Н.И.К.») в рамках Фонда содействия развитию малых форм предп
Программа «Участник молодежного научно-инновационного конкурса» («У.М.Н.И.К.») в рамках Фонда содействия развитию малых форм предп Презентация на тему Жизнь и творчество Николая Носова
Презентация на тему Жизнь и творчество Николая Носова Жизнь на 162%
Жизнь на 162% Современные ленточнопильные станки
Современные ленточнопильные станки I know Delphi
I know Delphi Стиль модерн
Стиль модерн Подготовка отчёта об исследовании
Подготовка отчёта об исследовании Мера ответственности родителей за воспитание ребенка
Мера ответственности родителей за воспитание ребенка Научно-методический семинар по подготовке к итоговому сочинению 2016-2017. Победа и поражение
Научно-методический семинар по подготовке к итоговому сочинению 2016-2017. Победа и поражение Презентация на тему Снежный барс 2 класс
Презентация на тему Снежный барс 2 класс Детский лагерь отдыха Ирандык
Детский лагерь отдыха Ирандык Реклама McDonald’s
Реклама McDonald’s Потребность. Блага. Услуги. Ресурсы
Потребность. Блага. Услуги. Ресурсы Красота в искусстве и в жизни
Красота в искусстве и в жизни Бадминтон
Бадминтон Концепция Mazda Accessories
Концепция Mazda Accessories Что такое кроссфит
Что такое кроссфит Карточка. Радиоактивность
Карточка. Радиоактивность