Содержание
- 2. План Відхилення реальних газів від законів для ідеальних газів. Сили міжмолекулярної взаємодії. Рівняння Ван-дер-Ваальса та його
- 3. Література: 1. Кучерук І.М., Горбачук І.Т., Луцик П.П. Загаль-ний курс фізики: Навч. посібник. – Т.1.: Механіка.
- 4. Відхилення реальних газів від законів для ідеальних газів Експериментально доведено, що закони ідеального газу виконуються при
- 5. Чи можна не враховувати розмір молекул в реальному газі ? Якщо створити тиск в 100 атм,
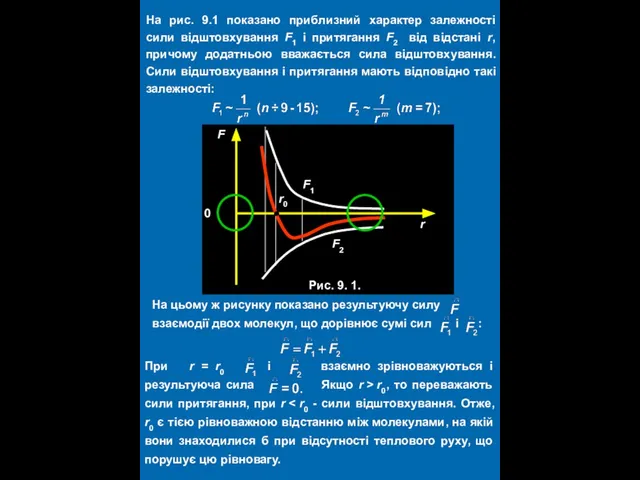
- 6. Сили міжмолекулярної взаємодії При низьких температурах або при високих тисках, коли молекули знаходяться близько одна до
- 7. На цьому ж рисунку показано результуючу силу взаємодії двох молекул, що дорівнює сумі сил і :
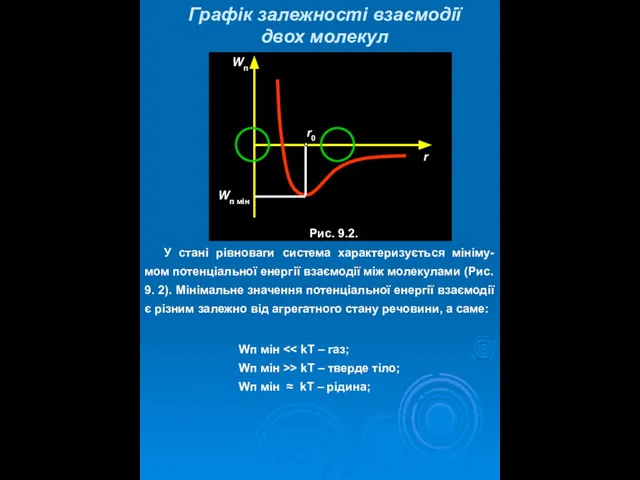
- 8. Графік залежності взаємодії двох молекул У стані рівноваги система характеризується мініму-мом потенціальної енергії взаємодії між молекулами
- 9. Рівняння Ван-дер-Ваальса та його аналіз Вперше врахував вплив молекулярних сил і, користуючись моделлю молекул, як твердих
- 10. Рівняння Ван-дер-Ваальса та його аналіз. Знайдемо значення об’єму b. Уявимо собі посудину в формі куба, об’ємом
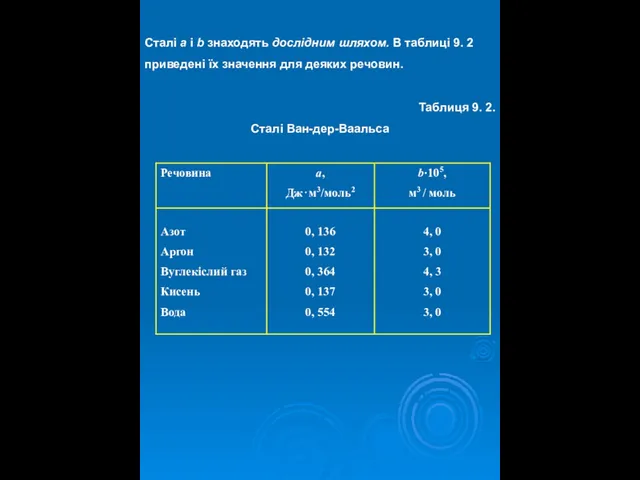
- 13. Сталі a і b знаходять дослідним шляхом. В таблиці 9. 2 приведені їх значення для деяких
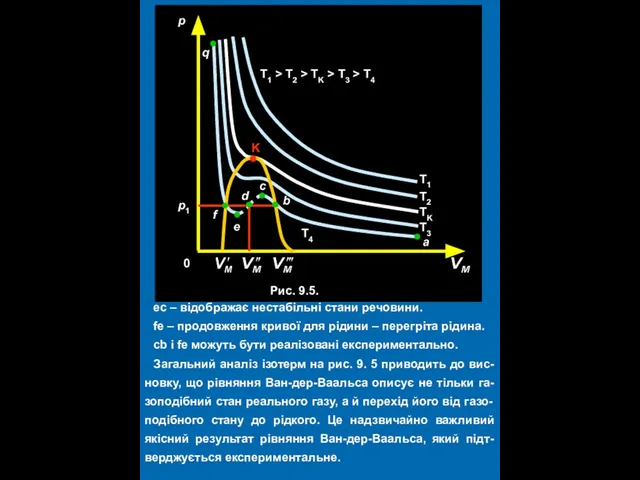
- 15. ес – відображає нестабільні стани речовини. fе – продовження кривої для рідини – перегріта рідина. сb
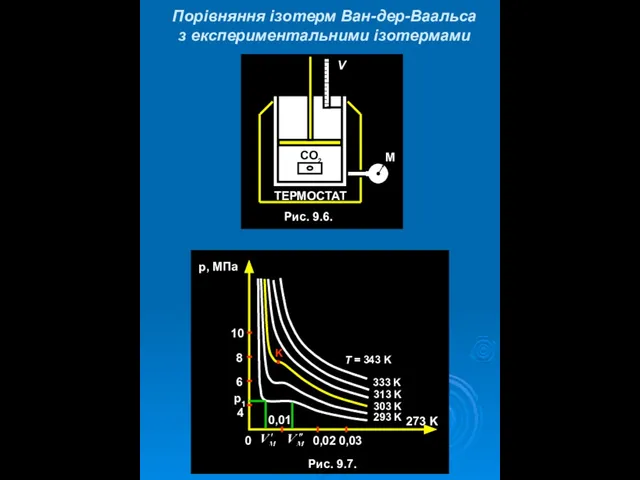
- 16. Порівняння ізотерм Ван-дер-Ваальса з експериментальними ізотермами
- 18. Скачать презентацию










 Проект Моё лицо
Проект Моё лицо Презентация на тему Компетенция должностных лиц по выявлению АП
Презентация на тему Компетенция должностных лиц по выявлению АП  Повестка родительского собрания от 26.01.2012года 1. Итоги 2 четверти 2. Задачи на 3 четверть 3. Знание и учёт возрастных особеннос
Повестка родительского собрания от 26.01.2012года 1. Итоги 2 четверти 2. Задачи на 3 четверть 3. Знание и учёт возрастных особеннос Презентация на тему Национальные костюмы народов России
Презентация на тему Национальные костюмы народов России Единицы площади. Обобщение
Единицы площади. Обобщение Программа добровольного медицинского страхования Доктор РЕСО. Екатеринбург
Программа добровольного медицинского страхования Доктор РЕСО. Екатеринбург Исследование бетонных конструкций методом ультразвукового зондирования поверхностного слоя
Исследование бетонных конструкций методом ультразвукового зондирования поверхностного слоя Великий русский писатель К.Д.Ушинский.
Великий русский писатель К.Д.Ушинский. ИНДИВИДУАЛЬНЫЕ СРЕДСТВА ЗАЩИТЫ (СИЗ)
ИНДИВИДУАЛЬНЫЕ СРЕДСТВА ЗАЩИТЫ (СИЗ) Микробиология на службе человека
Микробиология на службе человека Этюды овощей и фруктов. Живопись
Этюды овощей и фруктов. Живопись Применение солнечной энергетики в городском хозяйстве Москвы
Применение солнечной энергетики в городском хозяйстве Москвы Памятка для приезжающих в Ростовскую область из других регионов России
Памятка для приезжающих в Ростовскую область из других регионов России Текстология. Атрибуция текста, работа с рукописями
Текстология. Атрибуция текста, работа с рукописями 461 Спаситель мой живёт!
461 Спаситель мой живёт! Общая управленческая практика
Общая управленческая практика Вент& Винт. Вентиляционное оборудование
Вент& Винт. Вентиляционное оборудование Презентація_1662705410
Презентація_1662705410 1c7a5f862b5d4d6fb943f08d0af3ce8e
1c7a5f862b5d4d6fb943f08d0af3ce8e Направление Москва Юг. Дирекция Москва
Направление Москва Юг. Дирекция Москва Тематический семинар
Тематический семинар Бумажные картины Карлоса Мейра
Бумажные картины Карлоса Мейра Типы химических реакций
Типы химических реакций Презентация на тему Породы кроликов (4 класс)
Презентация на тему Породы кроликов (4 класс) Научно-практическая конференция 18 мая 2005г. Я – исследователь! Я открываю мир! МОУ Гимназия 30 им.Музалева Д.Н.
Научно-практическая конференция 18 мая 2005г. Я – исследователь! Я открываю мир! МОУ Гимназия 30 им.Музалева Д.Н. Такие разные мосты
Такие разные мосты Презентация на тему Русский язык
Презентация на тему Русский язык Концепция IOI
Концепция IOI