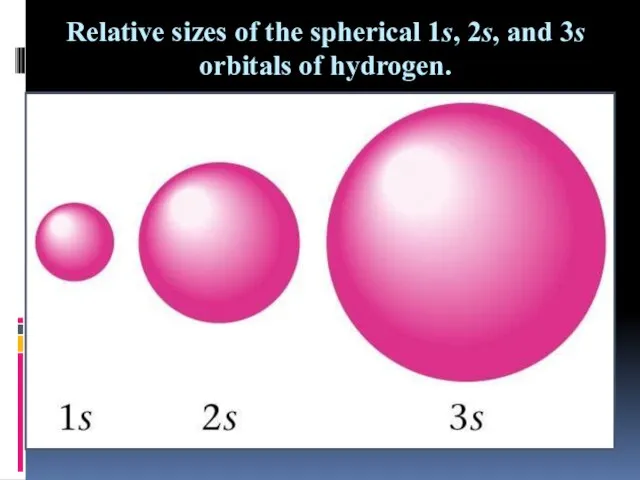
Слайд 2Relative sizes of the spherical 1s, 2s, and 3s orbitals of hydrogen.
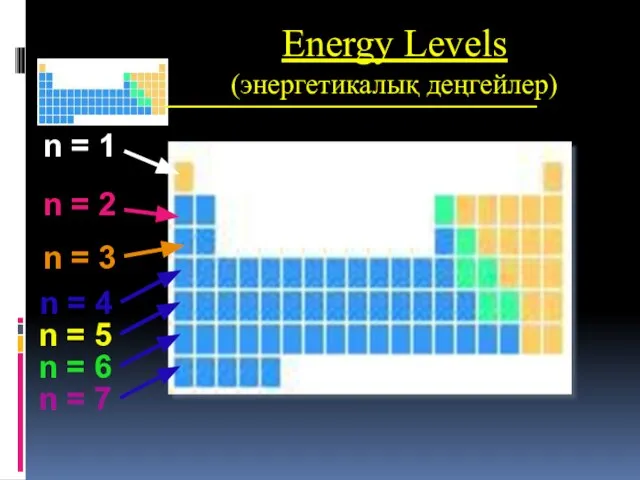
Слайд 3Energy Levels (энергетикалық деңгейлер)
Слайд 4Review
What is Electron Configuration?
(Электронды конфигурация дегеніміз не?)
1s22s22p63s23p4
Explain

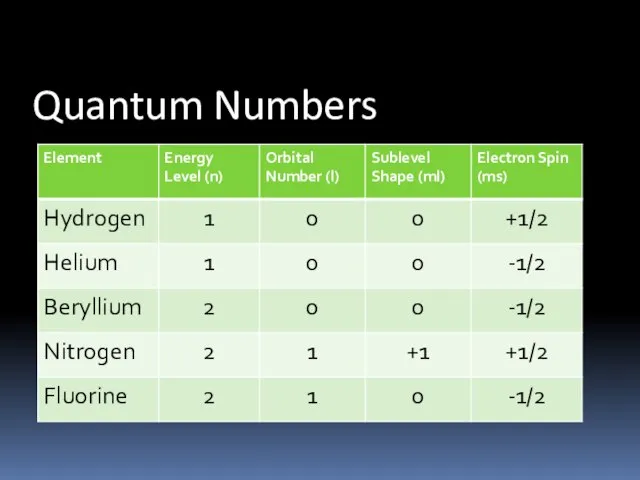
Слайд 5Quantum numbers
Энергетикалық деңгейлер(n)
Жоғары электрондық конфигурация негізінде
1 мен 7 сандары аралығында
Орбиталь

саны (l)
Указывает нахождение электрона в орбитале
Слайд 6Quantum numbers
Магнитные квантовые числа(m l)
Значения между – l и + l

рассказывает направление в каждой формы
Заместители (+1, 0, -1, +1, 0, -1)
Спин электрона квантовых чисел (m s)
Может иметь два значения
либо +1/2 or -1/2
Первая половина положительно, вторая половина отрицательна
Слайд 7© 1998 by Harcourt Brace & Company
s
p
d (n-1)
f (n-2)
1
2
3
4
5
6
7
6
7
Periodic Patterns:
“

Quantum Hotel”
Слайд 9 General Rules (Общие правила)
Паули Принцип
Каждый орбитальный может содержать два электрона

с противоположными спинами.
Слайд 10General Rules
Принцип Ауфтбауа
или правило Клечковского
Электроны заполняют
орбитали первыми
с наименьшей энергией
“Правило

Ленивый Орендатор”
Слайд 11RIGHT
WRONG
General Rules
Hund’s Rule (Правило Хунда)
Электрондық орбитальдарды толтыру барысында бір электроннан қою.
“Empty Seat
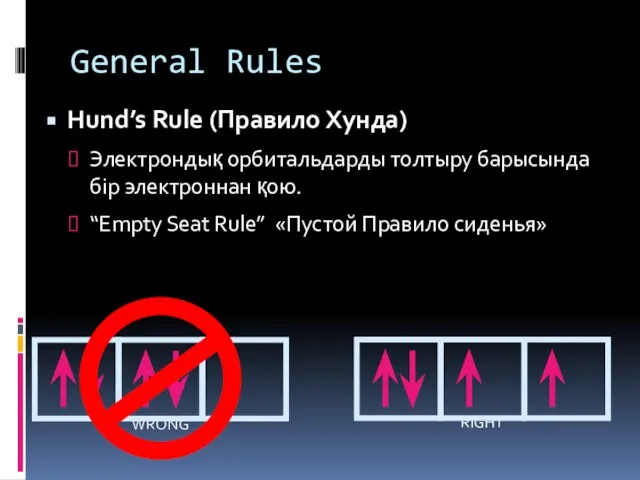
Rule” «Пустой Правило сиденья»









 ГЕОЛОГИЧЕСКАЯ РАБОТА ПОВЕРХНОСТНЫХ ТЕКУЧИХ ВОД
ГЕОЛОГИЧЕСКАЯ РАБОТА ПОВЕРХНОСТНЫХ ТЕКУЧИХ ВОД Центр довузовского образования ГУМРФ имени адмирала С.О. Макарова
Центр довузовского образования ГУМРФ имени адмирала С.О. Макарова Алгоритм оценивания письменных высказываний с элементами рассуждения
Алгоритм оценивания письменных высказываний с элементами рассуждения Влияние учетной политики на финансовый результат деятельности предприятия
Влияние учетной политики на финансовый результат деятельности предприятия Почка растений
Почка растений e2b2bf7752e93ea5095a63c392fa0930 (1)
e2b2bf7752e93ea5095a63c392fa0930 (1) Финкульт привет - онлайн-форум
Финкульт привет - онлайн-форум Человек и политика. Возможности участия граждан в политике
Человек и политика. Возможности участия граждан в политике Learning more about each other
Learning more about each other Семья и семейные традиции
Семья и семейные традиции Межкультурная толерантность и ее проявление в журналисткой практике
Межкультурная толерантность и ее проявление в журналисткой практике Информационные технологии в дизайне
Информационные технологии в дизайне 室外加热器
室外加热器 Рисуем пингвина
Рисуем пингвина История шелководства
История шелководства Презентация на тему Эмоции и здоровье
Презентация на тему Эмоции и здоровье  Мошенничество, то есть хищение чужого имущества или приобретение права на чужое имущество
Мошенничество, то есть хищение чужого имущества или приобретение права на чужое имущество Смерчи и торнадо
Смерчи и торнадо Обзор зарубежной литературы 1 половины 20 века
Обзор зарубежной литературы 1 половины 20 века Магазин Цветы для всех. Конфетные букеты
Магазин Цветы для всех. Конфетные букеты Мастер класс Русская матрешка
Мастер класс Русская матрешка Презентация на тему Путешествие в город обыкновенных дробей на проспект
Презентация на тему Путешествие в город обыкновенных дробей на проспект Ювелирное ремесло XVII-XVIII века в России
Ювелирное ремесло XVII-XVIII века в России Чистота залог здоровья
Чистота залог здоровья СМИ о хип-хоп культуре. Мы не угроза обществу - FREAK FRIENDS
СМИ о хип-хоп культуре. Мы не угроза обществу - FREAK FRIENDS 5. Обеспечение помехоустойчивости при конструктивной реализации схем
5. Обеспечение помехоустойчивости при конструктивной реализации схем Lata dzieciństwa
Lata dzieciństwa Молодежь как социальная группа
Молодежь как социальная группа