Содержание
- 2. Цель работы: Установление закономерностей механизма и кинетики ионного переноса в твердофазных электрохимических системах металл | твердый
- 3. Химические формулы и названия органических полупроводников (298 К) 3
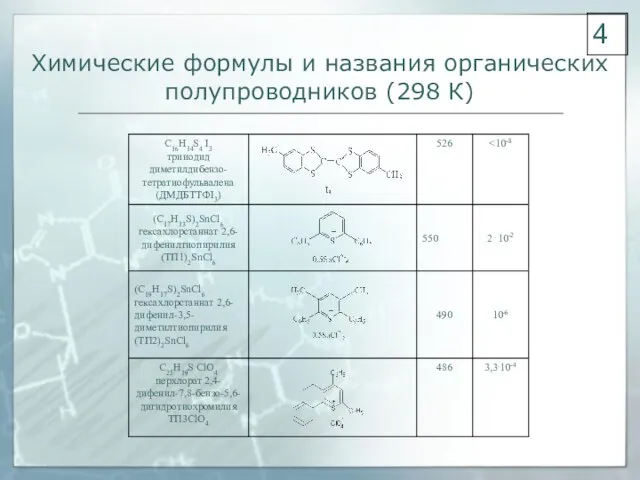
- 4. Химические формулы и названия органических полупроводников (298 К) 4
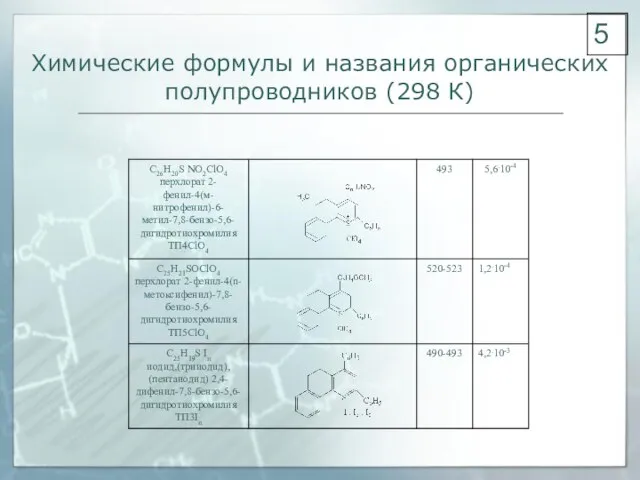
- 5. Химические формулы и названия органических полупроводников (298 К) 5
- 6. Химические формулы и названия органических полупроводников (298 К) 6 ТКЦ - 3,3-диэтилтиокарбоцианин; ТЦХМ - 7,7`,8,8`-тетрацианохиноиметан; ТФ
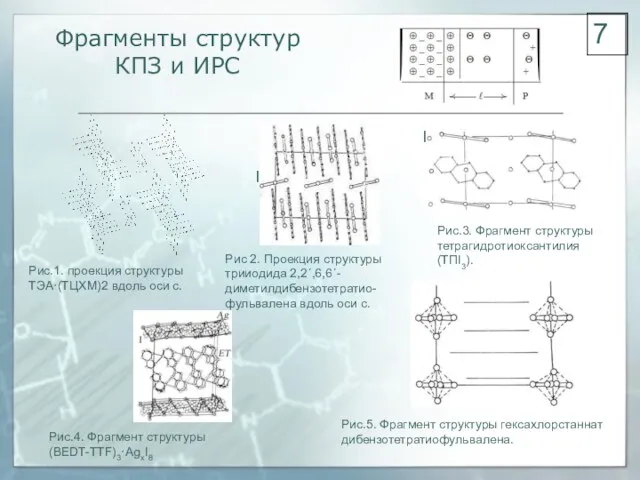
- 7. Фрагменты структур КПЗ и ИРС Рис.1. проекция структуры ТЭА·(ТЦХМ)2 вдоль оси с. Рис.3. Фрагмент структуры тетрагидротиоксантилия
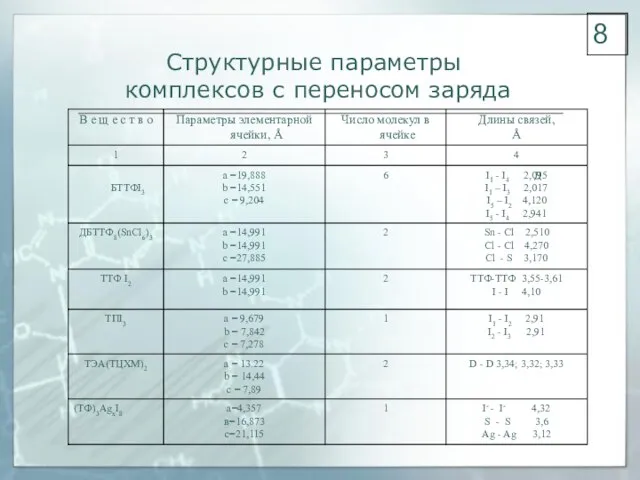
- 8. Структурные параметры комплексов с переносом заряда 8
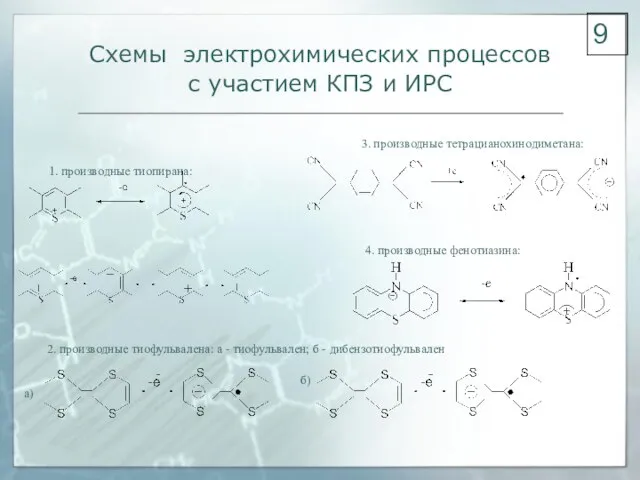
- 9. Схемы электрохимических процессов с участием КПЗ и ИРС 1. производные тиопирана: 2. производные тиофульвалена: а -
- 10. Уравнения температурной зависимости э.д.с. систем Na|Na+-β-Al2O3 | йодный КПЗ 10 1 2
- 11. Энергия Гиббса и направленность химических реакций в системе: Na|β-Аl2O3|I2;С Состав β-глинозема: Na2O·5Al2O3·0,1TiO2·0,8CoO. Энергия Гиббса образования NaI,
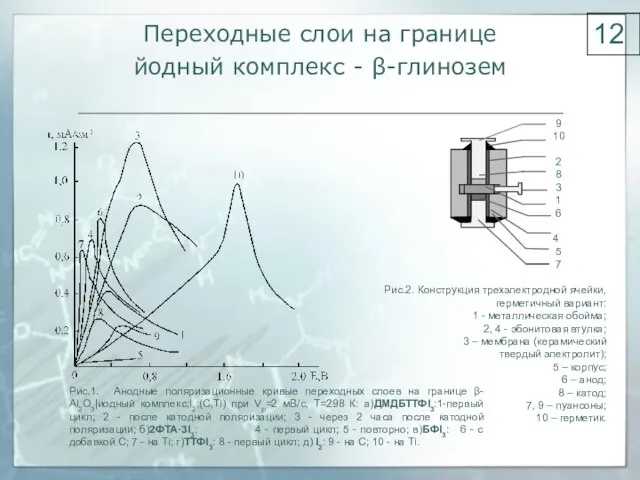
- 12. Переходные слои на границе йодный комплекс - β-глинозем Рис.1. Анодные поляризационные кривые переходных слоев на границе
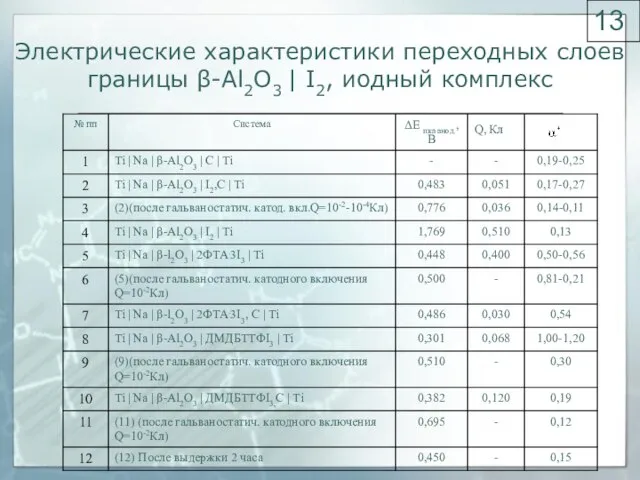
- 13. Электрические характеристики переходных слоев границы β-Al2O3 | I2, иодный комплекс Q, Кл 13
- 14. Поляризационные кривые границы: а: ФТАI3 / β-Al2O3; б, в: ДМДБТТФIх / β-Al2O3 а б в а
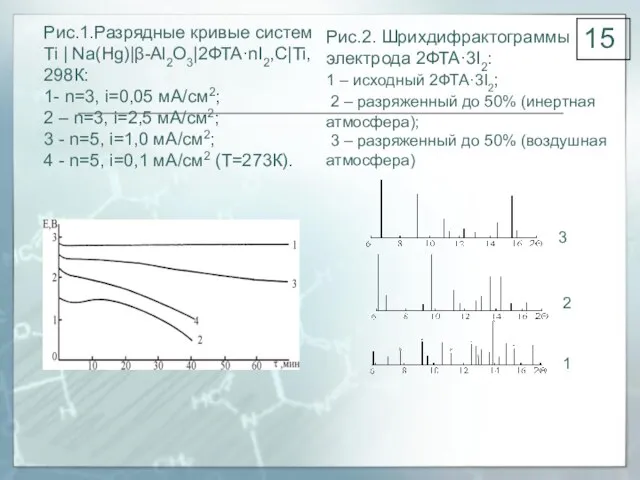
- 15. Рис.2. Шрихдифрактограммы электрода 2ФТА·3I2: 1 – исходный 2ФТА·3I2; 2 – разряженный до 50% (инертная атмосфера); 3
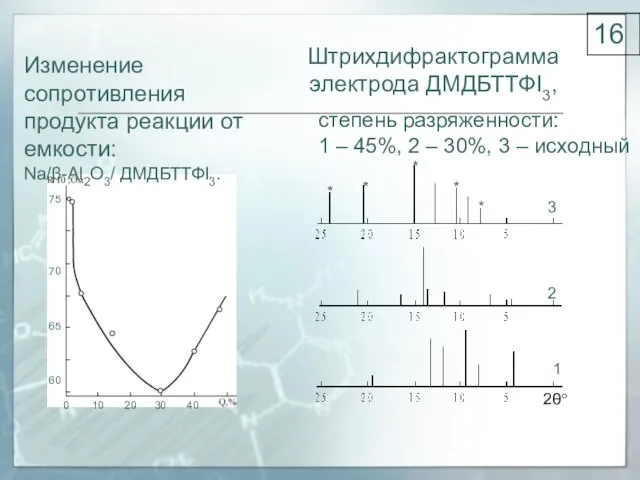
- 16. Изменение сопротивления продукта реакции от емкости: Na/β-Al2O3/ ДМДБТТФI3. 75 70 65 60 0 10 20 30
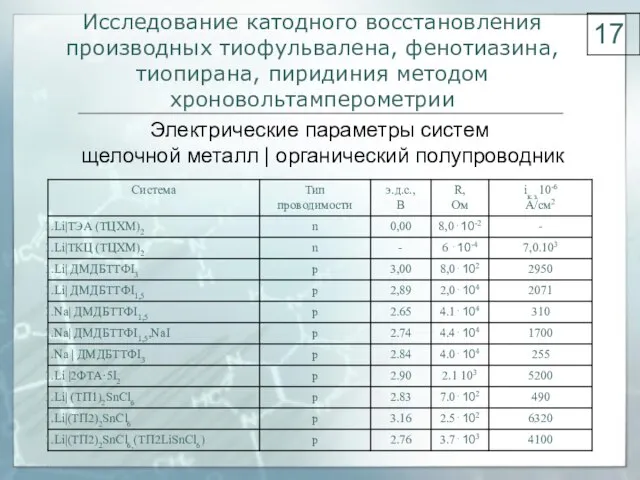
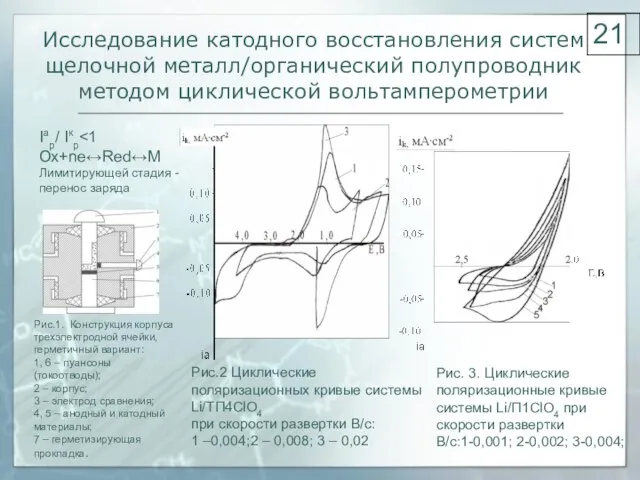
- 17. Исследование катодного восстановления производных тиофульвалена, фенотиазина, тиопирана, пиридиния методом хроновольтамперометрии Электрические параметры систем щелочной металл |
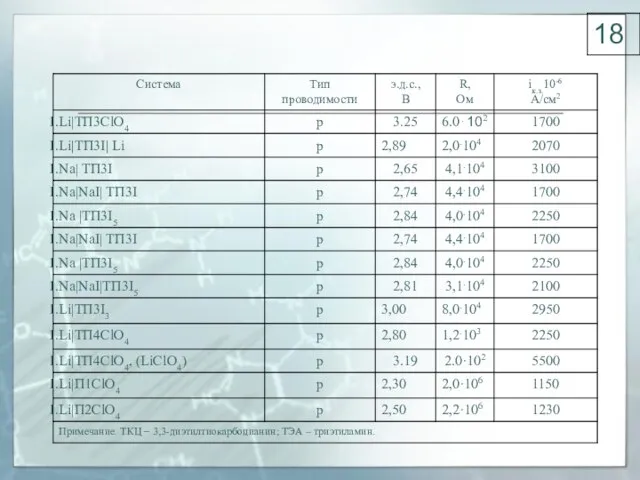
- 18. 18
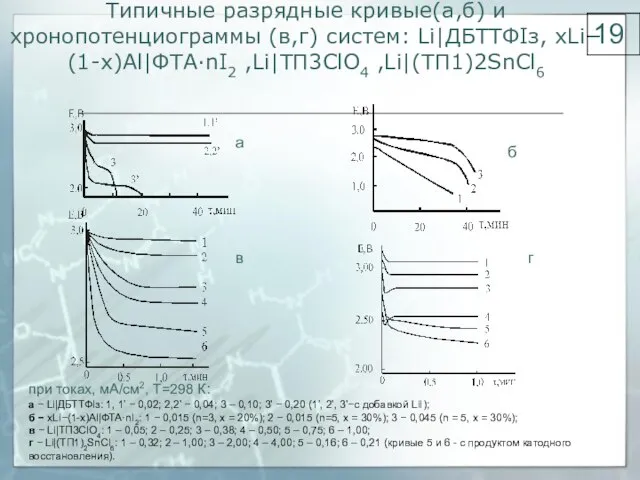
- 19. Типичные разрядные кривые(а,б) и хронопотенциограммы (в,г) систем: Li|ДБТТФIз, xLi−(1-х)Аl|ФТА·nI2 ,Li|ТП3ClO4 ,Li|(ТП1)2SnCl6 при токах, мА/см2, Т=298 К:
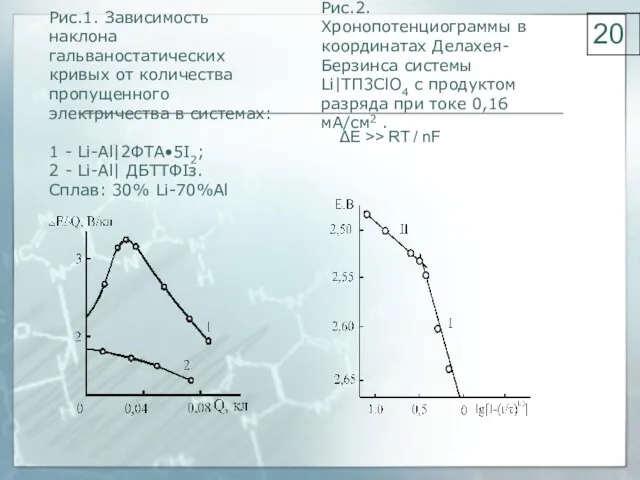
- 20. Рис.1. Зависимость наклона гальваностатических кривых от количества пропущенного электричества в системах: 1 - Li-Al|2ФTA•5I2; 2 -
- 21. Исследование катодного восстановления систем щелочной металл/органический полупроводник методом циклической вольтамперометрии Рис.2 Циклические поляризационных кривые системы Li/ТП4СlO4
- 22. Рис. 1. Зависимость константы скорости электрохимической реакции от потенциала системы Li|БФIз . Рис.2. Приложимость уравнения Ерофеева-Колмогорова-Аврами
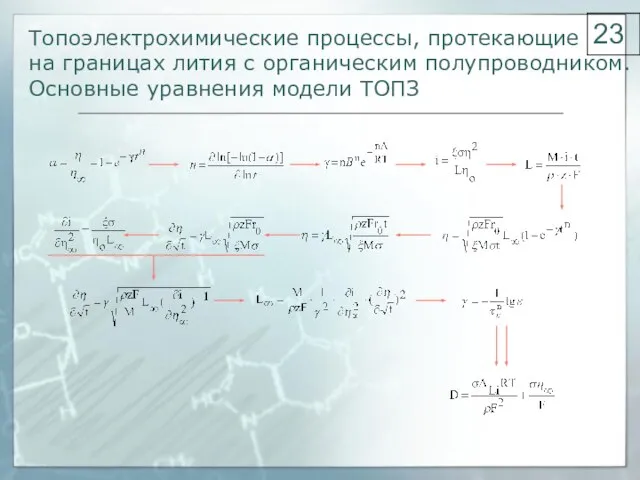
- 23. Топоэлектрохимические процессы, протекающие на границах лития с органическим полупроводником. Основные уравнения модели ТОПЗ 23
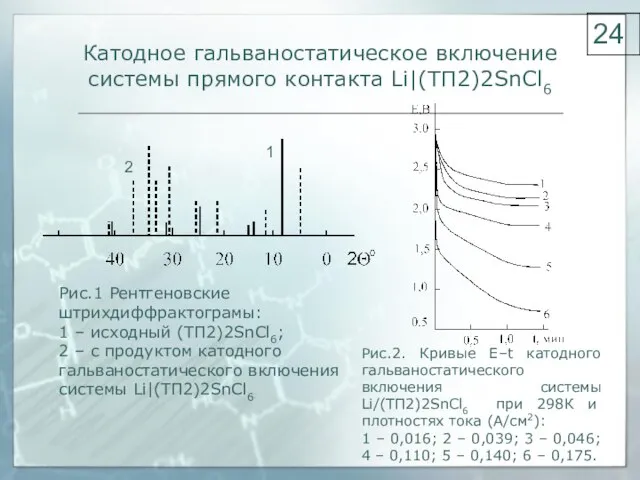
- 24. Катодное гальваностатическое включение системы прямого контакта Li|(ТП2)2SnCl6 Рис.1 Рентгеновские штрихдиффрактограмы: 1 – исходный (ТП2)2SnCl6; 2 –
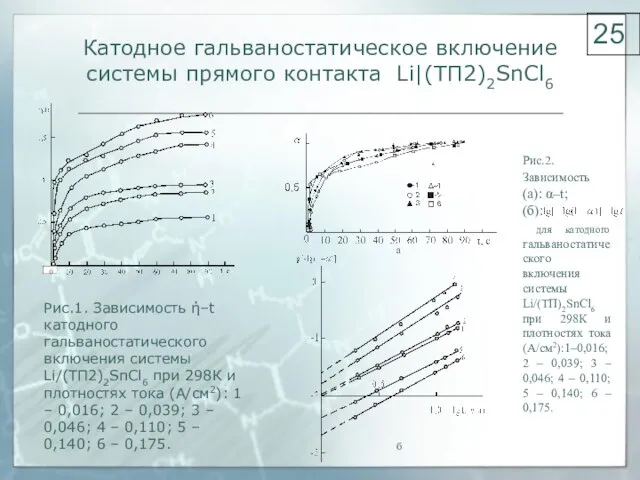
- 25. Катодное гальваностатическое включение системы прямого контакта Li|(ТП2)2SnCl6 Рис.1. Зависимость ή–t катодного гальваностатического включения системы Li/(ТП2)2SnCl6 при
- 26. Катодное гальваностатическое включение системы прямого контакта Li|(ТП2)2SnCl6 Рис.1. Зависимость стационарной толщины слоя переходной интерфазы от плотности
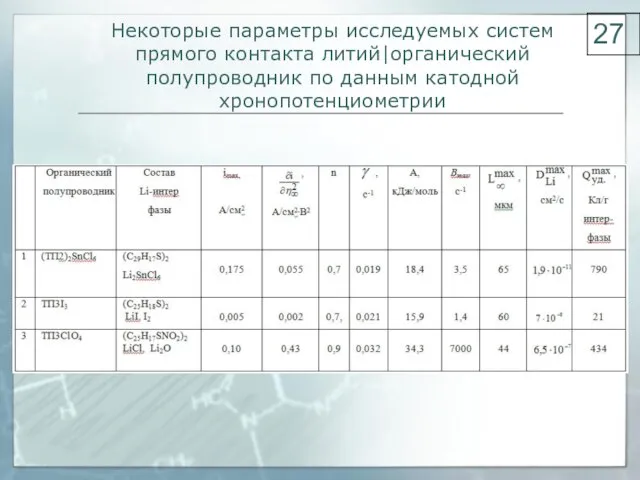
- 27. Некоторые параметры исследуемых систем прямого контакта литий|органический полупроводник по данным катодной хронопотенциометрии 27
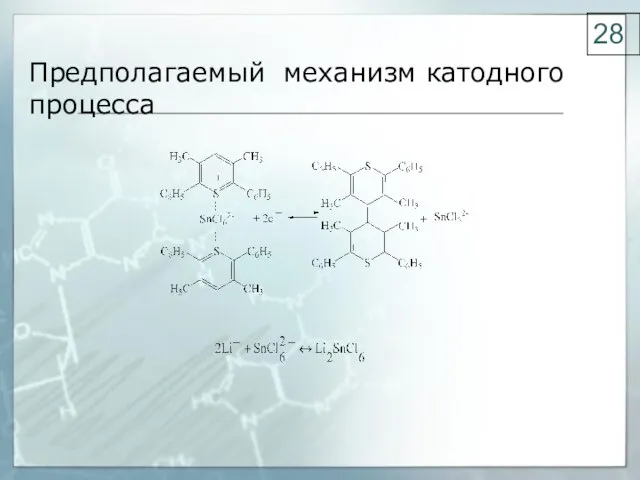
- 28. Предполагаемый механизм катодного процесса 28
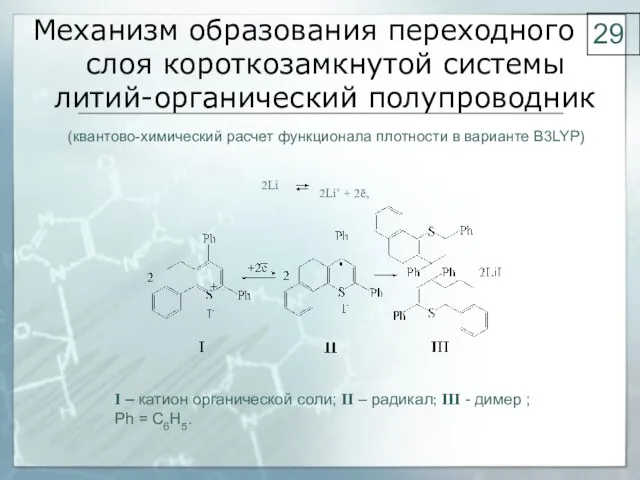
- 29. Механизм образования переходного слоя короткозамкнутой системы литий-органический полупроводник 2Li 2Li+ + 2ē, (квантово-химический расчет функционала плотности
- 30. Температурная зависимость электропроводности (σ0) синтезированных продуктов 30
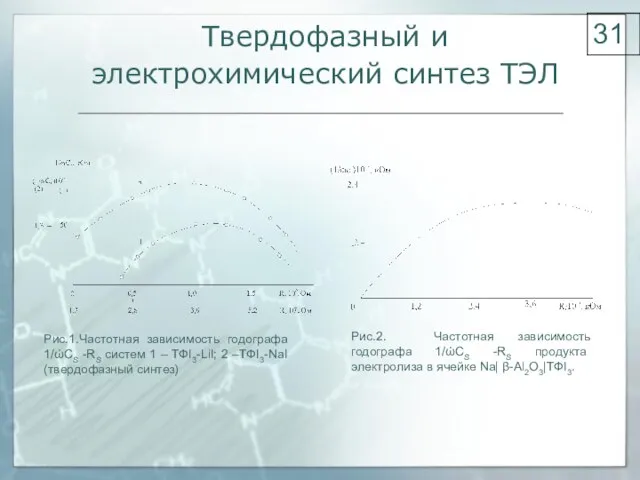
- 31. Твердофазный и электрохимический синтез ТЭЛ Рис.2. Частотная зависимость годографа 1/ώCS -RS продукта электролиза в ячейке Na|
- 32. Параметры общей (σобщ.) и электронной (σе) проводимостей продуктов электрохимических реакций короткозамкнутых систем (298 К) 32
- 33. Рис.1. Изменение сопротивления во времени при твердофазном синтезе (Т=298 К) в системах: 1 – LiI -ТПI;
- 34. Схемы механизмов реакций [R Me+] + MeA (I) R+A- + Me [R Me+]A- ; R -
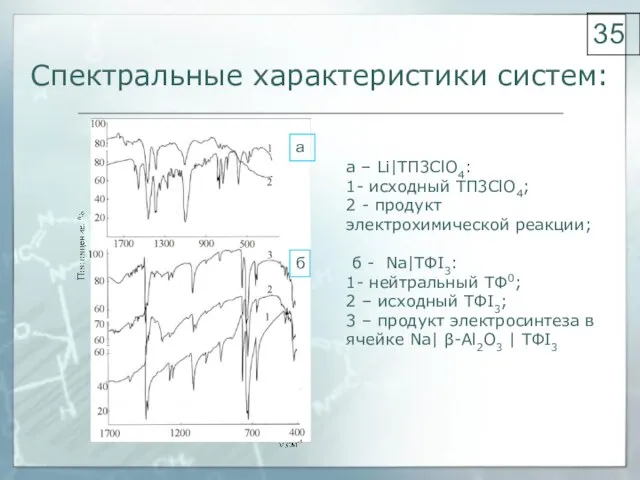
- 35. Спектральные характеристики систем: а – Li|ТП3ClO4: 1- исходный ТП3ClО4; 2 - продукт электрохимической реакции; б -
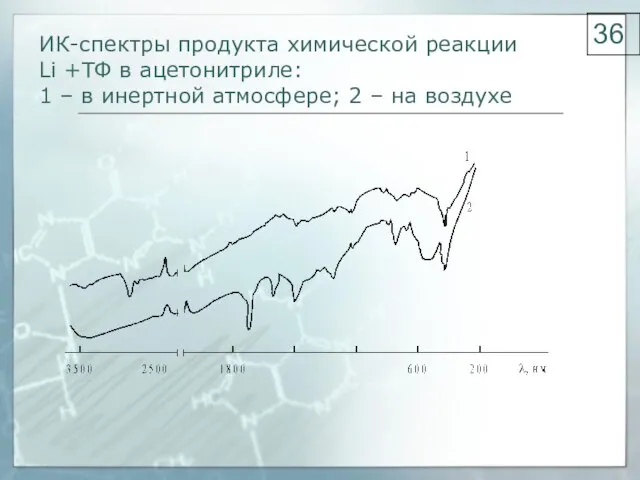
- 36. ИК-спектры продукта химической реакции Li +ТФ в ацетонитриле: 1 – в инертной атмосфере; 2 – на
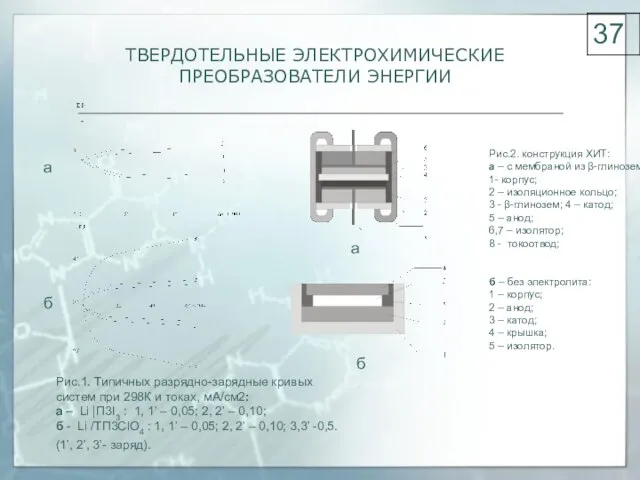
- 37. ТВЕРДОТЕЛЬНЫЕ ЭЛЕКТРОХИМИЧЕСКИЕ ПРЕОБРАЗОВАТЕЛИ ЭНЕРГИИ Рис.2. конструкция ХИТ: а – с мембраной из β-глинозема: 1- корпус; 2
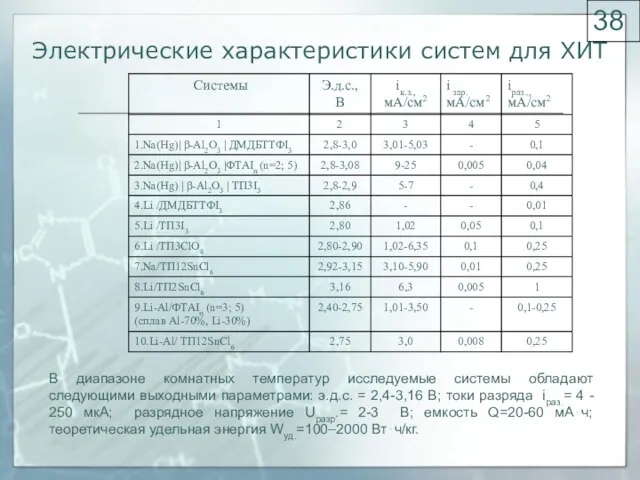
- 38. Электрические характеристики систем для ХИТ В диапазоне комнатных температур исследуемые системы обладают следующими выходными параметрами: э.д.с.
- 40. Скачать презентацию











![Схемы механизмов реакций [R Me+] + MeA (I) R+A- + Me [R](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/385297/slide-33.jpg)
 Титульный лист
Титульный лист Учителями славится Россия ,ученики приносят славу ей…
Учителями славится Россия ,ученики приносят славу ей… Авторское право и дизайн
Авторское право и дизайн ПРОЕКТ«ШКОЛЬНЫЙ ДВОР»МОУ СОШ № 18 г.Костромы
ПРОЕКТ«ШКОЛЬНЫЙ ДВОР»МОУ СОШ № 18 г.Костромы Экономическое развитие. Экономическая деятельность и условия её эффективности.
Экономическое развитие. Экономическая деятельность и условия её эффективности. Космические модули. Конфуций
Космические модули. Конфуций Бухгалтерский учёт и налоговый контроль
Бухгалтерский учёт и налоговый контроль Маркетинговые исследования. Тема 3
Маркетинговые исследования. Тема 3 2 людей тратят больше времени на общение в интернете, чем в реальной жизни 57 % крупных компаний США планируют использовать в продвиж
2 людей тратят больше времени на общение в интернете, чем в реальной жизни 57 % крупных компаний США планируют использовать в продвиж ПРОЕКТ«ИСТОРИЯ В ЮГУ»
ПРОЕКТ«ИСТОРИЯ В ЮГУ» Набор в секции. Отделение сложно-координационных видов
Набор в секции. Отделение сложно-координационных видов Предлагаем Вам рассмотреть коммерческое предложение на поставку самосвалов SHACMAN SX3255DR384 6x4 336 л.с. (технология МAN)
Предлагаем Вам рассмотреть коммерческое предложение на поставку самосвалов SHACMAN SX3255DR384 6x4 336 л.с. (технология МAN) Эпиграфы урока Человек – это звучит гордо ! Существует только человек, всё остальное – дело его рук, его мозга. М. Горький « На дне »
Эпиграфы урока Человек – это звучит гордо ! Существует только человек, всё остальное – дело его рук, его мозга. М. Горький « На дне »  Тема:220 г. до н.э. Чжан Чжунцзин публикует «Шань Хань Лунь»-самый древний полный учебник по медицине, уделяющий внимание диагностик
Тема:220 г. до н.э. Чжан Чжунцзин публикует «Шань Хань Лунь»-самый древний полный учебник по медицине, уделяющий внимание диагностик Основы психологии и педагогики
Основы психологии и педагогики Государственное управление комплексом черной металлургии
Государственное управление комплексом черной металлургии Мир увлечений
Мир увлечений Преступление и уголовная ответственность
Преступление и уголовная ответственность Школьная площадка МБОУ Марининской СОШ № 16
Школьная площадка МБОУ Марининской СОШ № 16 Информационные образовательные ресурсы нового поколения
Информационные образовательные ресурсы нового поколения Основы подготовки к военной службе. Практикумы
Основы подготовки к военной службе. Практикумы Однолетние цветковые растения
Однолетние цветковые растения Незаконный оборот наркотических веществ
Незаконный оборот наркотических веществ Отчет о финансовых результатах (форма №2)
Отчет о финансовых результатах (форма №2) Роль физической культуры в укреплении здоровья
Роль физической культуры в укреплении здоровья Mit App Inventor
Mit App Inventor ОДО ФЛиС
ОДО ФЛиС Население России. История переписи населения
Население России. История переписи населения