Содержание
- 2. Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании. Металлы обладают электропроводностью и теплопроводностью.
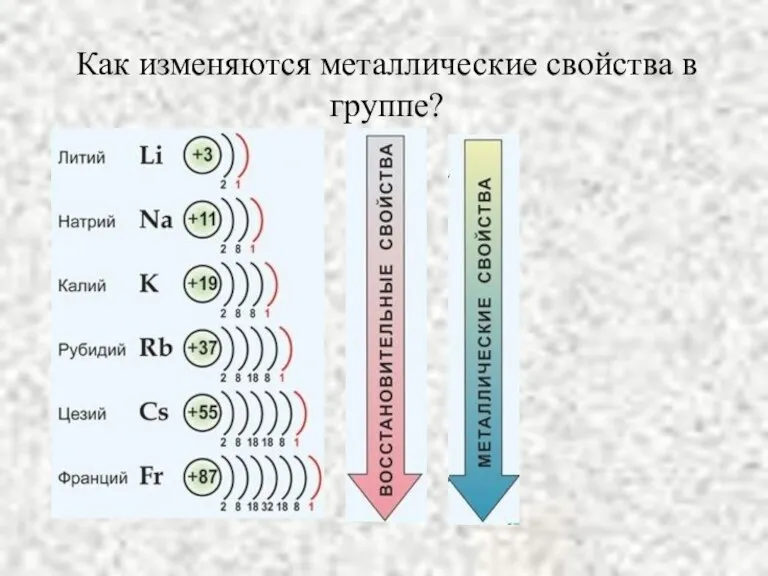
- 3. Как изменяются металлические свойства в группе?
- 4. Радиусы атомов элементов 1А группы
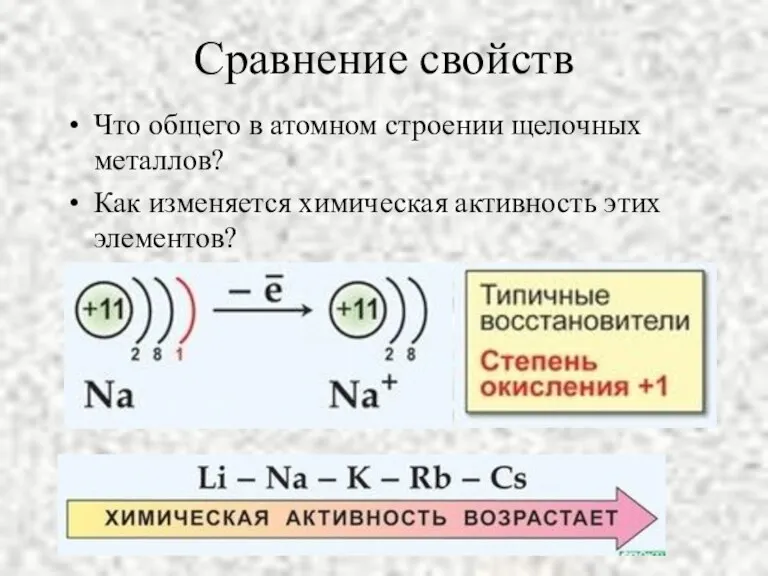
- 5. Сравнение свойств Что общего в атомном строении щелочных металлов? Как изменяется химическая активность этих элементов?
- 6. ИСТОРИЯ ОТКРЫТИЯ Натрий и калий – 1807г. Английский химик и физик Г.Дэви получил их в виде
- 7. Происхождение названий Li (1817) лат. " литос" - камень Na (1807) араб. "натрум" - сода К
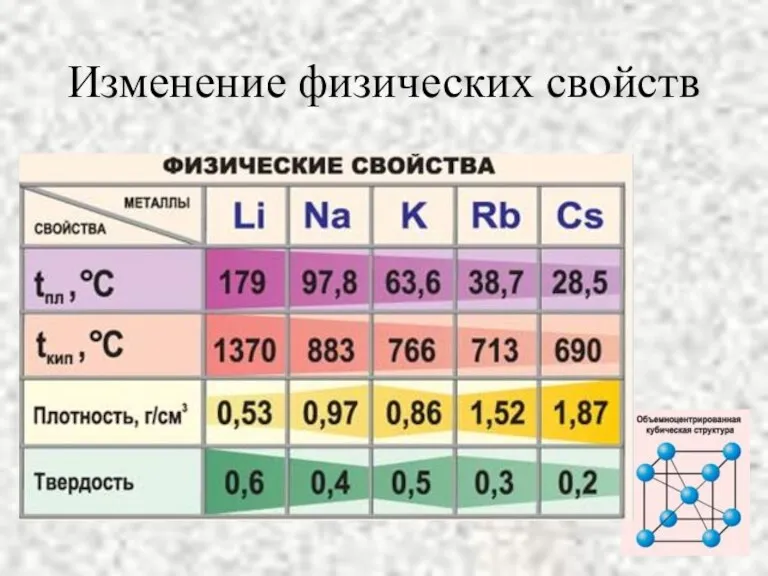
- 8. Изменение физических свойств
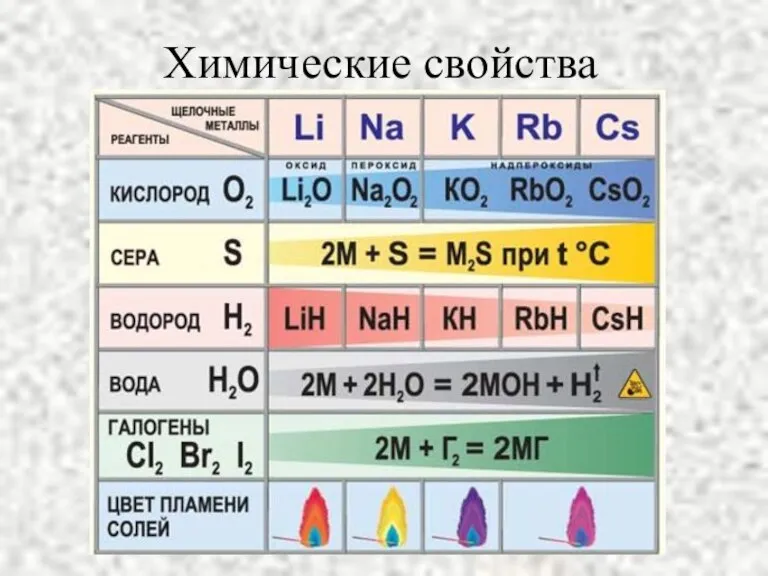
- 9. Химические свойства
- 10. Оксид лития Оксид натрия Оксиды щелочных металлов Составьте общую формулу оксидов.
- 11. KOH – гидроксид калия NaOH – гидроксид натрия LiOH – гидроксид лития Гидроксиды щелочных металлов Какова
- 12. Нахождение в природе Встречаются ли щелочные металлы в природе в свободном состоянии?
- 14. Немного истории Древнегреческий поэт Гомер, назвал поваренную соль «божественной». В те далекие времена она ценилась выше
- 15. Поваренная соль и география Поваренная соль известна человеку с незапамятных времен, и название ее сходно во
- 16. Поваренная соль в организме человека Соль – обязательная составная часть организма человека. Соль поддерживает нормальную деятельность
- 17. Применение поваренной соли Производство химических веществ --- соляной кислоты --- гидроксида натрия --- хлора --- соды
- 18. Сколько нужно времени для того, чтобы съесть пуд соли? Есть поговорка: «Чтобы хорошо узнать человека, надо
- 19. Карбонат калия - поташ Калийная селитра соли щелочных металлов
- 20. Задание На странице 130 учебника найдите ответ на вопрос: чем похожи и чем отличаются кальцинированная, стиральная
- 21. Проверьте Na2CO3 – кальцинированная сода Na2CO3*10Н2О – кристаллическая или стиральная сода Na2НCO3 – питьевая сода
- 22. Тест-проверка Вариант 1. 1-Б, 2-В, 3-В, 4-А,5-А. Вариант 2 1-Б, 2-В, 3-В, 4-Б, 5-А
- 23. Домашнее задание 1 уровень: Прочитать параграф 24, Выяснить: Какая связь между подводной лодкой и щелочными металлами
- 24. О каком элементе идет речь? Хранят обычно в керосине, и бегает он по воде, В природе,
- 26. Скачать презентацию



















 Презентация на тему Мировые природные ресурсы
Презентация на тему Мировые природные ресурсы  Карта желаний
Карта желаний Разработка высоконагруженных проектов(например – сайтов для сообществ)
Разработка высоконагруженных проектов(например – сайтов для сообществ) Финансовые бюджеты: особенности разработки
Финансовые бюджеты: особенности разработки «Восславим женщину-мать, чья любовь не знает преград, чьей грудью вскормлен весь мир! Всё прекрасное в человеке от лучей солнца и
«Восславим женщину-мать, чья любовь не знает преград, чьей грудью вскормлен весь мир! Всё прекрасное в человеке от лучей солнца и Новые решения для превосходного кондиционирования с дополнительным преимуществом мультифункционального загущения передовых ПА
Новые решения для превосходного кондиционирования с дополнительным преимуществом мультифункционального загущения передовых ПА Звук [Ш]
Звук [Ш] ПОРТФОЛИО
ПОРТФОЛИО Презентация
Презентация 2 Университет Прикладных Наук Аванс /Avans University of Applied Sciences Летняя школа /Summer course 2012 An exciting challenge for young internationals.
2 Университет Прикладных Наук Аванс /Avans University of Applied Sciences Летняя школа /Summer course 2012 An exciting challenge for young internationals. Подобные слагаемые
Подобные слагаемые История развития информационных технологий
История развития информационных технологий Способности и мотивация
Способности и мотивация ПРЕЗЕНТАЦИЯ к внеклассному мероприятию по русскому языку Учителя русского языка и литературы Власовой М.В.
ПРЕЗЕНТАЦИЯ к внеклассному мероприятию по русскому языку Учителя русского языка и литературы Власовой М.В. Опыт функционирования сайта www.fsb.ru в кризисных ситуациях полковник Правиков Д.И.
Опыт функционирования сайта www.fsb.ru в кризисных ситуациях полковник Правиков Д.И. Перспективы развития нефтеперерабатывающего комплексаОАО АНК «Башнефть»
Перспективы развития нефтеперерабатывающего комплексаОАО АНК «Башнефть» Презентация на тему Радиоактивность. Ядерные реакции
Презентация на тему Радиоактивность. Ядерные реакции Птицеград
Птицеград Информационные компьютерные технологии в практике логопеда
Информационные компьютерные технологии в практике логопеда Всероссийский налоговый диктант: участвуем вместе!
Всероссийский налоговый диктант: участвуем вместе! USA Etiquette
USA Etiquette Приложение № 4 к ВХ.3196 от 02.07.2020 09_35_35 (58638459 v1)
Приложение № 4 к ВХ.3196 от 02.07.2020 09_35_35 (58638459 v1) Видеонаблюдение (1)
Видеонаблюдение (1) Мастера Сысольского района на юбилейной республиканской выставке декоративно-прикладного искусства и художественных промыслов
Мастера Сысольского района на юбилейной республиканской выставке декоративно-прикладного искусства и художественных промыслов "Времена года на Дону".
"Времена года на Дону". Самый прибыльный бизнес
Самый прибыльный бизнес Моё увлечение кошки и черепахи!
Моё увлечение кошки и черепахи! Формирование социальной среды и развитие внешних связей.
Формирование социальной среды и развитие внешних связей.