Слайд 2 Пептиды и белки представляют собой высокомолекулярные органические соединения, построенные из остатков a-

аминокислот, соединенных между собой пептидными связями.
Слайд 3 Из истории
основу жизни на Земле составляют белки и нуклеиновые кислоты,
белки были

вторичны по отношению к нуклеиновым кислотам.
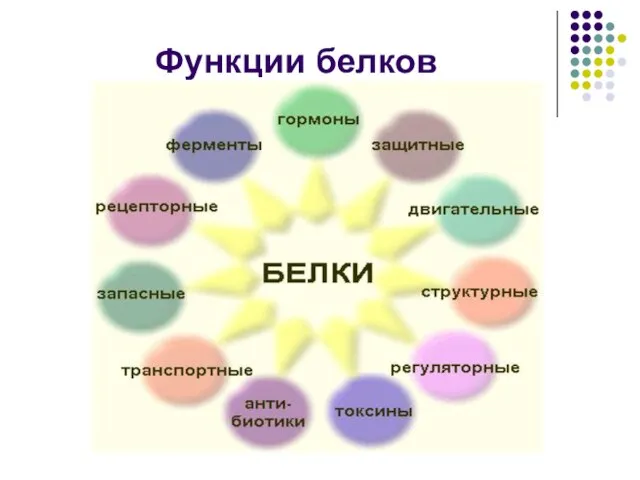
Слайд 4Белки служат питательными веществами, они регулируют обмен веществ, исполняя роль ферментов –

катализаторов обмена веществ, способствуют переносу кислорода по всему организму и его поглощению, играют важную роль в функционировании нервной системы, являются механической основой мышечного сокращения, участвуют в передаче генетической информации и т.д.
Слайд 5 Белки - функциональные молекулы, которые могут состоять:
из одного полипептида,
нескольких

полипептидов – одинаковых или разных,
включать в качестве дополнения к полипептидам другое вещество – олигосахарид, нуклеотид или другое.
Слайд 6Вывод:
Полипептиды состоят из аминокислот.

Слайд 7Пептиды и белки различают в зависимости от величины молекулярной массы. Условно считают,

что пептиды содержат в молекуле до 100, а белки - свыше 100 аминокислотных остатков.
При этом в пептидах различают олигопептиды, содержащие в цепи не более 10 аминокислотных остатков, и полипептиды, содержащие до 100 аминокислотных остатков.
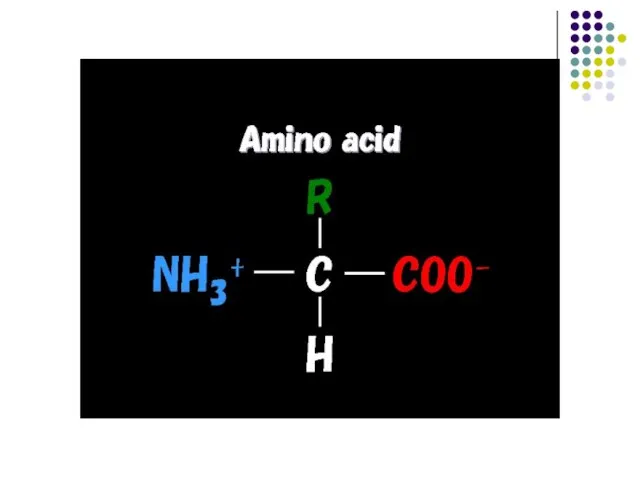
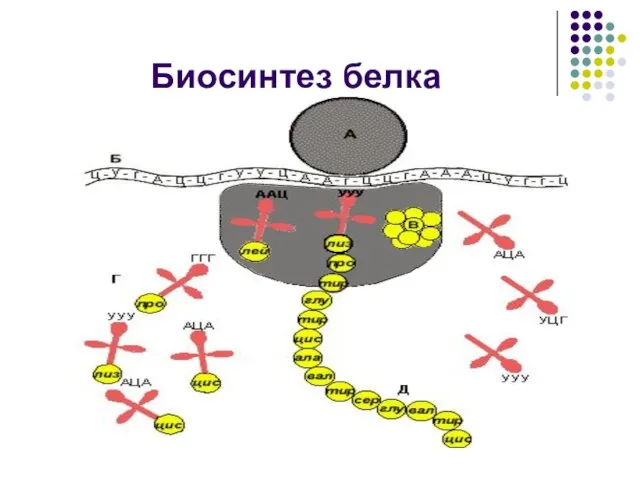
Слайд 8 Аминокислоты объединяются (конденсируются) в белки:
один из двух водородов аминогруппы одной аминокислоты

– OH из гидроксильной группы другой аминокислоты отщепляется с образованием молекулы воды (Н2О);
соответствующие атомы углерода и азота связываются друг с другом с образованием амидной, или пептидной, связи (это прочная ковалентная связь)
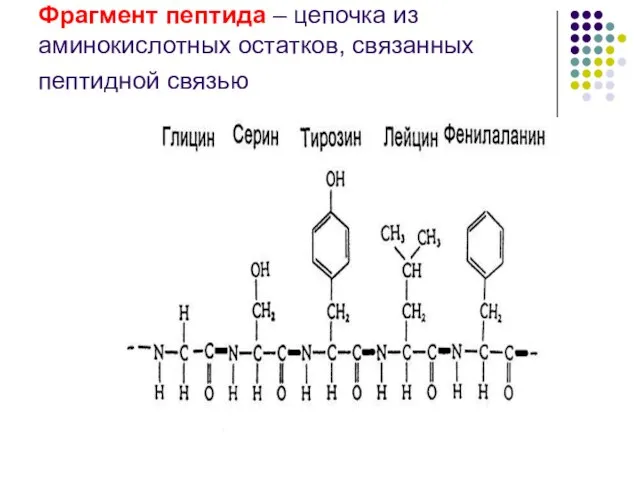
Слайд 9Конструкция полипептидной цепи одинакова для всего многообразия пептидов и белков. Эта цепь

имеет неразветвленное строение и состоит из чередующихся метиновых (CH) и пептидных (CONH) групп. Различия такой цепи заключаются в боковых радикалах, связанных с метиновой группой, и характеризующих ту или иную аминокислоту.
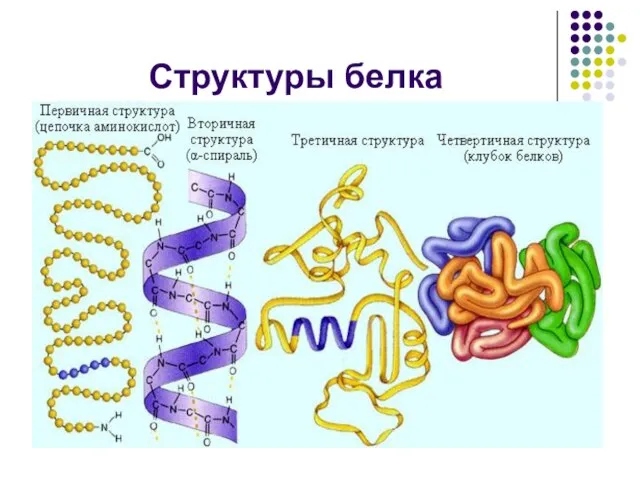
Слайд 10Для полипептидов и белков характерны четыре уровня пространственной организации, которые принято называть

первичной, вторичной, третичной и четвертичной структурами.
Слайд 12Фрагмент пептида – цепочка из аминокислотных остатков, связанных пептидной связью
Слайд 13Структуры белка
Каждая полипептидная цепь расположена в пространстве:
атом водорода, связанный с атомом

азота, образовывает водородную связь с атомом кислорода, пептидную связь.
Слайд 14Первичная структура белка - специфическая аминокислотная последовательность, т.е. порядок чередования a- аминокислотных остатков в

полипептидной цепи.
Вторичная структура белка - конформация полипептидной цепи, т.е. способ скручивания цепи в пространстве за счет водородных связей между группами NH и CO. Одна из моделей вторичной структуры – a- спираль.
Слайд 15Третичная структура белка - трехмерная конфигурация закрученной спирали в пространстве, образованная за счет

дисульфидных мостиков –S–S– между цистеиновыми остатками и ионных взаимодействий.
Четвертичная структура белка - структура, образующаяся за счет взаимодействия между разными полипептидными цепями. Четвертичная структура характерна лишь для некоторых белков, например гемоглобина.
Слайд 22Химические свойства
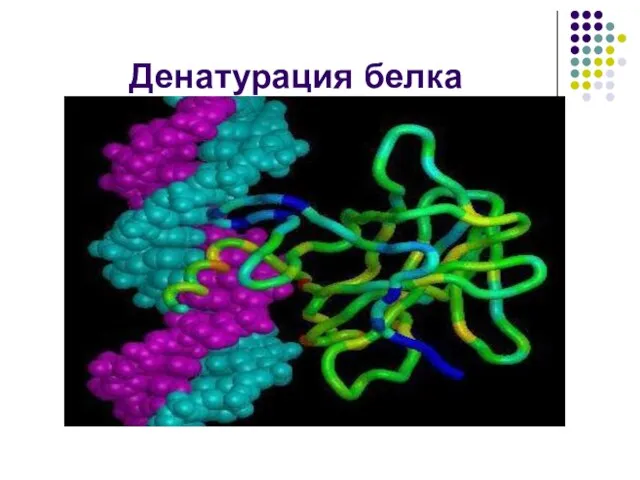
Денатурация. Утрата белком природной (нативной) конформации, сопровождающаяся обычно потерей его биологической

функции, называется денатурацией. С точки зрения структуры белка – это разрушение вторичной и третичной структур белка, обусловленное воздействием кислот, щелочей, нагревания, радиации и т.д.
Слайд 23Гидролиз белков – разрушение первичной структуры белка под действием кислот, щелочей или

ферментов, приводящее к образованию a- аминокислот, из которых он был составлен.
Слайд 243) Качественные реакции на белки:
a) Биуретовая реакция – фиолетовое окрашивание при действии солей меди

(II) в щелочном растворе. Такую реакцию дают все соединения, содержащие пептидную связь.
b) Ксантопротеиновая реакция – появление желтого окрашивания при действии концентрированной азотной кислоты на белки, содержащие остатки ароматических аминокислот (фенилаланина, тирозина).



















 Клеевые ловушки в интегрированной системе защиты растений. Виды и особенности
Клеевые ловушки в интегрированной системе защиты растений. Виды и особенности Изменчивость и ее виды
Изменчивость и ее виды Высшая нервная деятельность
Высшая нервная деятельность Черви
Черви Родословное древо семьи Соколовых
Родословное древо семьи Соколовых Экологические группы водорослей
Экологические группы водорослей Природа и наша безопасность
Природа и наша безопасность 2_5283125600205153429
2_5283125600205153429 Выращивание зелёного лука в различных условиях
Выращивание зелёного лука в различных условиях Общие закономерности физиологии, основные понятия
Общие закономерности физиологии, основные понятия Основы микробиологии, 4 лекция
Основы микробиологии, 4 лекция Половое размножение. Оплодотворение
Половое размножение. Оплодотворение Интересные домашние животные в нашем мире
Интересные домашние животные в нашем мире Биология – наука о жизни
Биология – наука о жизни Биоэлементы
Биоэлементы Органы чувств и их значение
Органы чувств и их значение Царство животные. Урок 1
Царство животные. Урок 1 Функции опорно-двигательной системы
Функции опорно-двигательной системы Виды защищенного грунта. Парники
Виды защищенного грунта. Парники Выращивание рассады огурца для теплицы
Выращивание рассады огурца для теплицы Ядовитые растения
Ядовитые растения Инструменты для груминга
Инструменты для груминга Презентация на тему Кроссворд на тему Рыбы
Презентация на тему Кроссворд на тему Рыбы  Скаты
Скаты Подготовка к ГИА задания С. 9 класс
Подготовка к ГИА задания С. 9 класс Царство Растения
Царство Растения Podstawy anatomiczne
Podstawy anatomiczne himicheskiy_sostav_kletki
himicheskiy_sostav_kletki