Содержание
- 2. Метаболизм представляет собой совокупность двух разнонаправленных процессов: катаболизма, анаболизма и энергетический обмен. Обмен веществ включает: поступление
- 3. Экзергонические реакции ΔG 0 1г. белков – 17кДж (4,2ккал) 1г. углеводов ̴ 17кДж (4,1ккал) 1г. жиров
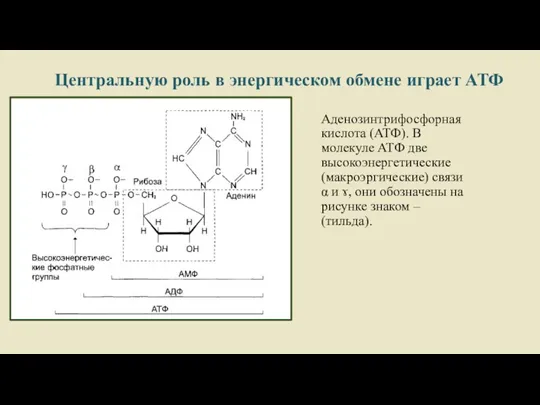
- 4. Центральную роль в энергическом обмене играет АТФ Аденозинтрифосфорная кислота (АТФ). В молекуле АТФ две высокоэнергетические (макроэргические)
- 5. Энергия Гиббса гидролиза некоторых соединений Если энергия, освобождающаяся при реакциях гидролиза превышает 30 кДж/моль, то гидролизуемую
- 6. Наиболее важными экзергоническими реакциями метаболизма являются реакции окисления органических веществ, в которых используется кислород и образуется
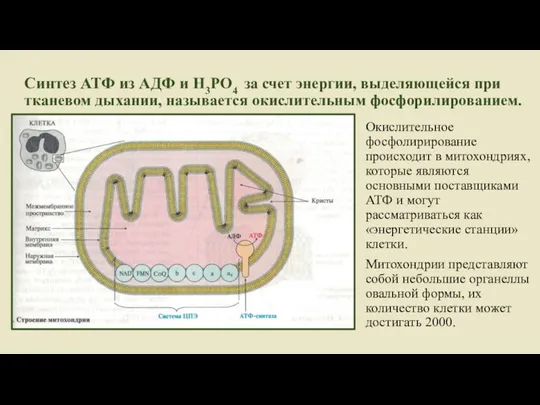
- 7. Синтез АТФ из АДФ и Н3РО4 за счет энергии, выделяющейся при тканевом дыхании, называется окислительным фосфорилированием.
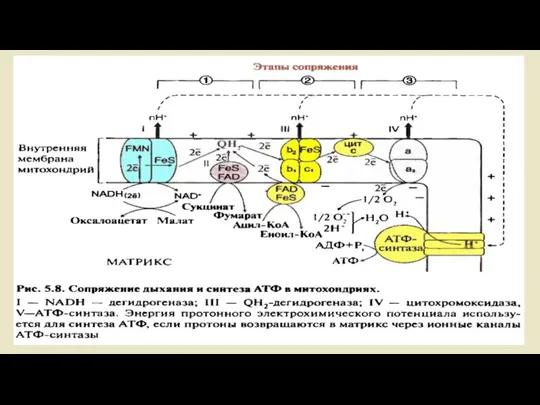
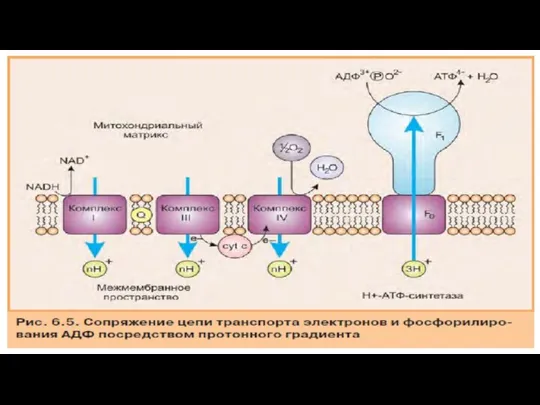
- 8. Функция дыхательной цепи заключается в ситезе АТФ, которая затем может использоваться для энергетически невыгодных реакциях. Хемиосмотическая
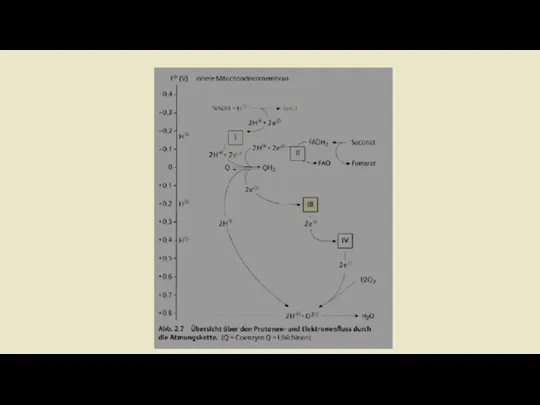
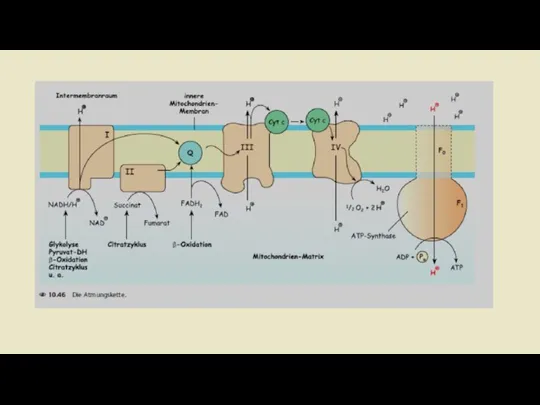
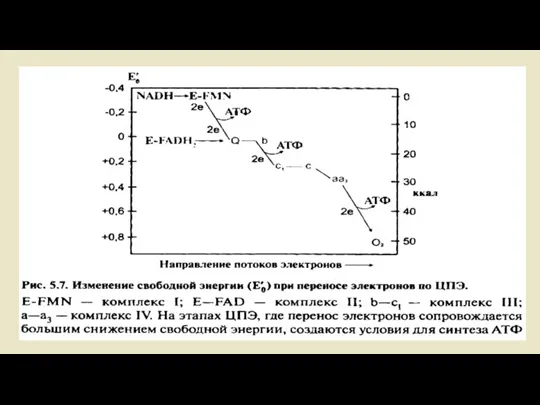
- 10. Дыхательная цепь как цепь переноса электронов -Химическая реакция, лежащая в основе образования воды в дыхательной цепи,
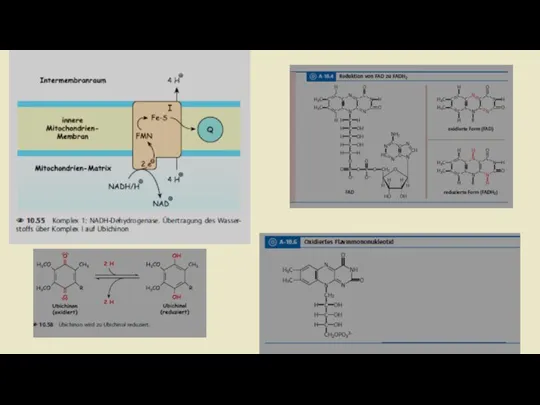
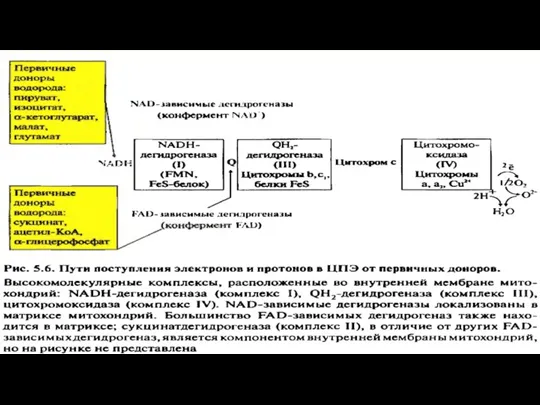
- 13. Комплексы дыхательной цепи Комплекс 1: НАДН-убихинон-редуктаза ln комплекс I происходит перенос электронов от NADH + H
- 15. Кластер железасерный встречаются в разных вариантах. В качестве простетической группы, они координированы с различными остатками цистеинабелка.
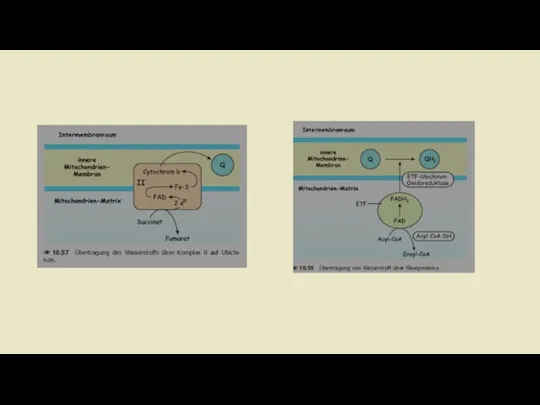
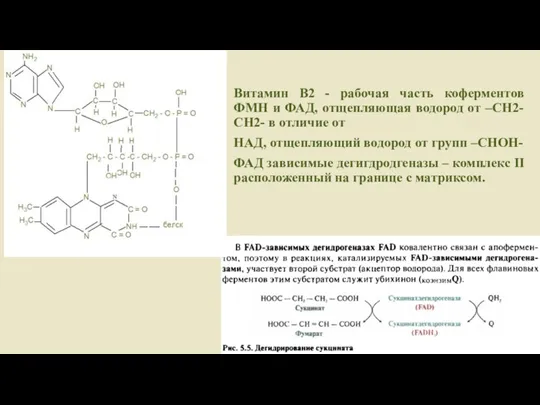
- 16. Комплекс II: Сукцинат-убихинон-редуктаза Комплекс II дыхательной цепи одновременно является ферментом цитратного цикла, а именно сукцинатдегидрогеназой. Это
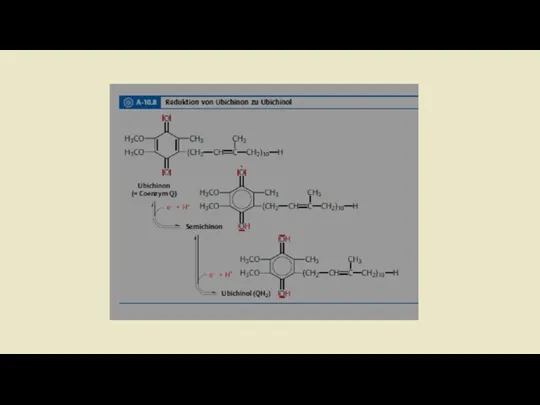
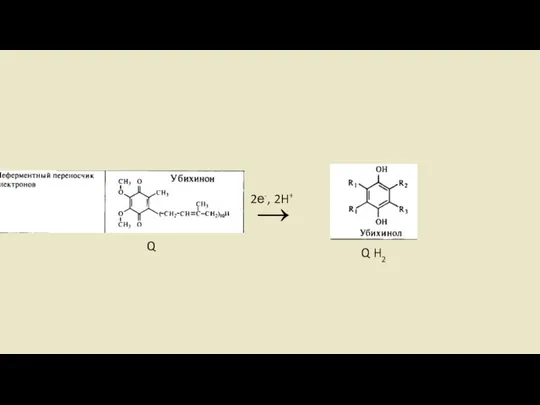
- 18. Ubichinon-Ubichino Системы Убихинон или кофермент Q состоит из одного хинона и одной изопреновая боковой цепи. Структурно
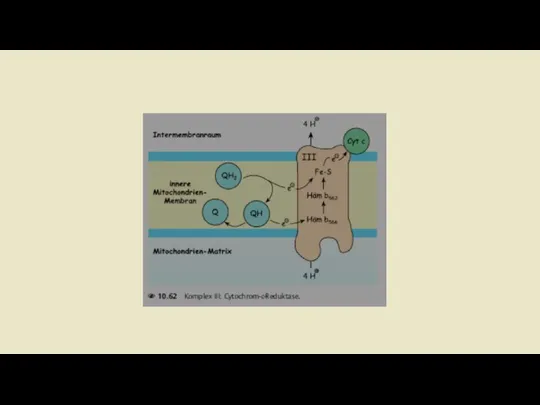
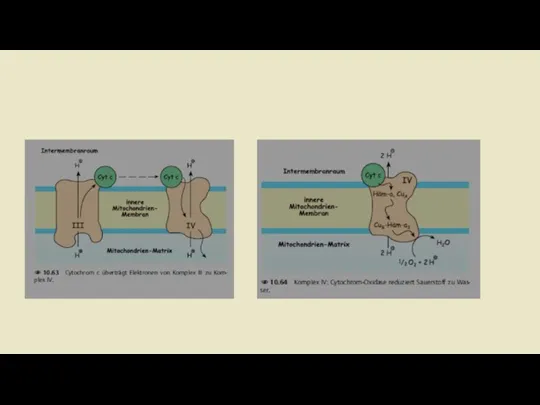
- 20. Комплекс III: Убихинол-цитохром с-редуктаза Задача комплекса 3 теперь заключается в передаче электронов убихинола на цитохром С.
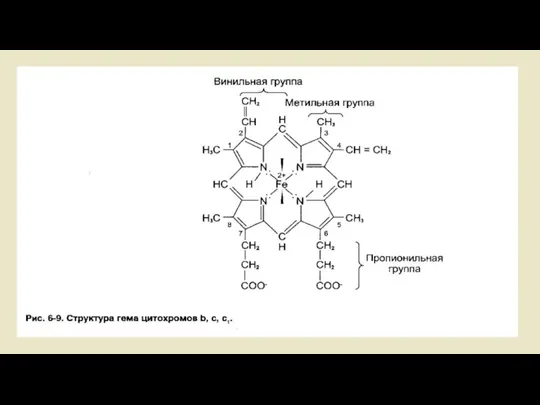
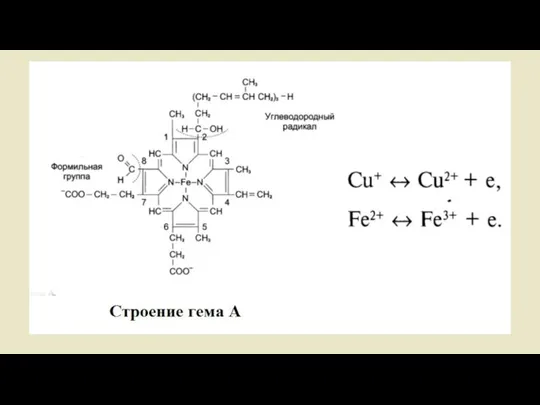
- 22. Цитохромы Цитохромы - это гемсодержащие белки. В видимом свете спектра поглощения востановительные группы гема имеют три
- 23. Комплекс IV: цитохром-с-оксидаза Задача комплекса IV заключается в переносе электронов с цитохрома с на молекулярный кислород.
- 25. Комплекс V: АТФ-синтаза Комплексы I. lll и IV способствуют созданию протонного градиента через внутреннюю мембрану митохондрий.
- 26. Строение и механизм действия АТФ - синтетазы. А – F0 и F1 – комплексы АТФ –
- 28. Коэффициент фосфорилирования P/O Коэффициент Р/О – это отношение количества неорганического фосфата, включенного в молекулу АТФ АТФ-синтазой,
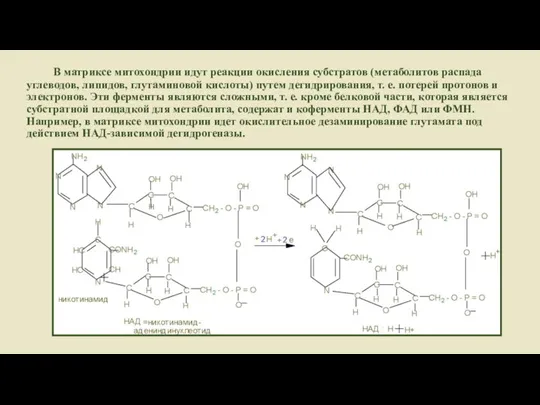
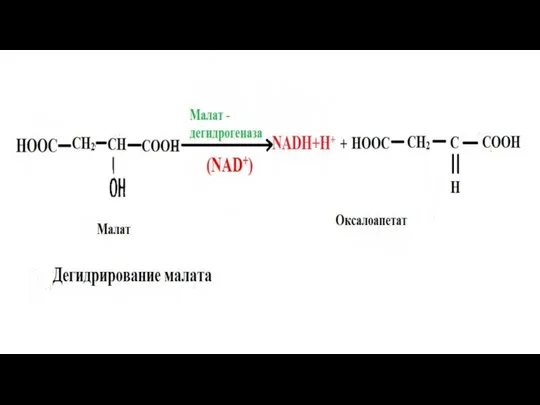
- 31. Большинство дегидрогеназ, поставляющих электроны в межмембранные пространства содержат НАД. Они катализируют реакции типа R – CHOH
- 32. В матриксе митохондрии идут реакции окисления субстратов (метаболитов распада углеводов, липидов, глутаминовой кислоты) путем дегидрирования, т.
- 36. Строение железо-серных центров Ι - FeS - центр; атом железа связан координационными связями с четырьмя атомами
- 37. → 2е-, 2H+ Q Q H2
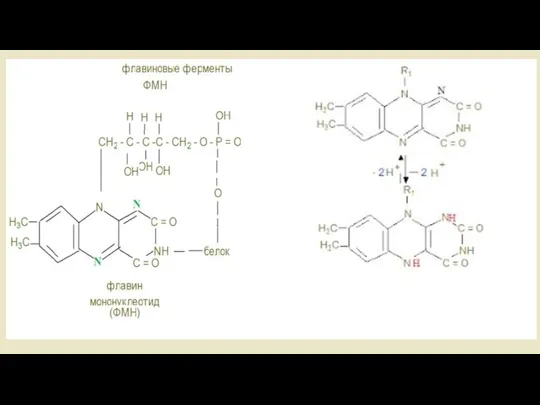
- 38. Витамин В2 - рабочая часть коферментов ФМН и ФАД, отщепляющая водород от –СН2- СН2- в отличие
- 41. На внутренней мембране митохондрии существует система переносчиков, их действие векторно. Они переносят протоны и электроны с
- 43. Протоны перенесенные в межмембранное пространство создают протонный градиент подкисляя его 1,4 рН. Кроме того, появляется разность
- 45. Механизм разобщения дыхания и фосфорилирования. Протонированная форма 2,4 – динитрофенола переносит протоны через внутреннюю мембрану митохондрий
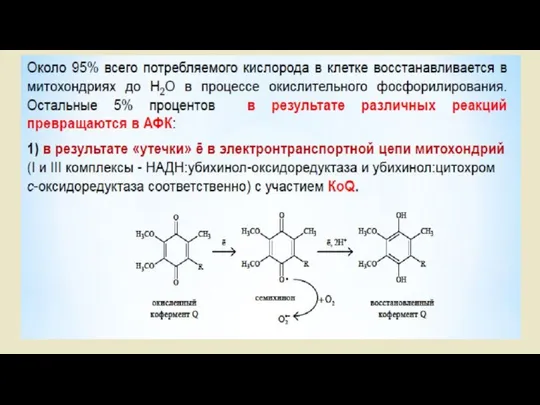
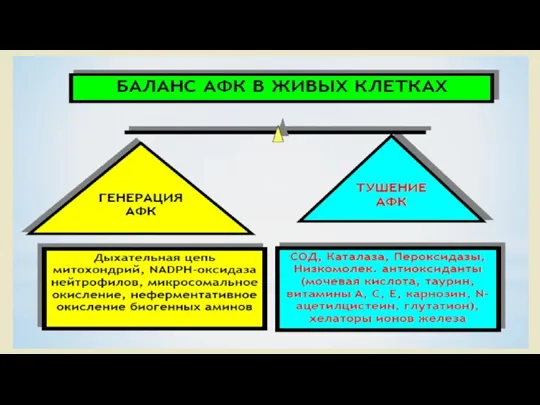
- 46. Активные формы кислорода и антиоксидантные системы. Проблема свободных радикалов в последнее десятилетие произвела настоящую революцию в
- 47. В эритроцитах окисление иона железа гемоглобина способствует образованию супероксидоного аниона. Hb (Fe2+) + O2 →MtHb (Fe+3)
- 48. Примеры свободных радикалов.
- 49. 2. ионы – гипохлорит -ион ClO4 – сопряженное основание для хлорноватистой кислоты, активный компонент отбеливателей. 3.
- 50. Образование токсичных форм при постепенном восстановлении кислорода.
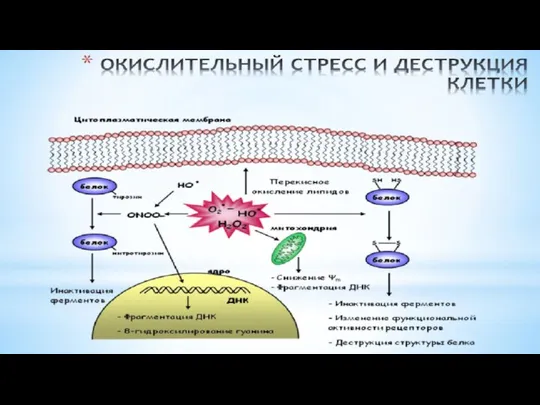
- 53. Свободно-радикальное окисление нарушает структуру нуклеиновых кислот, белков и, особенно, непредельные жирные кислоты (липиды), принимающие электрон от
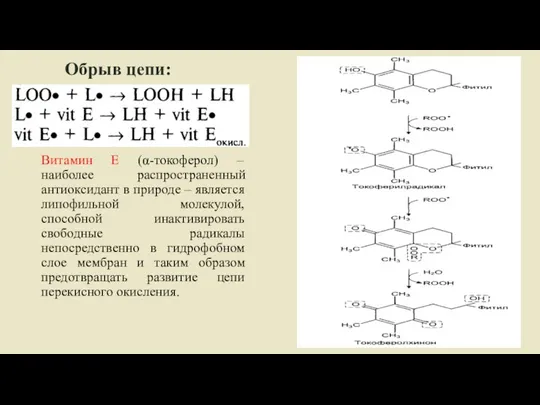
- 54. Обрыв цепи: Витамин Е (α-токоферол) – наиболее распространенный антиоксидант в природе – является липофильной молекулой, способной
- 55. В эритроцитах:
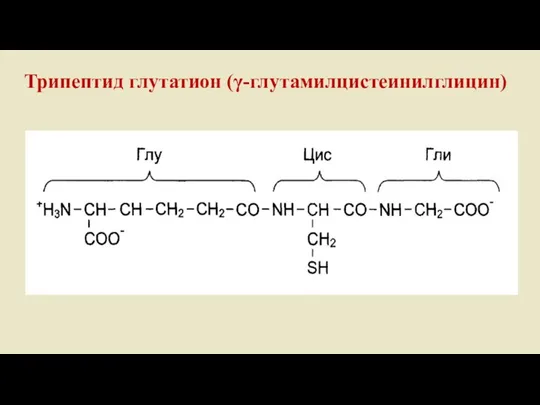
- 56. Трипептид глутатион (γ-глутамилцистеинилглицин)
- 57. Кроме витамина Е антиоксидантами являются: витамин С, β−каротин. Во-первых, витамин С восстанавливает окисленную форму витамина Е.
- 61. Скачать презентацию
































 Африканские слоны. 1 класс
Африканские слоны. 1 класс Значение бактерий
Значение бактерий Дыхательные движения. Регуляция дыхания
Дыхательные движения. Регуляция дыхания Презентация на тему История собаки динго
Презентация на тему История собаки динго  Генномодифицированные продукты
Генномодифицированные продукты Микробиологические, вирусологические и иммунологические термины на русском языке и их значения
Микробиологические, вирусологические и иммунологические термины на русском языке и их значения Синергетики гомеорезов биологических систем. Разработка новой междисциплинарной науки
Синергетики гомеорезов биологических систем. Разработка новой междисциплинарной науки Презентация на тему Паразитирующие жгутиконосцы
Презентация на тему Паразитирующие жгутиконосцы  Механизм секреции желчи
Механизм секреции желчи Физиология гепато-билиарной системы
Физиология гепато-билиарной системы Презентация на тему СТРОЕНИЕ ПТИЦ
Презентация на тему СТРОЕНИЕ ПТИЦ  Грибы и их влияние на организм человека
Грибы и их влияние на организм человека Капустные овощные растения
Капустные овощные растения Проект ”Наиболее распространённые грибы Звенигородской биостанции и их экологические роли”
Проект ”Наиболее распространённые грибы Звенигородской биостанции и их экологические роли”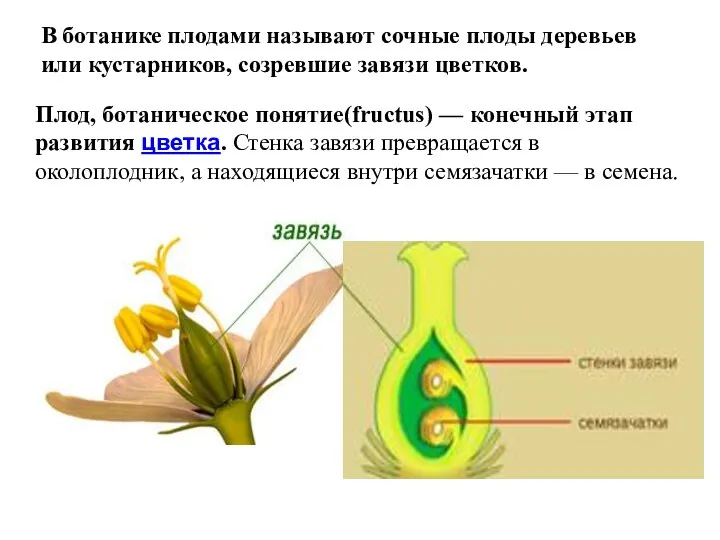 SVEZhIE_PLODY
SVEZhIE_PLODY Органы чувств и анализаторы
Органы чувств и анализаторы Поле
Поле Что такое туман?
Что такое туман? Роль меди в организме человека
Роль меди в организме человека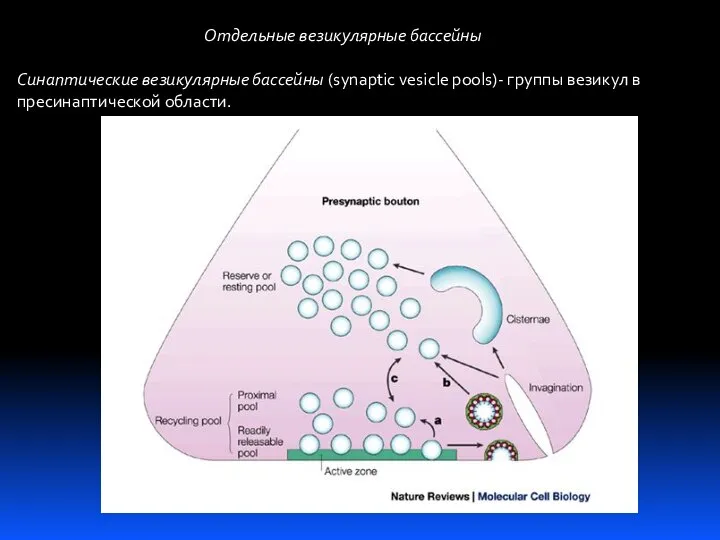 Отдельные везикулярные бассейны. Синаптические везикулярные бассейны - группы везикул в пресинаптической области
Отдельные везикулярные бассейны. Синаптические везикулярные бассейны - группы везикул в пресинаптической области Гемофилия
Гемофилия В мире животных и растений
В мире животных и растений 4. 1. Характеристика и систематика растений
4. 1. Характеристика и систематика растений Основи культури in vitro рослин
Основи культури in vitro рослин Презентация на тему Почвенное питание растений: понятие
Презентация на тему Почвенное питание растений: понятие  § 53. Заболевания и повреждения глаз 8 класс биология
§ 53. Заболевания и повреждения глаз 8 класс биология Темновая фаза фотосинтеза. Цикл Кальвина
Темновая фаза фотосинтеза. Цикл Кальвина Презентация на тему Скорпионы
Презентация на тему Скорпионы