Содержание
- 2. Электричество и нервная система Представления о том, что нервные импульсы живых существ имеют электрическую природу, восходят
- 3. Электричество и мозг Ричард Катон (1842—1926) — английский физиолог и хирург, профессор, член Лондонского королевского общества,
- 4. После катона Исследования электрической активности мозга на границе XIX и XX веков активно велись и на
- 5. Электроцереброграмма Правдич-Неминский регистрировал электрическую активность мозга животных при помощи струнного гальванометра . Его записи, выполненные в
- 6. SCAN Ханс Бергер (1873—1941) — немецкий физиолог и психиатр, создатель электроэнцефалографического метода регистрации мозговой активности. В
- 7. Получение карты электромагнитной активности Позитронная эмиссионная томография (ПЭТ, PET), она же двухфотонная эмиссионная томография — радионуклидный
- 8. Получение карты электромагнитной активности SQUID — сверхпроводящий квантовый интерферометр SERF-магнитометр (свободный от спин-обменного уширения) Феррит-гранатовая мембрана
- 9. ИЗОБРАЖЕНИЯ ИЗ МОЗГА Реконструкция наблюдаемых человеком объектов на основе данных fMRI, продемонстрированная в работе компании ATR
- 10. ONCE UPON A TIME…
- 11. ПЕРЕДАЧА данных из МОЗГа в мозг Криста и Татьяна Хоган. В утробе матери они срослись головами.
- 12. Звук Кохлеарный имплантат — медицинский прибор, протез, позволяющий компенсировать потерю слуха некоторым пациентам с выраженной или
- 13. СЛУХ
- 14. ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ Нил Харбиссон — британский деятель современного искусства, музыкант, художник и «киборг-активист», известный
- 15. ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ Одним из первых учёных, создавших зрительный протез, стал частный исследователь Уильям Добелл.
- 16. ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
- 17. ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ 30 июня 2017 года в НИЦ офтальмологии ФГБОУ ВО РНИМУ имени Н.И.
- 18. Оптогенетика Под воздействием синего света ChR2 открывает доступ притоку Na+ в клетку, а связанный с опсином
- 19. Оптогенетика 2015, август — FDA выдало разрешение компании Retrosense на испытание на людях препарата RST-001 для
- 20. Оптогенетика Существующая концепция предполагает использование аденоассоциированного вируса (AAV) серотипа 2 (либо его мутантной версии) для доставки
- 21. Оптогенетика
- 22. Оптогенетика Изначально для оптогенетических манипуляций использовали управляемые светом натриевые каналы, с помощью которых можно было активировать
- 23. Оптогенетика
- 24. Оптогенетика Объём глобального оптогенетического рынка в 2016 году составил $19.36 млн и к 2022 году планируется
- 25. Искусственный гиппокамп Исследователи из университета Южной Калифорнии (USC) уже не первый год работают над созданием искусственного
- 26. BLUE BRAIN & Human brain project 2005: завершение работ по созданию первой клеточной модели. Ноябрь 2007:
- 27. альтернативы
- 28. Спасибо за внимание!
- 30. Скачать презентацию
Слайд 2Электричество и нервная система
Представления о том, что нервные импульсы живых существ имеют
Электричество и нервная система
Представления о том, что нервные импульсы живых существ имеют
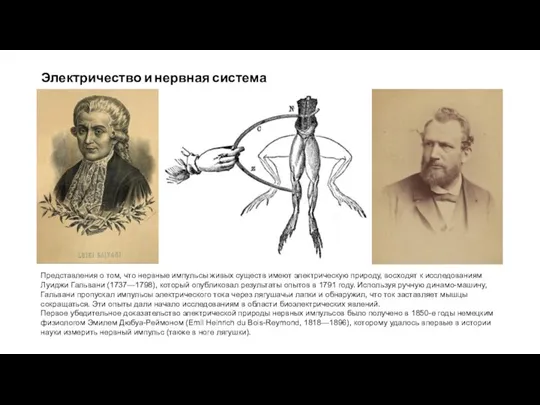
Первое убедительное доказательство электрической природы нервных импульсов было получено в 1850-е годы немецким физиологом Эмилем Дюбуа-Реймоном (Emil Heinrich du Bois-Reymond, 1818—1896), которому удалось впервые в истории науки измерить нервный импульс (также в ноге лягушки).
Слайд 3Электричество и мозг
Ричард Катон (1842—1926) — английский физиолог и хирург, профессор, член
Электричество и мозг
Ричард Катон (1842—1926) — английский физиолог и хирург, профессор, член

В своих опытах Катон использовал устройство, называемое отражающим гальванометром. Гальванометр состоял из провода и катушки, которые вибрировали при обнаружении слабых токов. Прибор также имел зеркало, прикреплённое к катушкам, и яркая кислородно-водородная лампа направляла на зеркало узкий луч света, который затем, отражаясь, попадал на изображённую на стене затемнённой комнаты шкалу длиной около полутора метров. Чем сильнее был сигнал, тем выше поднимался по шкале световой луч. Катон прикасался электродами своего инструмента к поверхности мозга во вскрытых черепах кроликов, кошек и обезьян. Катон обнаружил, что внешняя поверхность серого вещества имела положительный заряд по отношению к глубоким структурам мозга. Он также отметил, что электрические токи головного мозга, по-видимому, имеют отношение к основной функции: «Когда какая-либо часть серого вещества находится в состоянии функциональной активности, его электрический ток обычно демонстрирует изменения в отрицательную сторону».
Когда животное двигалось, жевало пищу или улавливало глазами свет, прибор регистрировал возрастание электрической активности. Мысли, заметил Катон, также порождали активность. Он подключил обезьяну к устройству и записывал ток, связанный с жеванием. «Когда я показал обезьяне изюм, но не дал ей его, произошло небольшое отрицательное изменение тока», — писал он.
Слайд 4После катона
Исследования электрической активности мозга на границе XIX и XX веков активно
После катона
Исследования электрической активности мозга на границе XIX и XX веков активно

Три российских физиолога: Николай Введенский (Николай Евгеньевич Введенский, 1852—1922), Павел Кауфман (Павел Юрьевич Кауфман, 1877–1951) и Владимир Правдич-Неминский (Владимир Владимирович Правдич-Неминский, 1879–1952) продолжили исследования в этом направлении.
Ученик самого Сеченова (Иван Михайлович Сеченов, 1829—1905), Введенский в 1884 году защитил магистерскую диссертацию по теме «Телефонические исследования над электрическими явлениями в мышечных и нервных аппаратах». В этой работе рассматривается, среди прочего, использование телефонного контура для регистрации нервных импульсов в обнажённых мозгах лягушек, кроликов и собак. Введенскому удалось подтвердить результаты, полученные его учителем с применением гальванометра.
Слайд 5Электроцереброграмма
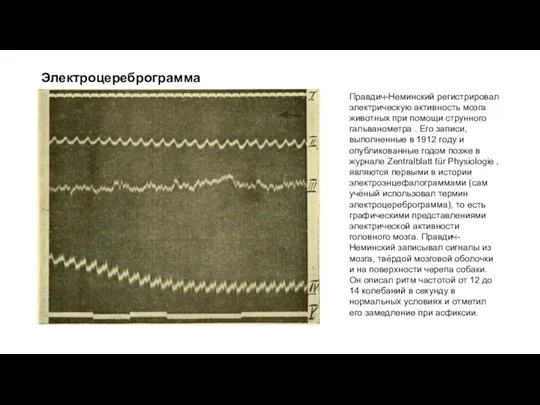
Правдич-Неминский регистрировал электрическую активность мозга животных при помощи струнного гальванометра . Его
Электроцереброграмма
Правдич-Неминский регистрировал электрическую активность мозга животных при помощи струнного гальванометра . Его
Слайд 6SCAN
Ханс Бергер (1873—1941) — немецкий физиолог и психиатр, создатель электроэнцефалографического метода регистрации
SCAN
Ханс Бергер (1873—1941) — немецкий физиолог и психиатр, создатель электроэнцефалографического метода регистрации
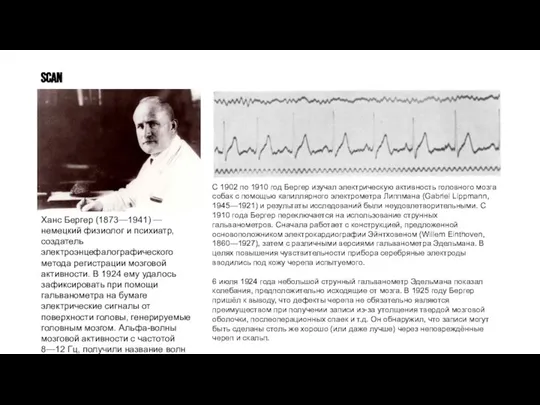
С 1902 по 1910 год Бергер изучал электрическую активность головного мозга собак с помощью капиллярного электрометра Липпмана (Gabriel Lippmann, 1945—1921) и результаты исследований были неудовлетворительными. С 1910 года Бергер переключается на использование струнных гальванометров. Сначала работает с конструкцией, предложенной основоположником электрокардиографии Эйнтховеном (Willem Einthoven, 1860—1927), затем с различными версиями гальванометра Эдельмана. В целях повышения чувствительности прибора серебряные электроды вводились под кожу черепа испытуемого.
6 июля 1924 года небольшой струнный гальванометр Эдельмана показал колебания, предположительно исходящие от мозга. В 1925 году Бергер пришёл к выводу, что дефекты черепа не обязательно являются преимуществом при получении записи из-за утолщения твердой мозговой оболочки, послеоперационных спаек и т.д. Он обнаружил, что записи могут быть сделаны столь же хорошо (или даже лучше) через неповреждённые череп и скальп.
Слайд 7Получение карты электромагнитной активности
Позитронная эмиссионная томография (ПЭТ, PET), она же двухфотонная эмиссионная
Получение карты электромагнитной активности
Позитронная эмиссионная томография (ПЭТ, PET), она же двухфотонная эмиссионная
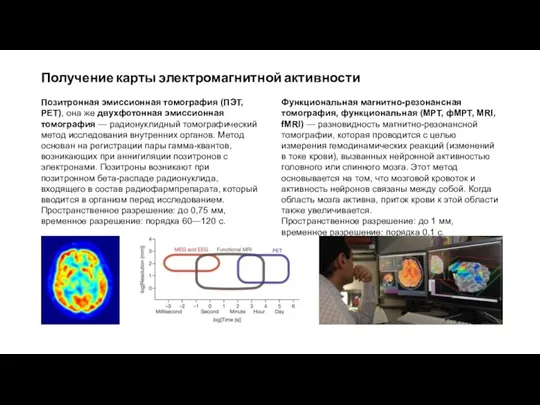
Пространственное разрешение: до 0,75 мм, временное разрешение: порядка 60—120 с.
Функциональная магнитно-резонансная томография, функциональная (МРТ, фМРТ, MRI, fMRI) — разновидность магнитно-резонансной томографии, которая проводится с целью измерения гемодинамических реакций (изменений в токе крови), вызванных нейронной активностью головного или спинного мозга. Этот метод основывается на том, что мозговой кровоток и активность нейронов связаны между собой. Когда область мозга активна, приток крови к этой области также увеличивается.
Пространственное разрешение: до 1 мм, временное разрешение: порядка 0,1 с.
Слайд 8Получение карты электромагнитной активности
SQUID — сверхпроводящий квантовый интерферометр
SERF-магнитометр (свободный от спин-обменного уширения)
Получение карты электромагнитной активности
SQUID — сверхпроводящий квантовый интерферометр
SERF-магнитометр (свободный от спин-обменного уширения)
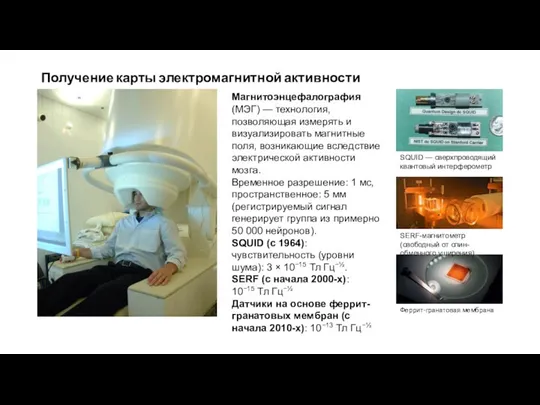
Феррит-гранатовая мембрана
Магнитоэнцефалография (МЭГ) — технология, позволяющая измерять и визуализировать магнитные поля, возникающие вследствие электрической активности мозга.
Временное разрешение: 1 мс, пространственное: 5 мм (регистрируемый сигнал генерирует группа из примерно 50 000 нейронов).
SQUID (c 1964): чувствительность (уровни шума): 3 × 10−15 Тл Гц−½.
SERF (c начала 2000-х): 10−15 Тл Гц−½
Датчики на основе феррит-гранатовых мембран (с начала 2010-х): 10−13 Тл Гц−½
Слайд 9ИЗОБРАЖЕНИЯ ИЗ МОЗГА
Реконструкция наблюдаемых человеком объектов на основе данных fMRI, продемонстрированная в
ИЗОБРАЖЕНИЯ ИЗ МОЗГА
Реконструкция наблюдаемых человеком объектов на основе данных fMRI, продемонстрированная в
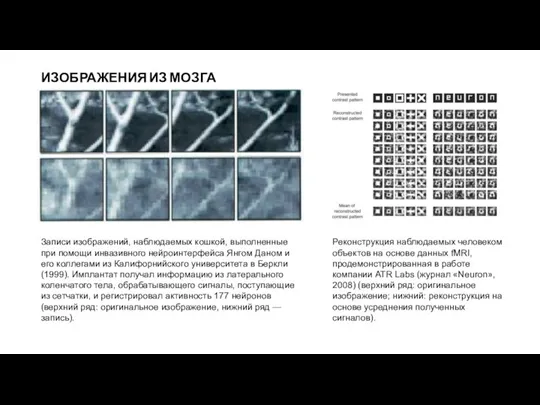
Записи изображений, наблюдаемых кошкой, выполненные при помощи инвазивного нейроинтерфейса Янгом Даном и его коллегами из Калифорнийского университета в Беркли (1999). Имплантат получал информацию из латерального коленчатого тела, обрабатывающего сигналы, поступающие из сетчатки, и регистрировал активность 177 нейронов (верхний ряд: оригинальное изображение, нижний ряд — запись).
Слайд 10ONCE UPON A TIME…
ONCE UPON A TIME…

Слайд 11ПЕРЕДАЧА данных из МОЗГа в мозг
Криста и Татьяна Хоган. В утробе матери
ПЕРЕДАЧА данных из МОЗГа в мозг
Криста и Татьяна Хоган. В утробе матери
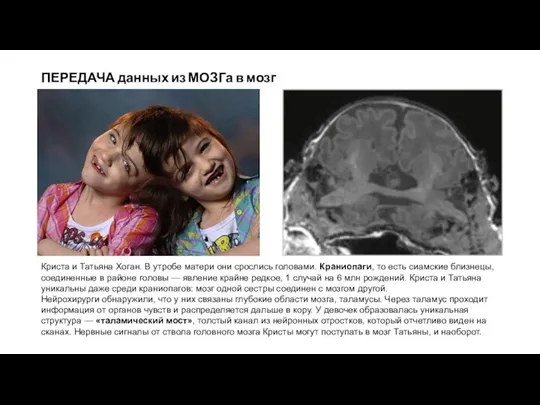
Нейрохирурги обнаружили, что у них связаны глубокие области мозга, таламусы. Через таламус проходит информация от органов чувств и распределяется дальше в кору. У девочек образовалась уникальная структура — «таламический мост», толстый канал из нейронных отростков, который отчетливо виден на сканах. Нервные сигналы от ствола головного мозга Кристы могут поступать в мозг Татьяны, и наоборот.
Слайд 12Звук
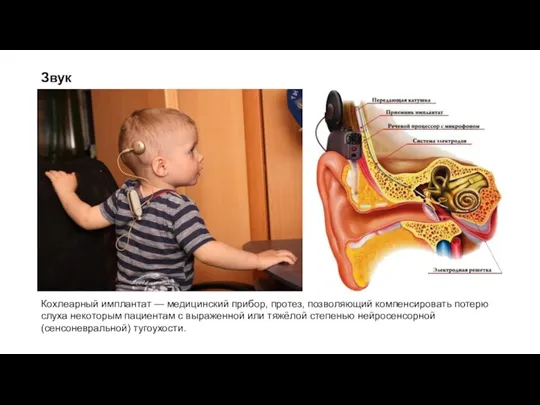
Кохлеарный имплантат — медицинский прибор, протез, позволяющий компенсировать потерю слуха некоторым пациентам
Звук
Кохлеарный имплантат — медицинский прибор, протез, позволяющий компенсировать потерю слуха некоторым пациентам
Слайд 13СЛУХ
СЛУХ

Слайд 14ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
Нил Харбиссон — британский деятель современного искусства, музыкант, художник
ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
Нил Харбиссон — британский деятель современного искусства, музыкант, художник

Слайд 15ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
Одним из первых учёных, создавших зрительный протез, стал частный
ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
Одним из первых учёных, создавших зрительный протез, стал частный

Первый прототип Добелл был имплантирован в 1978 году «Джерри», мужчине, потерявшему зрение в зрелом возрасте. Однослойный массив из 68 электродов был имплантирован в визуальную кору Джерри и был способен передавать в мозг изображение в тонах серого цвета в ограниченной области зрения с низкой частотой кадров.
В 2002 году Дженс Науманн стал первым в серии из 16 пациентов, получившим зрительный протез на коммерческой основе. В 2004 году Добелл умер, оставив большую часть работ недокументированной.
Слайд 16ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ

Слайд 17ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
30 июня 2017 года в НИЦ офтальмологии ФГБОУ ВО
ПЕРЕДАЧА ИЗОБРАЖЕНИЯ В МОЗГ
30 июня 2017 года в НИЦ офтальмологии ФГБОУ ВО
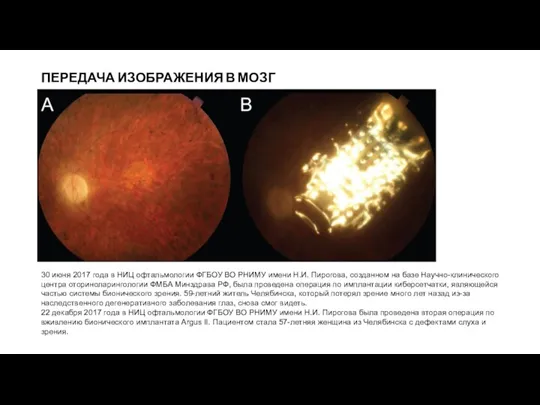
22 декабря 2017 года в НИЦ офтальмологии ФГБОУ ВО РНИМУ имени Н.И. Пирогова была проведена вторая операция по вживлению бионического имплантата Argus II. Пациентом стала 57-летняя женщина из Челябинска с дефектами слуха и зрения.
Слайд 18Оптогенетика
Под воздействием синего света ChR2 открывает доступ притоку Na+ в клетку, а
Оптогенетика
Под воздействием синего света ChR2 открывает доступ притоку Na+ в клетку, а
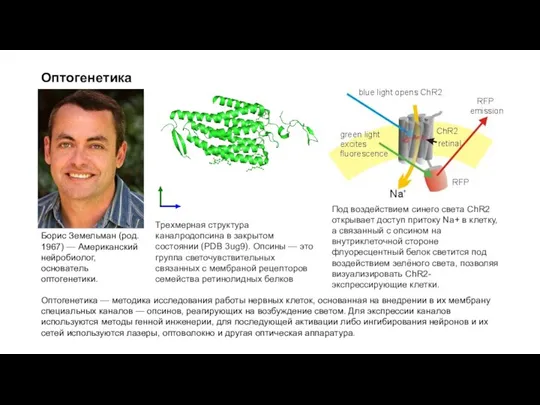
Трехмерная структура каналродопсина в закрытом состоянии (PDB 3ug9). Опсины — это группа светочувствительных связанных с мембраной рецепторов семейства ретинолидных белков
Оптогенетика — методика исследования работы нервных клеток, основанная на внедрении в их мембрану специальных каналов — опсинов, реагирующих на возбуждение светом. Для экспрессии каналов используются методы генной инженерии, для последующей активации либо ингибирования нейронов и их сетей используются лазеры, оптоволокно и другая оптическая аппаратура.
Борис Земельман (род. 1967) — Американский нейробиолог, основатель оптогенетики.
Слайд 19Оптогенетика
2015, август — FDA выдало разрешение компании Retrosense на испытание на людях
Оптогенетика
2015, август — FDA выдало разрешение компании Retrosense на испытание на людях
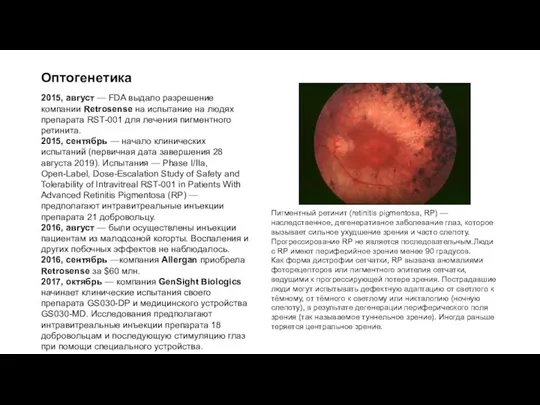
2015, сентябрь — начало клинических испытаний (первичная дата завершения 28 августа 2019). Испытания — Phase I/IIa, Open-Label, Dose-Escalation Study of Safety and Tolerability of Intravitreal RST-001 in Patients With Advanced Retinitis Pigmentosa (RP) — предполагают интравитреальные инъекции препарата 21 добровольцу.
2016, август — были осуществлены инъекции пациентам из малодозной когорты. Воспаления и других побочных эффектов не наблюдалось.
2016, сентябрь —компания Allergan приобрела Retrosense за $60 млн.
2017, октябрь — компания GenSight Biologics начинает клинические испытания своего препарата GS030-DP и медицинского устройства GS030-MD. Исследования предполагают интравитреальные инъекции препарата 18 добровольцам и последующую стимуляцию глаз при помощи специального устройства.
Пигментный ретинит (retinitis pigmentosa, RP) — наследственное, дегенеративное заболевание глаз, которое вызывает сильное ухудшение зрения и часто слепоту. Прогрессирование RP не является последовательным.Люди с RP имеют периферийное зрение менее 90 градусов.
Как форма дистрофии сетчатки, RP вызвана аномалиями фоторецепторов или пигментного эпителия сетчатки, ведущими к прогрессирующей потере зрения. Пострадавшие люди могут испытывать дефектную адаптацию от светлого к тёмному, от тёмного к светлому или никталопию (ночную слепоту), в результате дегенерации периферического поля зрения (так называемое туннельное зрение). Иногда раньше теряется центральное зрение.
Слайд 20Оптогенетика
Существующая концепция предполагает использование аденоассоциированного вируса (AAV) серотипа 2 (либо его мутантной
Оптогенетика
Существующая концепция предполагает использование аденоассоциированного вируса (AAV) серотипа 2 (либо его мутантной

Слайд 21Оптогенетика
Оптогенетика
Слайд 22Оптогенетика
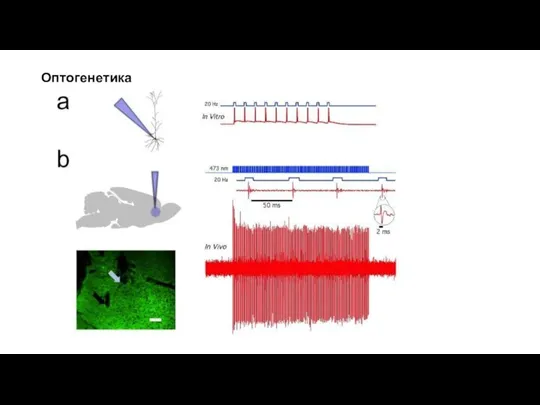
Изначально для оптогенетических манипуляций использовали управляемые светом натриевые каналы, с помощью которых можно было
Оптогенетика
Изначально для оптогенетических манипуляций использовали управляемые светом натриевые каналы, с помощью которых можно было

Схематическое изображение управляемого светом калиевого канала. На синий свет реагирует часть чувствительного белка, позаимствованная у овса (LOV2, light-oxygen-voltage-sensing domain 2). Она изменяет конформацию и открывает калиевый канал, природный хозяин которого — хлоровирус PBCV. Буквами обозначены различные домены белков (TM1 и TM2 — трансмембранные).
Слайд 23Оптогенетика
Оптогенетика

Слайд 24Оптогенетика
Объём глобального оптогенетического рынка в 2016 году составил $19.36 млн и к
Оптогенетика
Объём глобального оптогенетического рынка в 2016 году составил $19.36 млн и к

Компании, упоминающиеся в докладе:
Allergan
Applied Genetic Technologies Corporation
Bionic Sight
Boehringer Ingelheim
Bruker
Circuit therapeutic
Coherent, Inc.
GenSight Biologics S.A.
Jackson Laboratory
Laserglow Technologies
Noldus Information technology
Regenexbio, Inc.
RetroSense Therapeutics
Thorlabs, Inc
Слайд 25Искусственный гиппокамп
Исследователи из университета Южной Калифорнии (USC) уже не первый год работают
Искусственный гиппокамп
Исследователи из университета Южной Калифорнии (USC) уже не первый год работают

Два рычага (показаны зелёным и красным), нажимая которые животное получало вознаграждение, позволили учёным записать, как работает гиппокамп в процессе обучения грызуна.
В первой части эксперимента исследователи показали, что крыс можно научить нажимать левый либо правый рычаг для получения вознаграждения. Учёные вживили в мозг животных электроды, которые записывали взаимодействие участков гиппокампа, условно называемых CA3 и CA1.
Животное запоминает, какое действие приносит ожидаемый результат, благодаря взаимодействию этих отделов. В процессе обучения мозг трансформирует кратковременные воспоминания в долговременную память. Однако стоит медикаментозными способами отключить гиппокамп, как эта связь пропадает.
У натренированных крыс остаётся только кратковременная память. Дальнейшие опыты показали, что новую информацию они запомнить не в состоянии. «Они по-прежнему знали, что надо нажимать на рычаги, но о том, какой из них уже был нажат, они помнили лишь 5—10 секунд», — рассказывает профессор Бергер.
Затем по модели, записанной электродами, учёные создали электронный протез гиппокампа, копирующий взаимодействие CA3 и CA1. Вторая часть эксперимента показала, что когда грызунам внедрили устройство, в их мозге снова начала формироваться долговременная память.
Дополнительные исследования принесли ещё более поразительный результат: способности крыс с нормально работающим гиппокампом возрастали, когда в их мозг встраивали чип.
Профессор Теодор Бергер
Иллюстрация к опыту
Слайд 26BLUE BRAIN & Human brain project
2005: завершение работ по созданию первой клеточной
BLUE BRAIN & Human brain project
2005: завершение работ по созданию первой клеточной

Ноябрь 2007: завершение первой фазы, включавшей в себя разработку процесса создания на основе собираемого массива данных модели единичной колонки неокортекса, её валидации и исследования.
2008: первая искусственная колонка неокортекса (10 000 клеток).
Июль 2011: первое мезозамыкание 100 колонок неокортекса (1 000 000 клеток).
2014: планировалось получить полную модель крысиного мозга, данные пока не опубликованы (100 мезозамыканий, 100 000 000 клеток).
2015: учёные из École Polytechnique Fédérale de Lausanne (EPFL) разработали численную модель ранее неизвестной связи между глиальными астроцитами и нейронами. Эта модель описывает энергетический обмен в мозге через нейро-глиальные васкулярные модули (NGV). В настоящий момент эта вторичная сеть интегрируется в Blue Brain.
2023: оценочное время появления первой модели человеческого мозга (эквивалент 1000 мозгов крысы).
Слайд 27альтернативы
альтернативы
Слайд 28Спасибо за внимание!
Спасибо за внимание!

 Тип инфузории (ciliofora)
Тип инфузории (ciliofora) Гормоны
Гормоны Органы нервной системы. Практикум
Органы нервной системы. Практикум Применение ЦОР на уроках биологии и химии
Применение ЦОР на уроках биологии и химии Взаимоотношения в системе паразит-хозяин
Взаимоотношения в системе паразит-хозяин Органы дыхания
Органы дыхания Cирийский хомяк
Cирийский хомяк Методы исследования в биологии
Методы исследования в биологии Паукообразные Крыма
Паукообразные Крыма Значение бактерий в природе и для человека. 5 класс
Значение бактерий в природе и для человека. 5 класс Удивительные открытия
Удивительные открытия Отряд Блохи Aphaniptera
Отряд Блохи Aphaniptera Областная экологическая акция Международный год овощей и фруктов,
Областная экологическая акция Международный год овощей и фруктов, Изменчивость в микробных популяциях
Изменчивость в микробных популяциях Протерозойская эра
Протерозойская эра Рекорды хвойных растений
Рекорды хвойных растений Типы питания живых организмов
Типы питания живых организмов Раздражимость и регуляция организмов
Раздражимость и регуляция организмов Зоология
Зоология Лесное сообщество. Животный и растительный мир
Лесное сообщество. Животный и растительный мир Насекомые
Насекомые Хромосомний аналіз як метод виявлення порушень у структурі каріотипу
Хромосомний аналіз як метод виявлення порушень у структурі каріотипу Звери, встречающиеся в природе твоего региона
Звери, встречающиеся в природе твоего региона Филогенез скелета позвоночных животных
Филогенез скелета позвоночных животных Морфологический обзор млекопитающих
Морфологический обзор млекопитающих Спинно-мозговые нервы
Спинно-мозговые нервы Кислотно-щелочной баланс
Кислотно-щелочной баланс lektsia_6_Genetika_cheloveka_1
lektsia_6_Genetika_cheloveka_1