Содержание
- 2. Сера. Характеристика химического элемента и простого вещества
- 3. Закрепим умения 1.характеризовать: - элементы по ПС -Состав атома -строение атома -окислительно-восстановительные свойства 2.Составлять ОВР с
- 4. Узнаем: -аллотропные модификации серы -нахождение серы в природе -физические свойства серы -химические свойства -применение серы
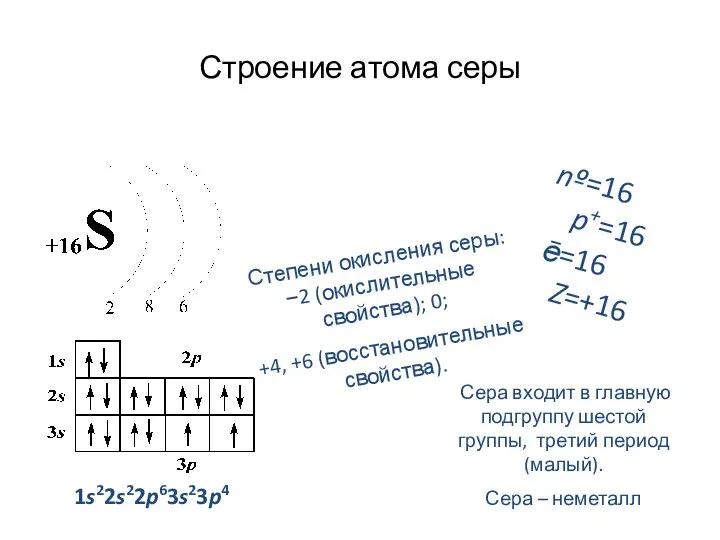
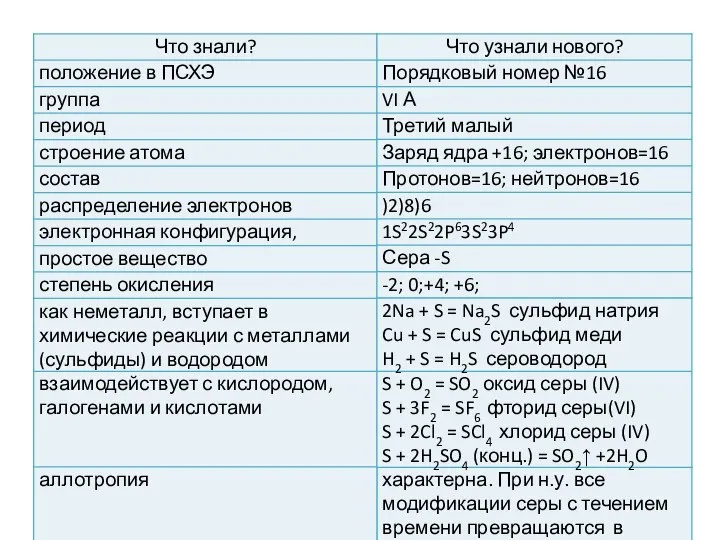
- 5. Строение атома серы 1s22s22p63s23p4 nº=16 p+=16 ē=16 Z=+16 Сера входит в главную подгруппу шестой группы, третий
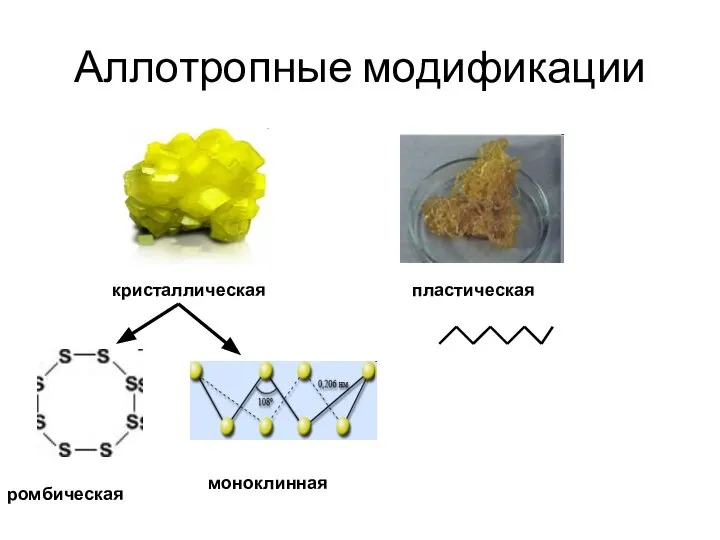
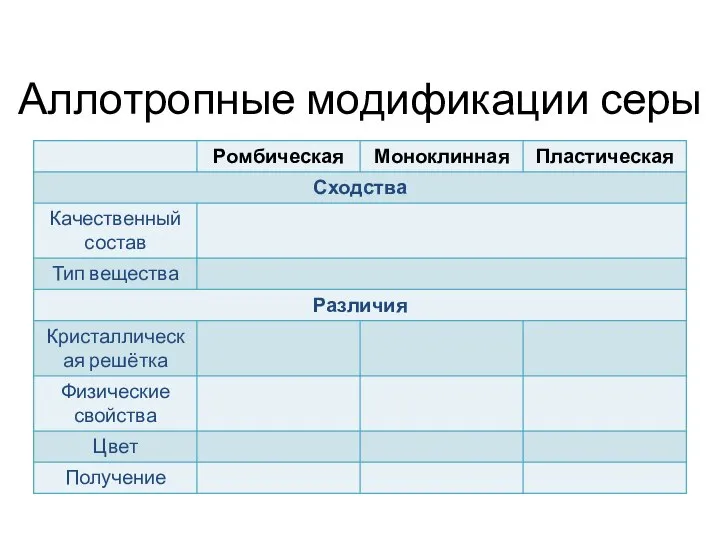
- 6. Аллотропные модификации кристаллическая пластическая ромбическая моноклинная
- 7. Кристаллическая, пластическая и моноклинная сера
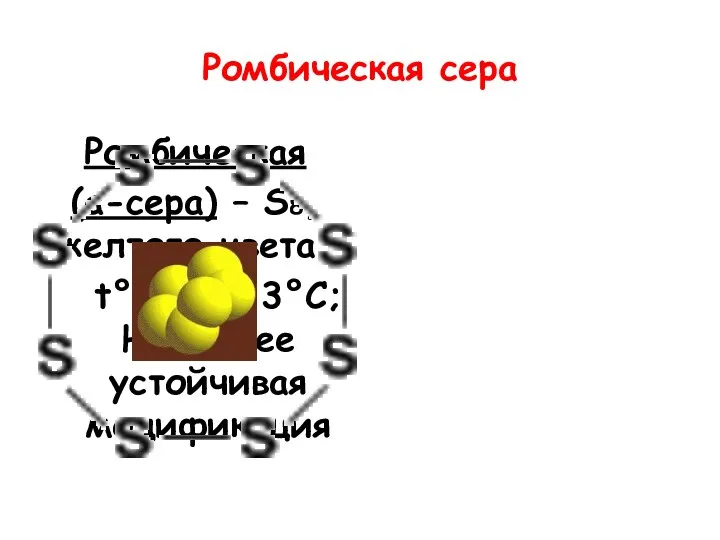
- 8. Ромбическая сера Ромбическая (α-сера) – S8, желтого цвета, t°пл.=113°C; Наиболее устойчивая модификация
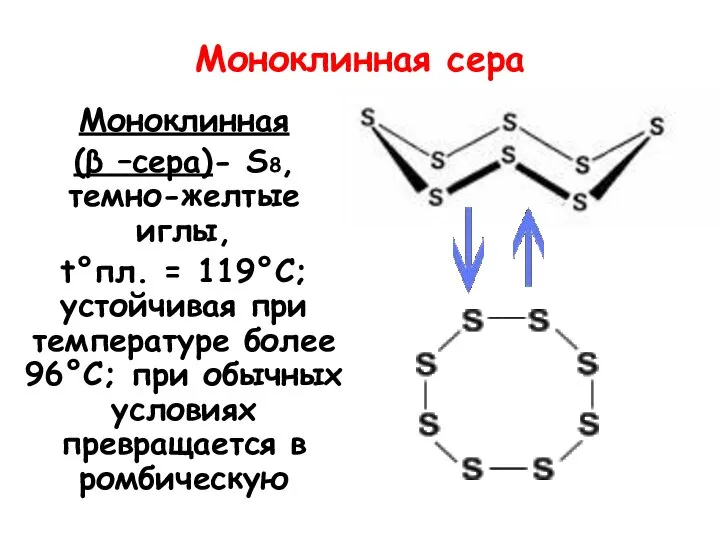
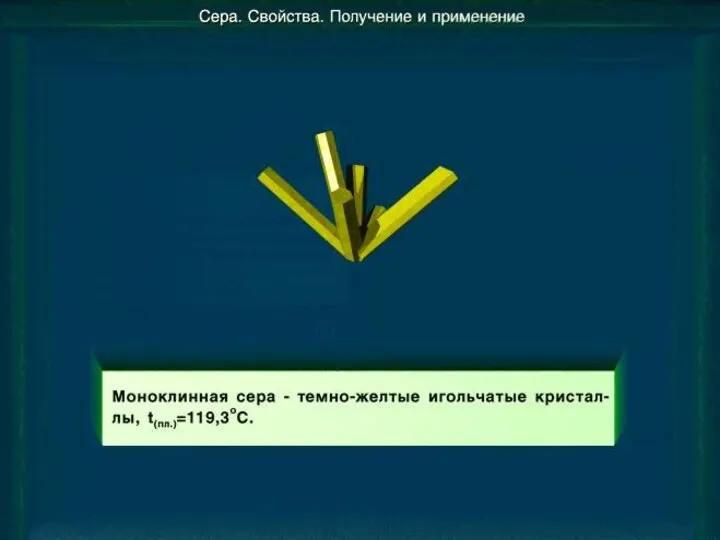
- 10. Моноклинная сера Моноклинная (β –сера)- S8, темно-желтые иглы, t°пл. = 119°C; устойчивая при температуре более 96°С;
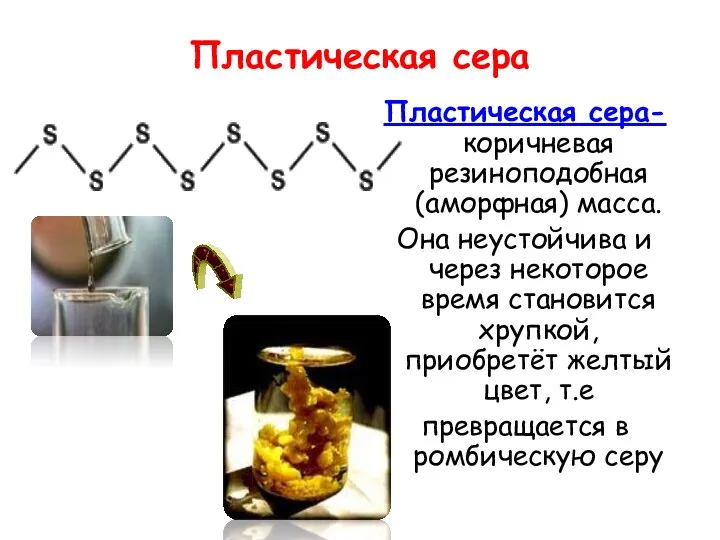
- 12. Пластическая сера Пластическая сера- коричневая резиноподобная (аморфная) масса. Она неустойчива и через некоторое время становится хрупкой,
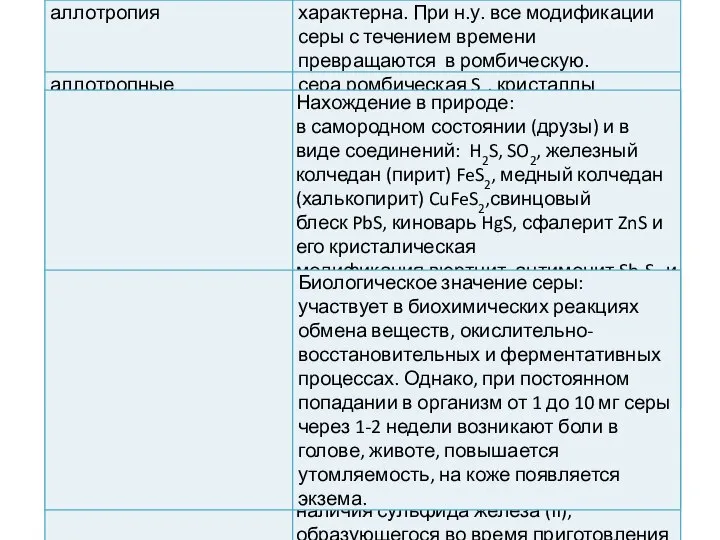
- 14. Нахождение серы в природе Сера является на 16-м месте по распространённости в земной коре. Встречается в
- 15. Сера в природе Самородная Сульфидная: Сероводород H2S Цинковая обманка ZnS Киноварь HgS Свинцовый блеск PbS Пирит
- 16. Сера также встречается в виде сульфатов - солей серной кислоты - мирабилит
- 17. Пирит – «огненный камень» (соединение серы в природе)
- 18. Сера входит в состав белков. Особенно много серы в белках волос, рогов, шерсти. Кроме этого сера
- 19. Серой богаты бобовые растения (горох, чечевица), овсяные хлопья, яйца
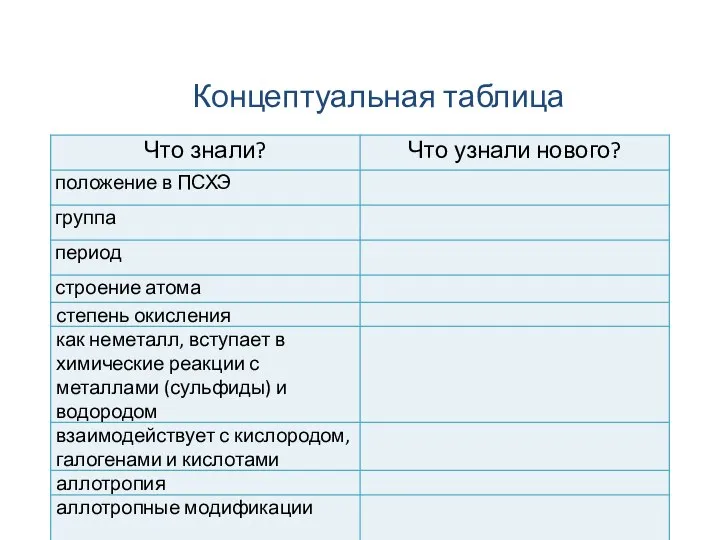
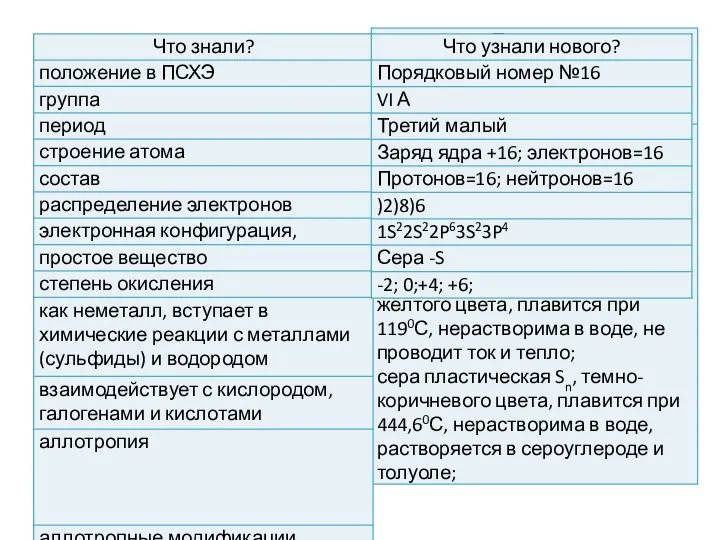
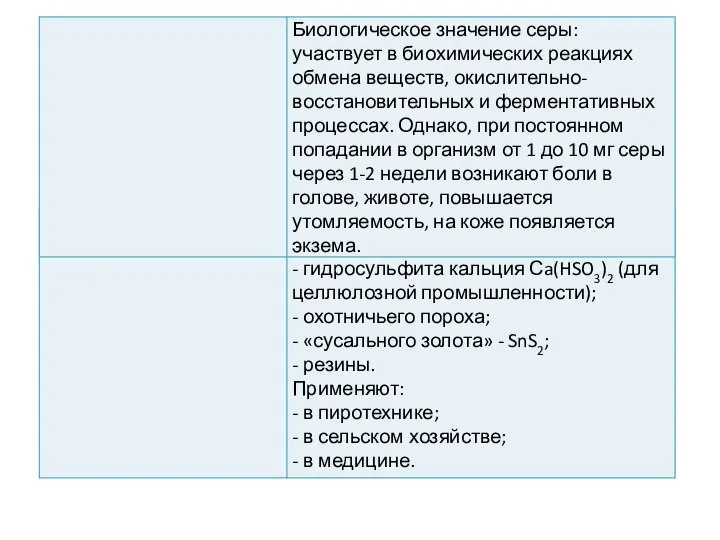
- 20. Концептуальная таблица
- 22. Аллотропные модификации серы
- 23. Сера Химические свойства
- 24. Примеры химических реакций S + O2 = SO2 Zn + S = ZnS 2Na + S
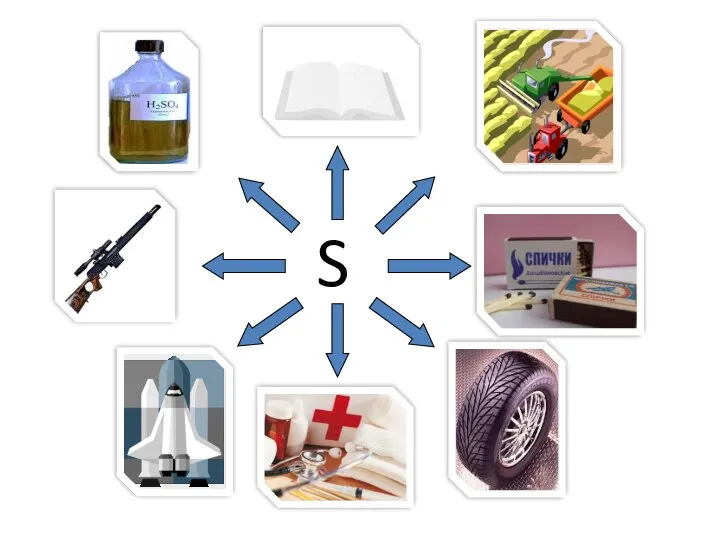
- 27. Сера Применение
- 28. S
- 30. Что вам на уроке удалось лучше всего? Что вам понравилось на уроке? С каким настроением заканчиваете
- 32. Скачать презентацию
















 Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Магний и кальций
Магний и кальций Свойства белков
Свойства белков Жидкая углекислота
Жидкая углекислота Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Нитробактерии. Нитратное дыхание
Нитробактерии. Нитратное дыхание Про краски
Про краски Вероятность протекания химических реакций
Вероятность протекания химических реакций Природные источники углеводородов
Природные источники углеводородов Типы загрязнений биосферы
Типы загрязнений биосферы Степень окисления
Степень окисления Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Силикатная промышленность
Силикатная промышленность Аллотропия Аллотропные видоизменения (модификации)
Аллотропия Аллотропные видоизменения (модификации) Кислоты в химии
Кислоты в химии Состав и строение атома. Изотопы
Состав и строение атома. Изотопы Количество вещества. Моль
Количество вещества. Моль Методи визначення корозійної стійкості матеріалів (тема 11)
Методи визначення корозійної стійкості матеріалів (тема 11) Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка
Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка Характеристика элемента по Периодической системе Д.И. Менделеева
Характеристика элемента по Периодической системе Д.И. Менделеева Презентация на тему Химический состав клетки: ультрамикроэлементы
Презентация на тему Химический состав клетки: ультрамикроэлементы  Получение серной кислоты
Получение серной кислоты Искусство фотографии и химия
Искусство фотографии и химия Предмет органической химии
Предмет органической химии Химия и география. Викторина
Химия и география. Викторина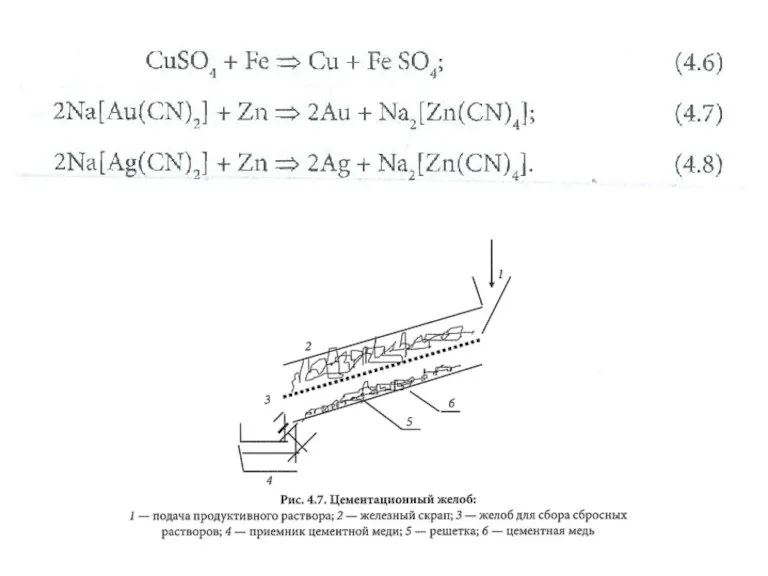 Гальванохимическая очистка. Сорбция
Гальванохимическая очистка. Сорбция