Содержание
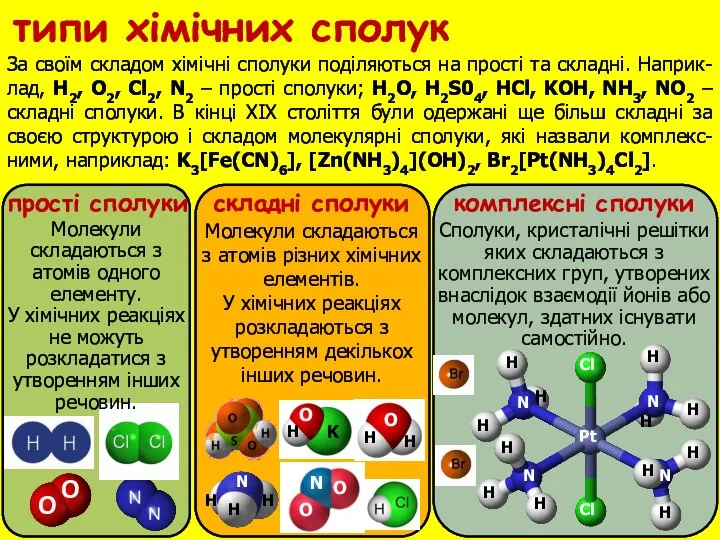
- 2. прості сполуки складні сполуки комплекснi сполуки типи хiмiчних сполук За своїм складом хімічні сполуки поділяються на
- 3. Альфред Вернер Головною ознакою комплексних сполук є координація, тому їх називають координаційними. У 1893 році швейцарський
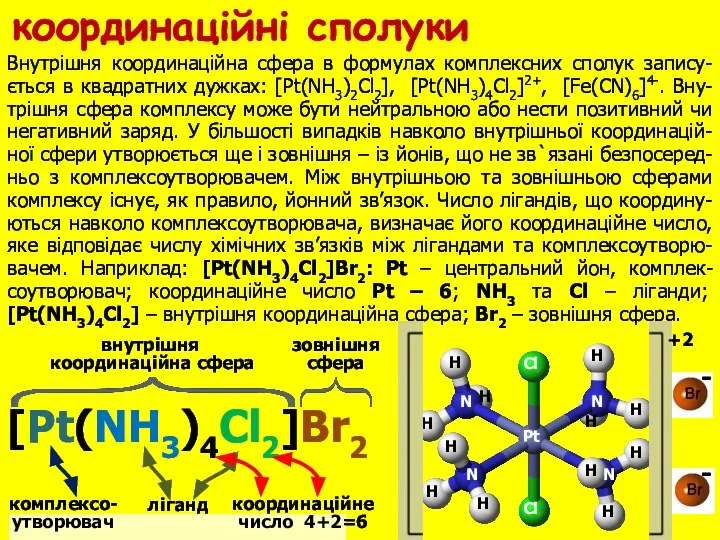
- 4. координаційне число 4+2=6 зовнішня сфера комплексо- утворювач ліганд Внутрішня координаційна сфера в формулах комплексних сполук запису-ється
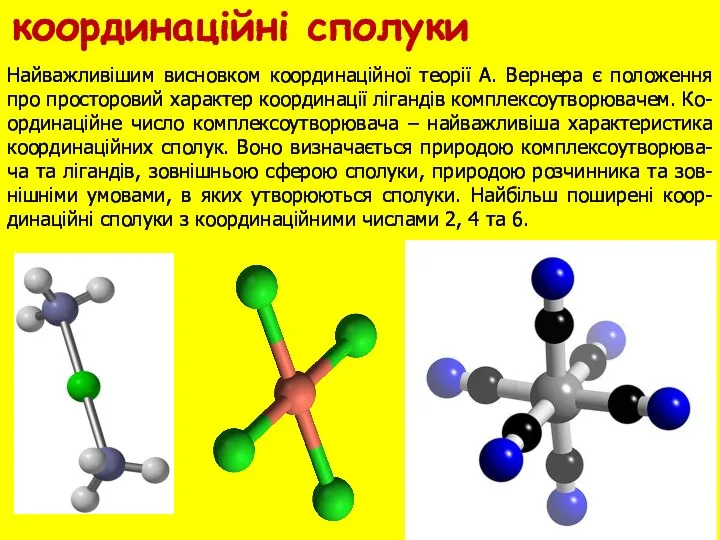
- 5. Найважливішим висновком координаційної теорії А. Вернера є положення про просторовий характер координації лігандів комплексоутворювачем. Ко-ординаційне число
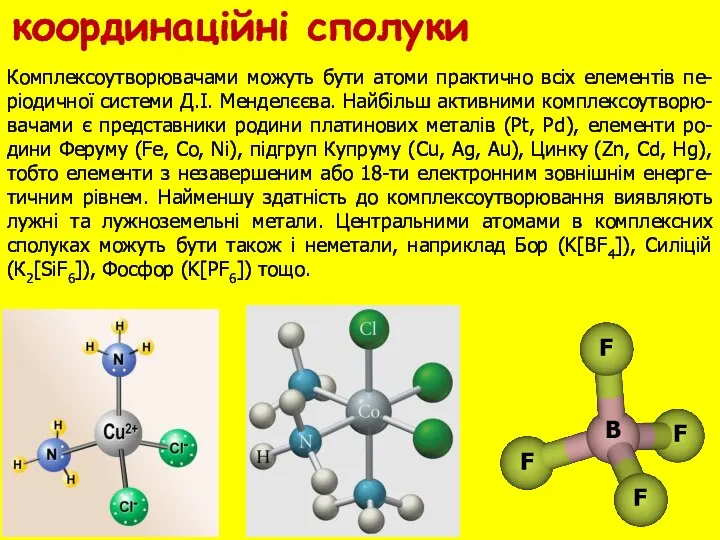
- 6. Комплексоутворювачами можуть бути атоми практично всіх елементів пе-ріодичної системи Д.І. Менделєєва. Найбільш активними комплексоутворю-вачами є представники
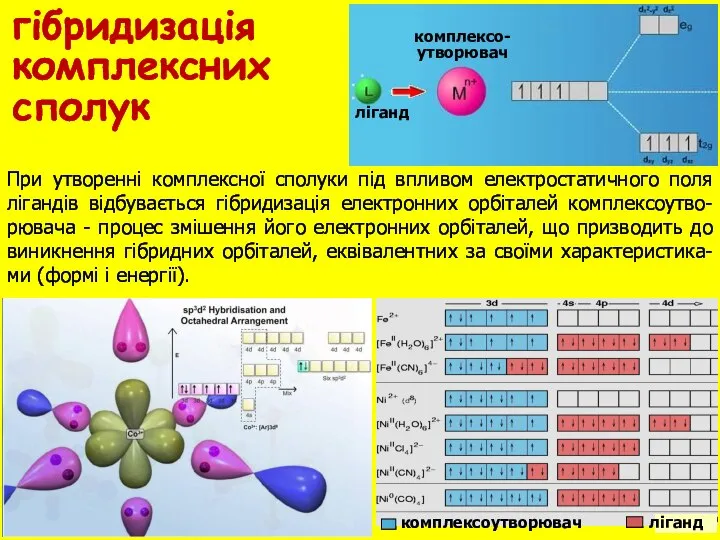
- 7. комплексоутворювач ліганд гібридизація комплексних сполук комплексо- утворювач ліганд При утворенні комплексної сполуки під впливом електростатичного поля
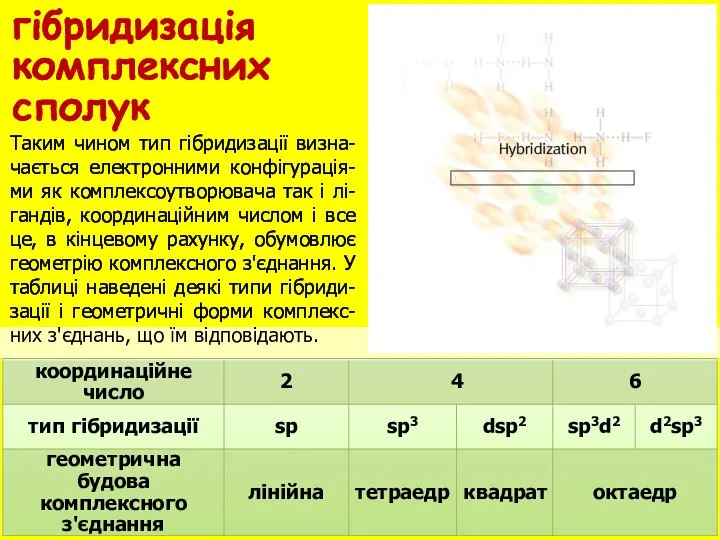
- 8. гібридизація комплексних сполук Таким чином тип гібридизації визна-чається електронними конфігурація-ми як комплексоутворювача так i лi-гандiв, координаційним
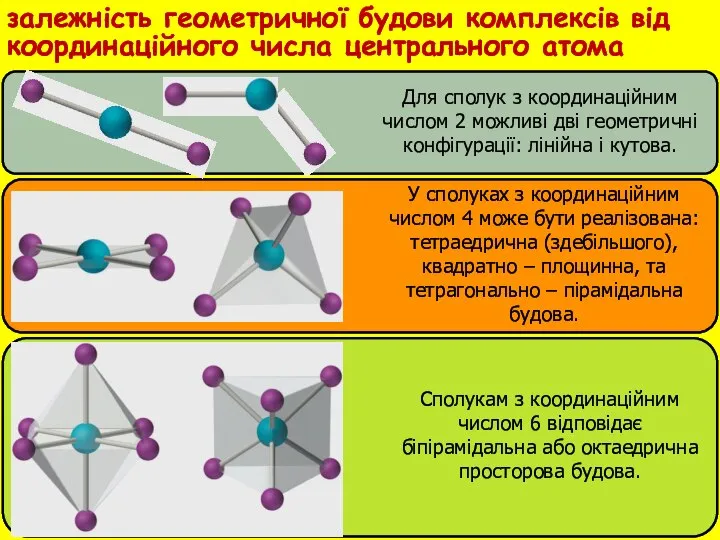
- 9. Для сполук з координаційним числом 2 можливі дві геометричні конфігурації: лінійна і кутова. У сполуках з
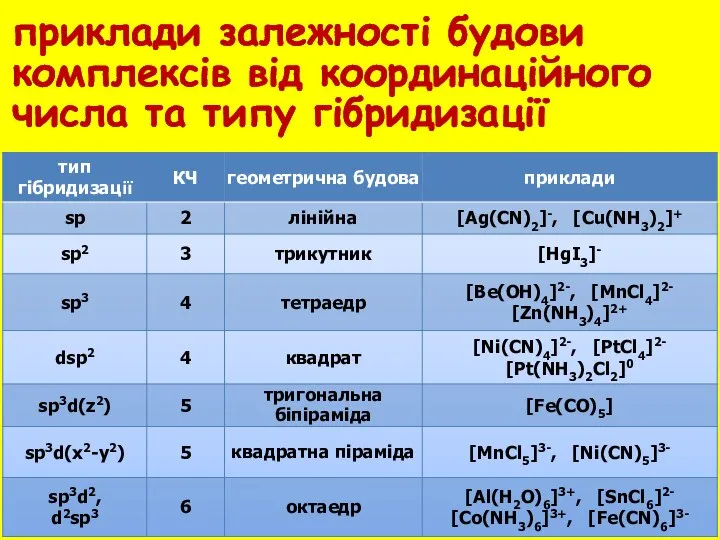
- 10. приклади залежності будови комплексів від координаційного числа та типу гібридизації
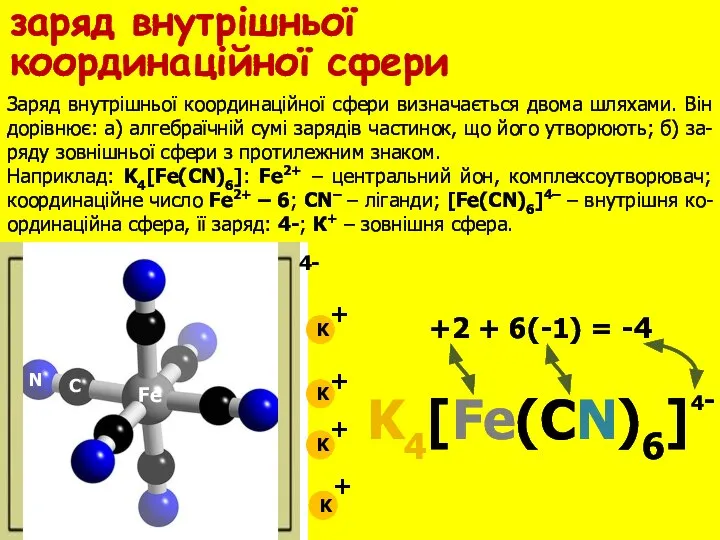
- 11. Заряд внутрішньої координаційної сфери визначається двома шляхами. Він дорівнює: а) алгебраїчній сумі зарядів частинок, що його
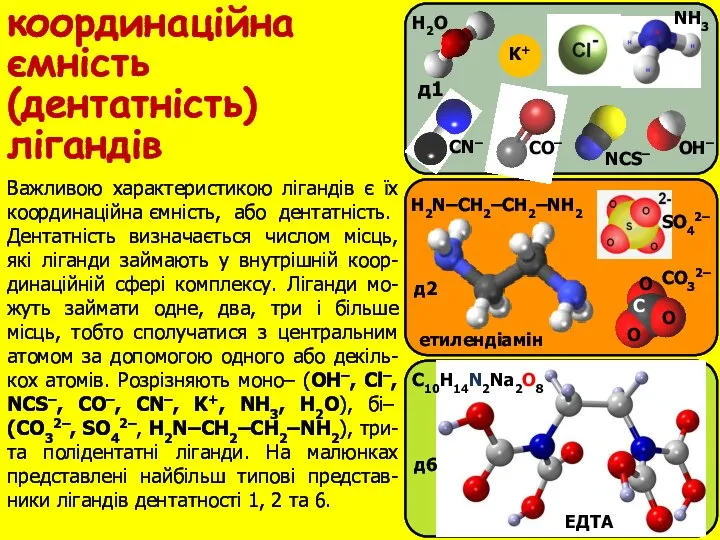
- 12. д1 Важливою характеристикою лігандів є їх координаційна ємність, або дентатність. Дентатність визначається числом місць, які ліганди
- 13. (C55H72N4O5Mg) (Co[C62H88N13O14P])CN (C34H32N4O4Fe) Біоорганічні молекули (білки, гормони, пептиди, нуклеїнові кислоти тощо) є полідентатними лігандами, які разом
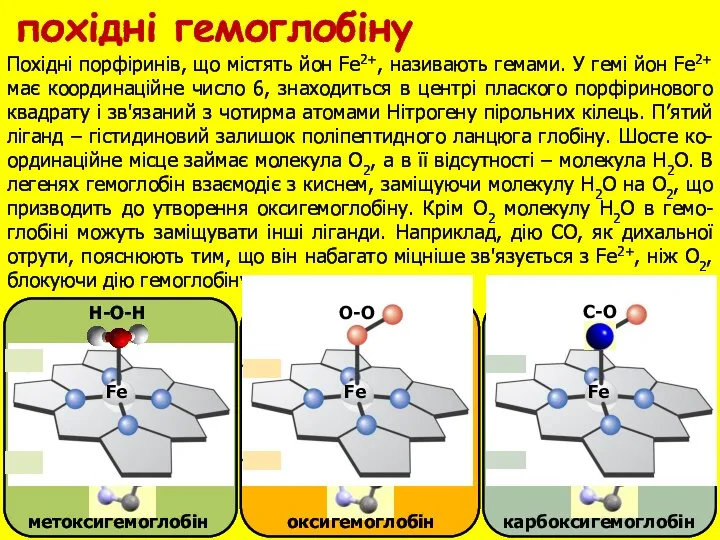
- 14. Похідні порфіринів, що містять йон Fe2+, називають гемами. У гемі йон Fe2+ має координаційне число 6,
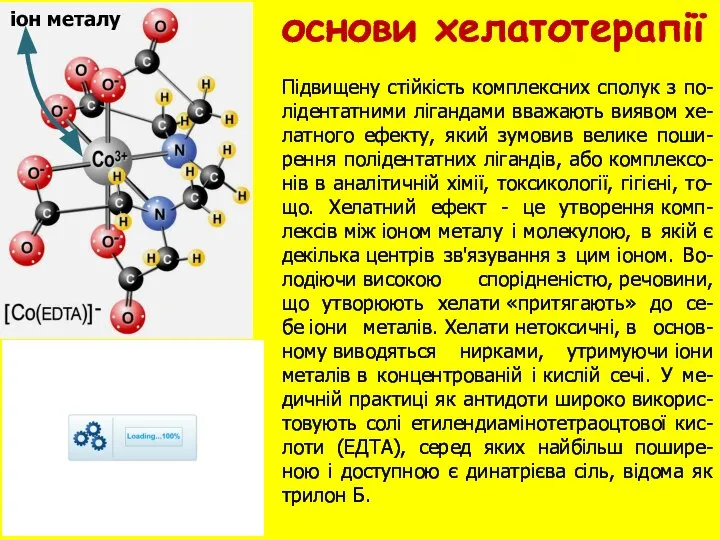
- 15. Підвищену стійкість комплексних сполук з по-лідентатними лігандами вважають виявом хе-латного ефекту, який зумовив велике поши-рення полідентатних
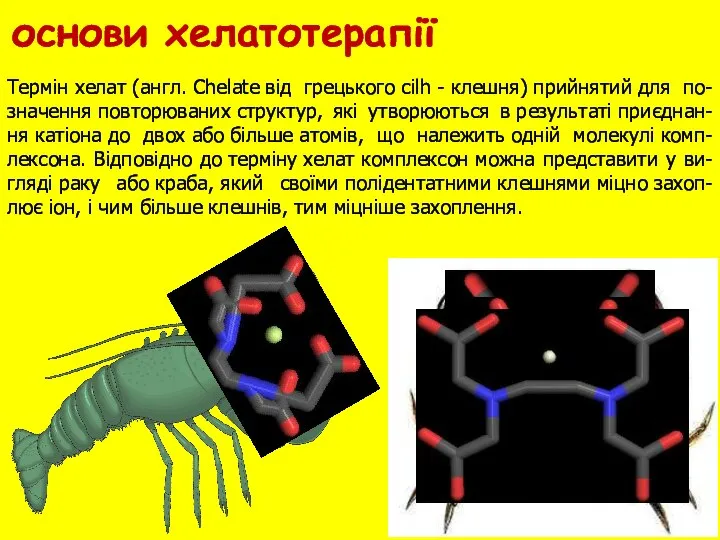
- 16. Термін хелат (англ. Chelate від грецького cilh - клешня) прийнятий для по-значення повторюваних структур, які утворюються
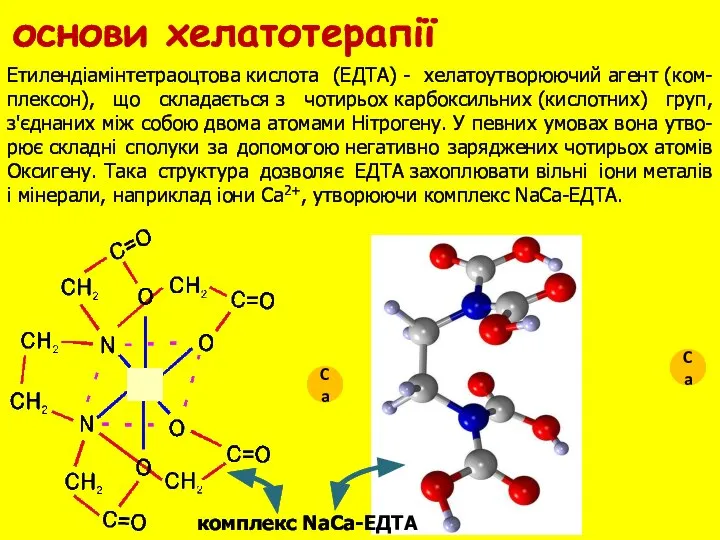
- 17. Етилендіамінтетраоцтова кислота (ЕДТА) - хелатоутворюючий агент (ком-плексон), що складається з чотирьох карбоксильних (кислотних) груп, з'єднаних між
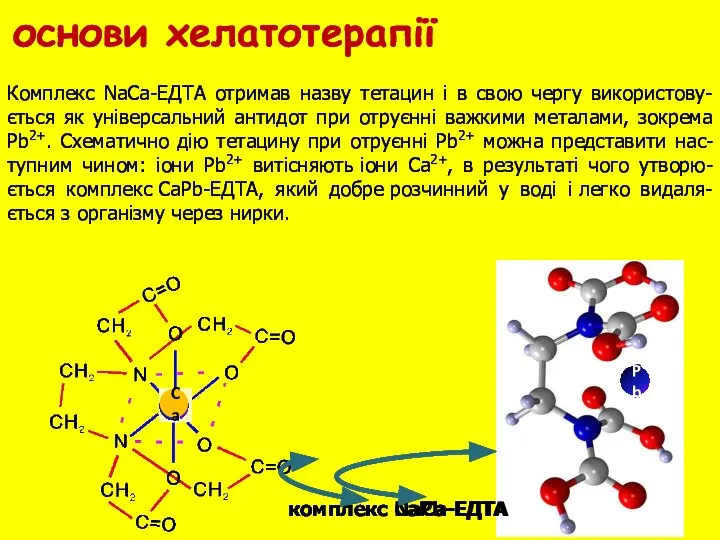
- 18. Pb Ca Комплекс NaCa-ЕДТА отримав назву тетацин i в свою чергу використову-ється як унiверсальний антидот при
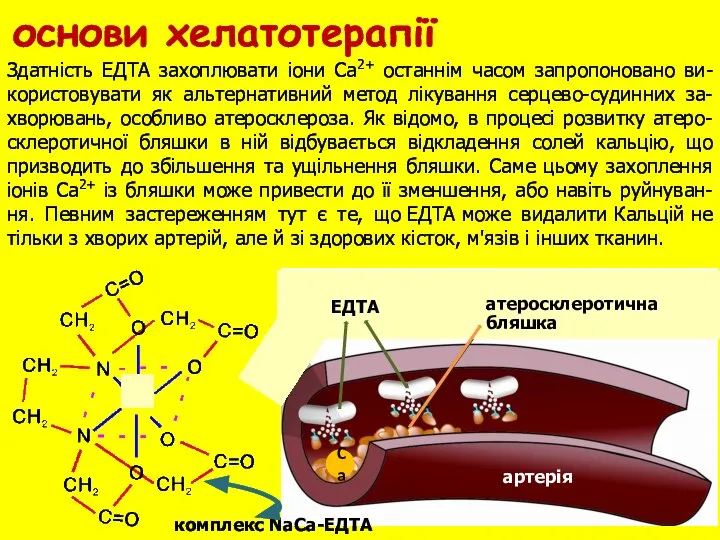
- 19. Ca атеросклеротична бляшка ЕДТА артерiя Здатнiсть ЕДТА захоплювати iони Са2+ останнiм часом запропоновано ви-користовувати як альтернативний
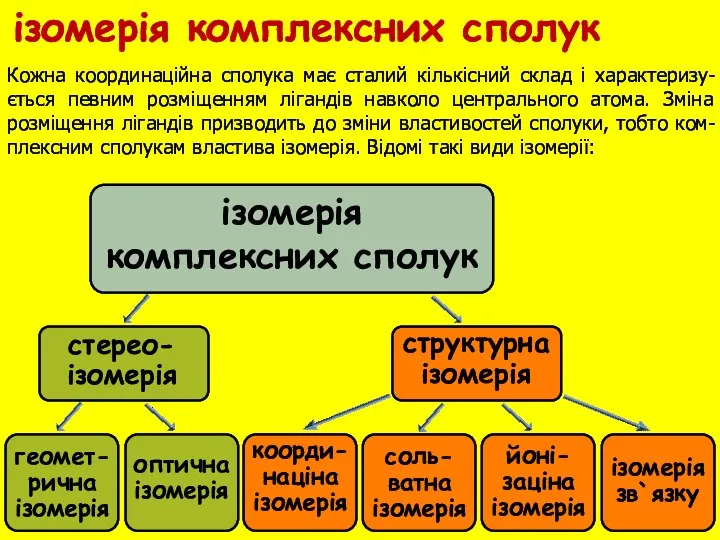
- 20. ізомерія комплексних сполук стерео- ізомерія структурна ізомерія Кожна координаційна сполука має сталий кількісний склад і характеризу-ється
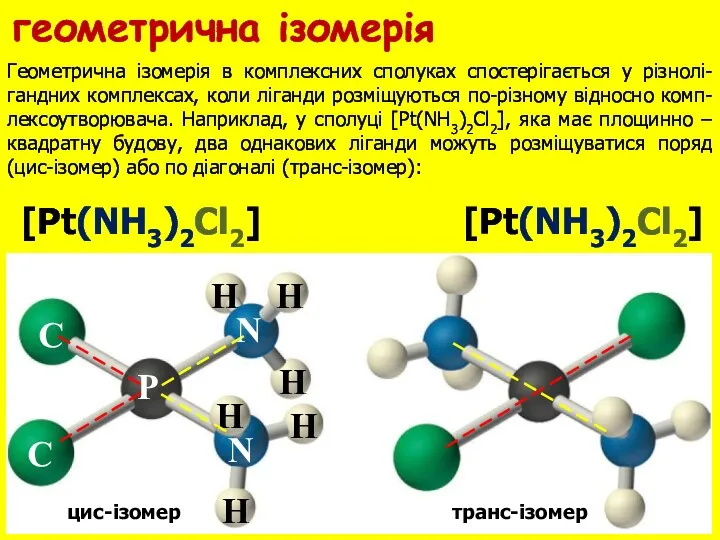
- 21. Геометрична ізомерія в комплексних сполуках спостерігається у різнолі-гандних комплексах, коли ліганди розміщуються по-різному відносно комп-лексоутворювача. Наприклад,
- 22. mer-ізомер fac-ізомер Схожа ізомерія характерна і для комплексів складу [Pt(NH3)3Cl3], але тут вживається інше маркування: конфігурація
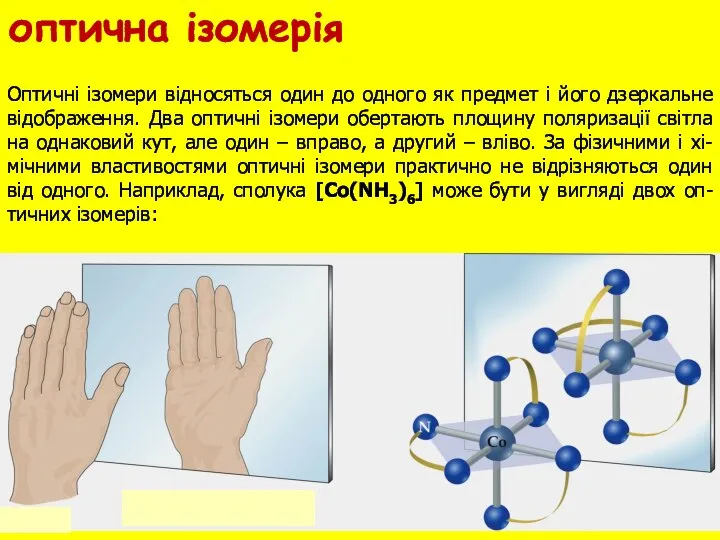
- 23. Оптичні ізомери відносяться один до одного як предмет і його дзеркальне відображення. Два оптичні ізомери обертають
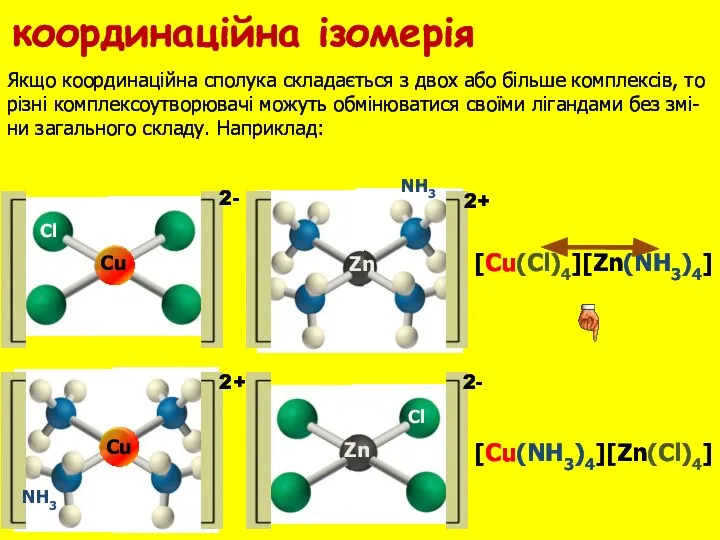
- 24. Zn Cu Cu Zn Якщо координаційна сполука складається з двох або більше комплексів, то різні комплексоутворювачі
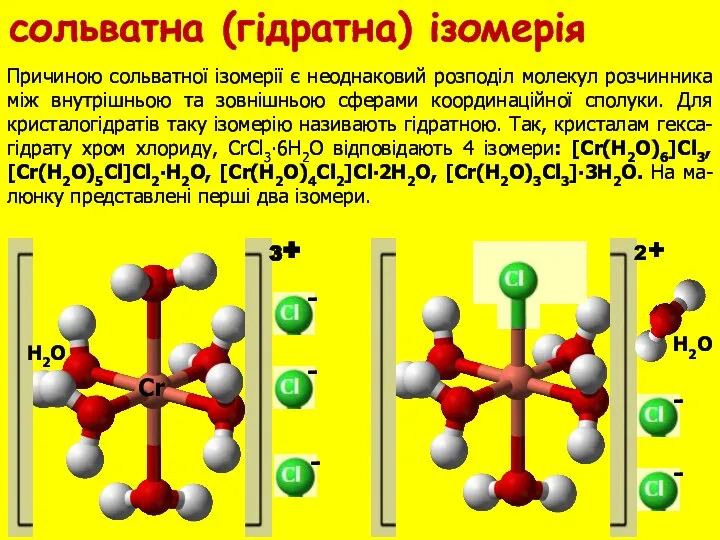
- 25. Причиною сольватної ізомерії є неоднаковий розподіл молекул розчинника між внутрішньою та зовнішньою сферами координаційної сполуки. Для
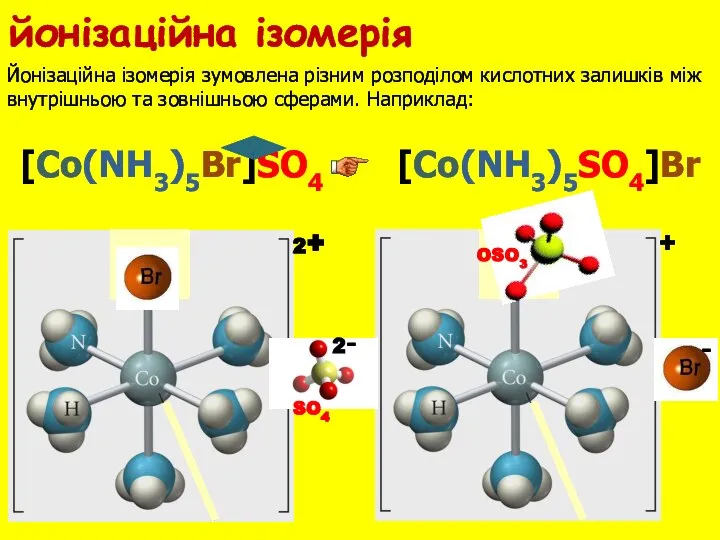
- 26. Йонізаційна ізомерія зумовлена різним розподілом кислотних залишків між внутрішньою та зовнішньою сферами. Наприклад: [Co(NH3)5Br]SO4 [Co(NH3)5SO4]Br йонiзацiйна
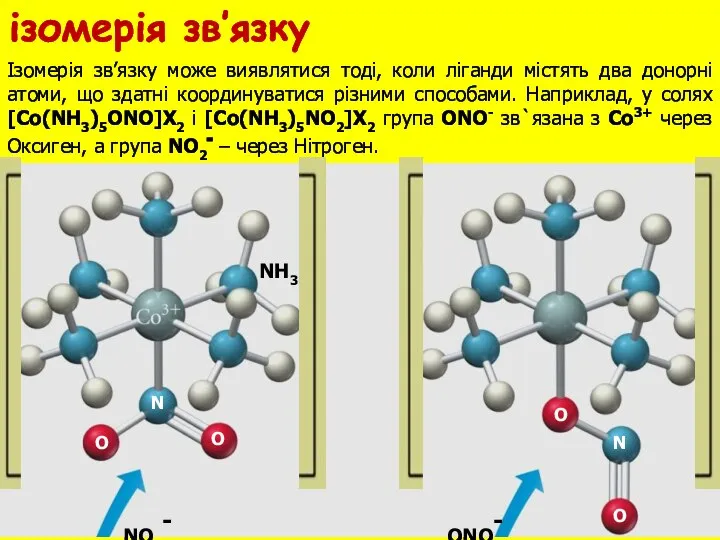
- 27. Ізомерія зв’язку може виявлятися тоді, коли ліганди містять два донорні атоми, що здатні координуватися різними способами.
- 28. У живому організмі d-елементи в біохімічних процесах беруть участь у виг-ляді біокомплексів металів. Лігандами в цих
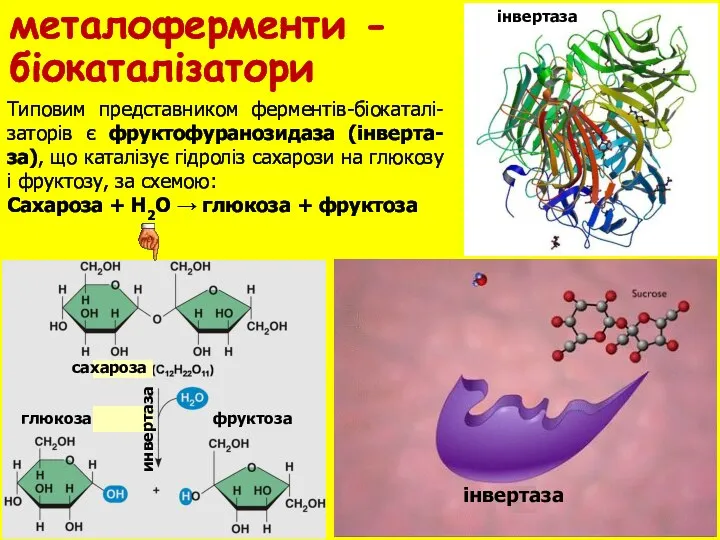
- 29. металоферменти - біокаталізатори инвертаза сахароза глюкоза фруктоза iнвертаза Типовим представником ферментiв-бiокаталi-заторiв є фруктофуранозидаза (інверта-за), що каталізує
- 30. Карбоангідраза - каталізує зворотну гідратацію карбон (IV) оксиду: CO2 + H2O H2CO3 H+ + HCO Карбоксипепсидаза
- 32. Скачать презентацию

![(C55H72N4O5Mg) (Co[C62H88N13O14P])CN (C34H32N4O4Fe) Біоорганічні молекули (білки, гормони, пептиди, нуклеїнові кислоти тощо) є](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1021480/slide-12.jpg)
![mer-ізомер fac-ізомер Схожа ізомерія характерна і для комплексів складу [Pt(NH3)3Cl3], але тут](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1021480/slide-21.jpg)


 Оплодотворение и его значение. 9 класс
Оплодотворение и его значение. 9 класс Концепции биологии. Строение живого
Концепции биологии. Строение живого Тренировочный тест. Пресмыкающиеся
Тренировочный тест. Пресмыкающиеся Правильное питание - залог здоровья. Голод - геоэкологическая проблема
Правильное питание - залог здоровья. Голод - геоэкологическая проблема Кокетльові господарочки
Кокетльові господарочки Нерпа. 6 класс
Нерпа. 6 класс Вирусы (1)
Вирусы (1) Основы систематики позвоночных
Основы систематики позвоночных 1 апреля - День птиц
1 апреля - День птиц Методики применения средств физической культуры для направленной коррекции телосложения
Методики применения средств физической культуры для направленной коррекции телосложения Паукообразные. Паук бабуин
Паукообразные. Паук бабуин Анатомо - морфологические особенности и основные физиологические функции организма
Анатомо - морфологические особенности и основные физиологические функции организма Përshtatjet e bimëve
Përshtatjet e bimëve Неполное доминирование. Анализирующее скрещивание
Неполное доминирование. Анализирующее скрещивание Питание грибов
Питание грибов 07. Обеспечение клеток энергией
07. Обеспечение клеток энергией эволюция пищеварения животных
эволюция пищеварения животных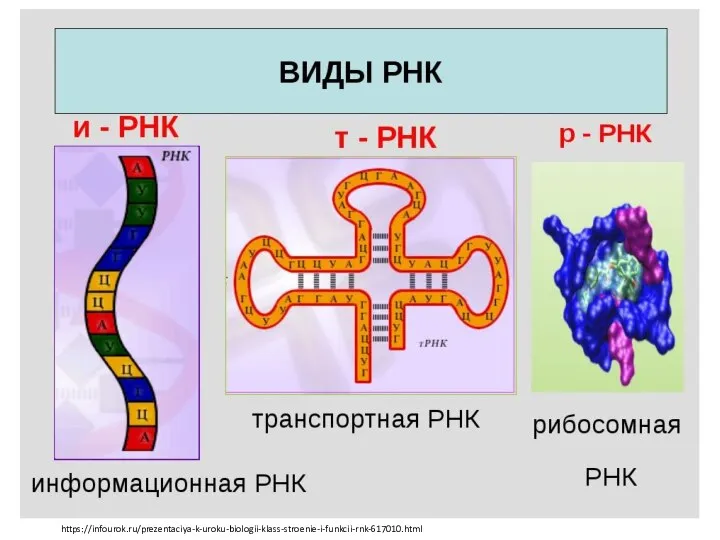 ДНК и РНК
ДНК и РНК Корреляция структуры ксенобиотика и его токсичности. Топологические индексы
Корреляция структуры ксенобиотика и его токсичности. Топологические индексы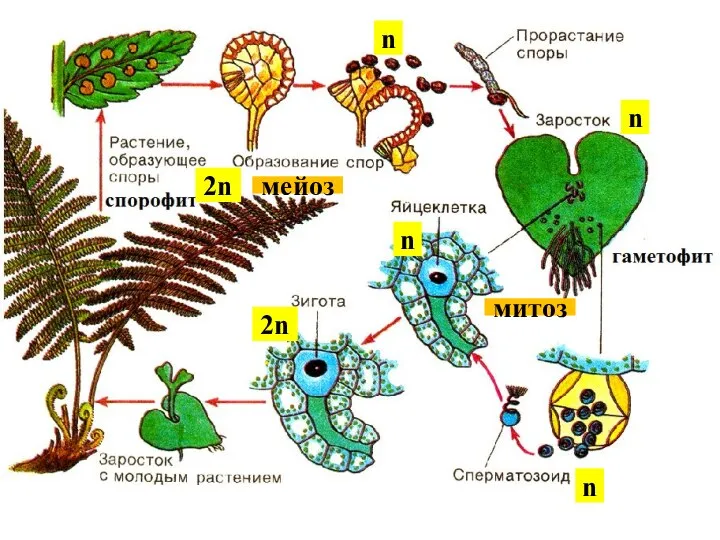 Жизненные циклы растений
Жизненные циклы растений Презентация на тему Удобрения
Презентация на тему Удобрения  Журавль - птица 2020 года
Журавль - птица 2020 года Знатоки естественных наук. Игра-путешествие
Знатоки естественных наук. Игра-путешествие Системы органов в организме. Уровни организации организма
Системы органов в организме. Уровни организации организма Биотехнологии. Биоинженерия
Биотехнологии. Биоинженерия Адаптация рецепторов
Адаптация рецепторов Презентация на тему Лекарственные растения
Презентация на тему Лекарственные растения  Конкуренция непосредственно взаимодействия
Конкуренция непосредственно взаимодействия