Содержание
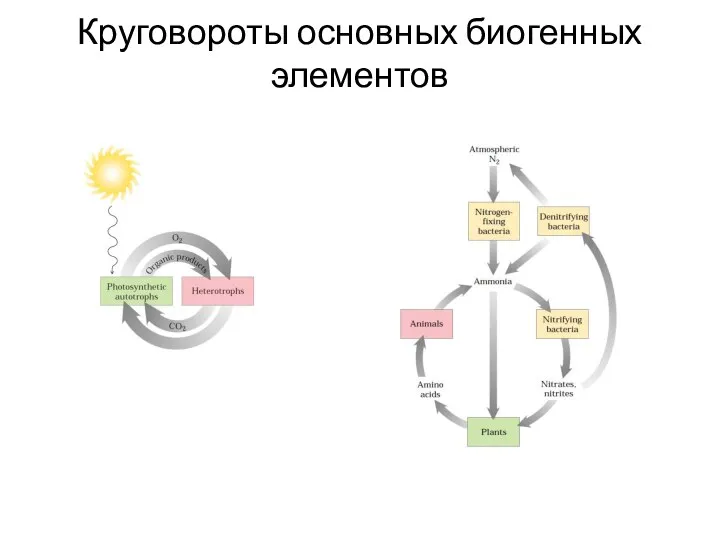
- 2. Круговороты основных биогенных элементов
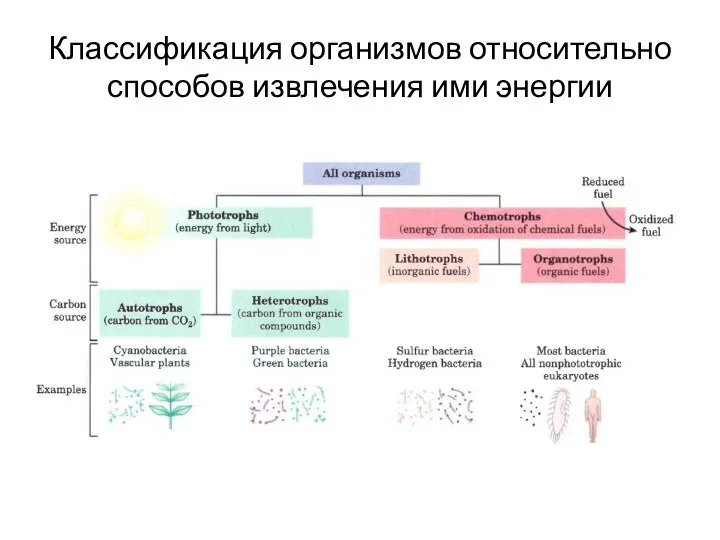
- 3. Классификация организмов относительно способов извлечения ими энергии
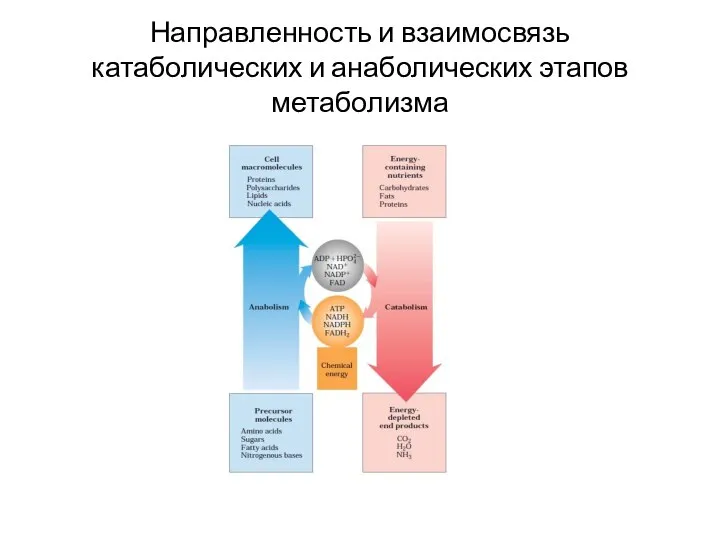
- 4. Направленность и взаимосвязь катаболических и анаболических этапов метаболизма
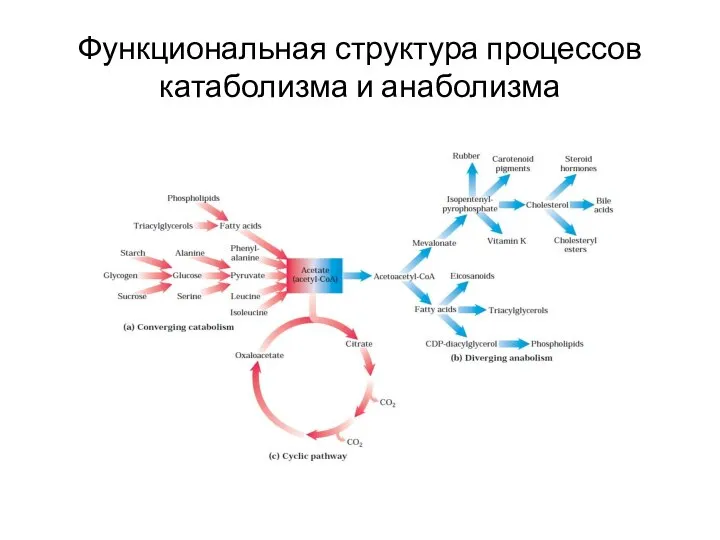
- 5. Функциональная структура процессов катаболизма и анаболизма
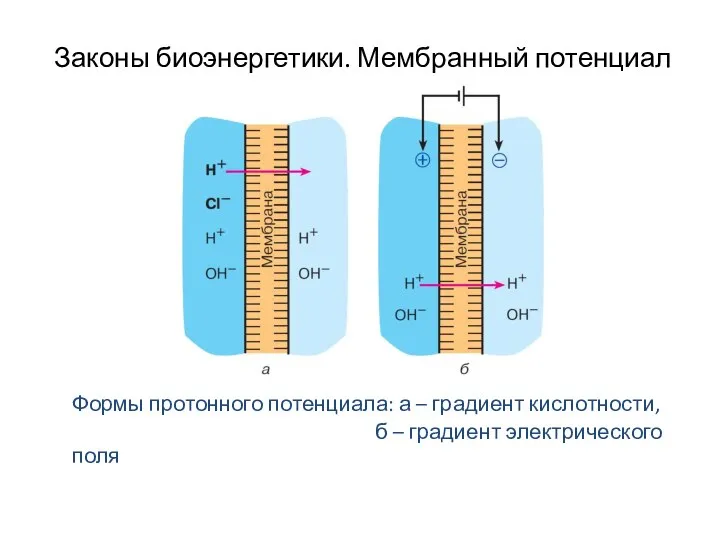
- 6. Законы биоэнергетики. Мембранный потенциал Формы протонного потенциала: а – градиент кислотности, б – градиент электрического поля
- 7. Законы биоэнергетики. Мембранный потенциал
- 8. Законы биоэнергетики. Первый закон
- 9. Законы биоэнергетики. Второй закон Клетка всегда имеет как минимум две формы энергии: макроэргические связи АТФ энергию,
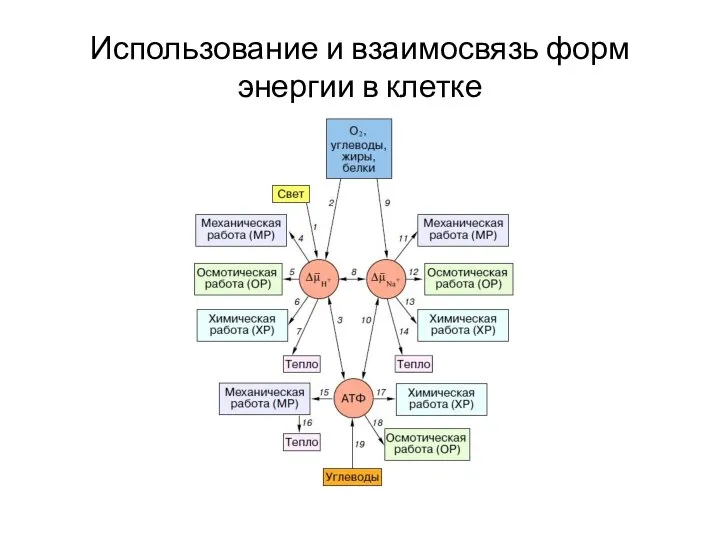
- 10. Использование и взаимосвязь форм энергии в клетке
- 11. Законы биоэнергетики. Третий закон Энергетические формы могут превращаться одна в другую Na+-АТФ-синтаза : АТФ ↔Δ μNa+,
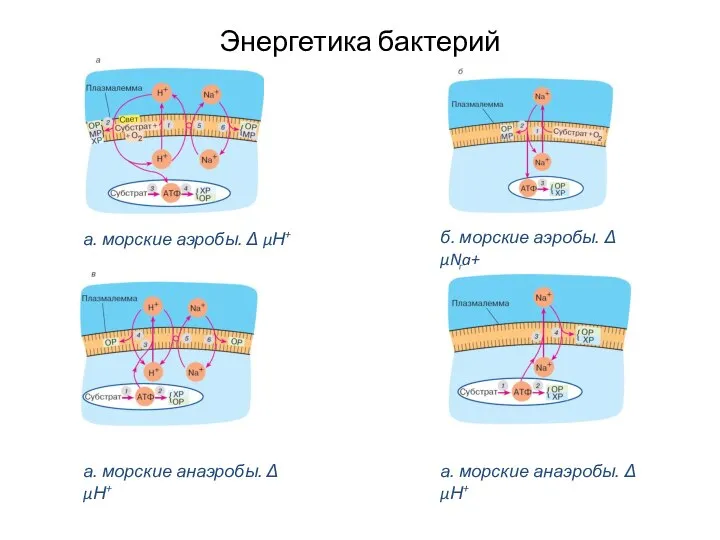
- 12. Энергетика бактерий а. морские аэробы. Δ μН+ б. морские аэробы. Δ μNa+ а. морские анаэробы. Δ
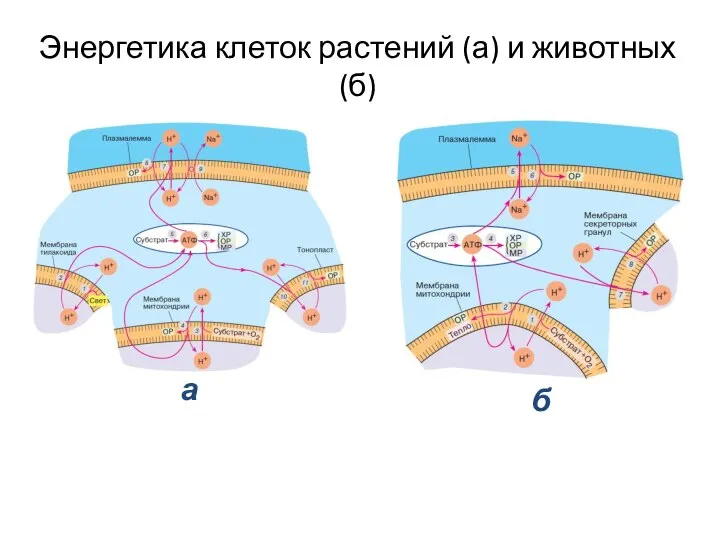
- 13. Энергетика клеток растений (а) и животных (б) а б
- 14. Основы термодинамики Энергия (от гр. energeia - деятельность) - одно из основных свойств материи, мера её
- 15. Основы термодинамики Работа - упорядоченная форма передачи энергии, связанная с преодолением внешнего сопротивления Теплота - неупорядоченная
- 16. Основы термодинамики Система - это тело или совокупность тел, выделенных из пространства Среда - всё, что
- 17. Виды системы в зависимости от фаз Гомогенные системы - состоят из одной фазы (физиологический раствор, плазма
- 18. Типы систем в зависимости от связи со средой Открытые Закрытые Изолированные
- 19. Основы термодинамики Состояние системы - совокупность условий существования и состава системы
- 21. Типы термодинамических систем
- 22. Термодинамика. Первый закон Общее количество энергии (U) замкнутой системы сохраняется постоянным U = const или ΔU
- 23. Термодинамика. Первый закон U2 – U1 = ΔU = ΔQ + ΔA ΔQ - теплообмен ΔA
- 24. Термодинамика. Второй закон Процессы, связанные с превращениями энергии, могут происходить самопроизвольно только при условии, что энергия
- 25. Свободная энергия и энтальпия U = F + TS U – внутренняя энергия F – свободная
- 26. Свободная энергия и энтальпия - при постоянном объеме и изменении давления: ΔU = ΔF + T
- 27. Связь энергии и энтальпии ΔH = ΔU + p ΔV; ΔG = ΔF + p ΔV
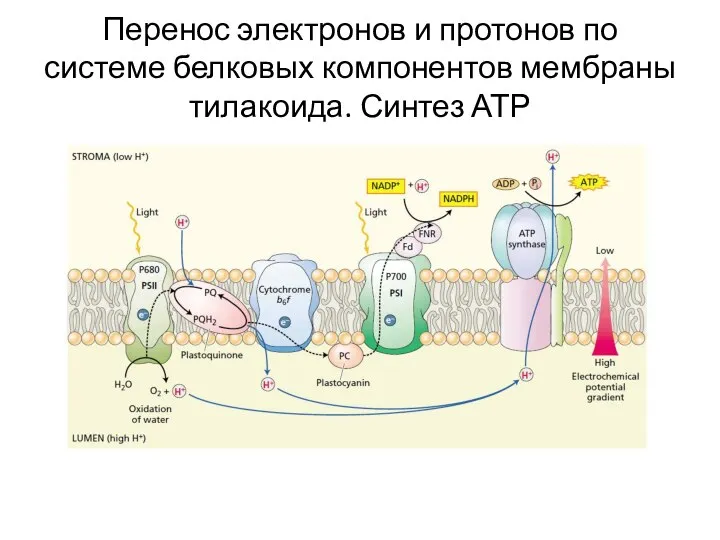
- 28. Перенос электронов и протонов по системе белковых компонентов мембраны тилакоида. Синтез АТР
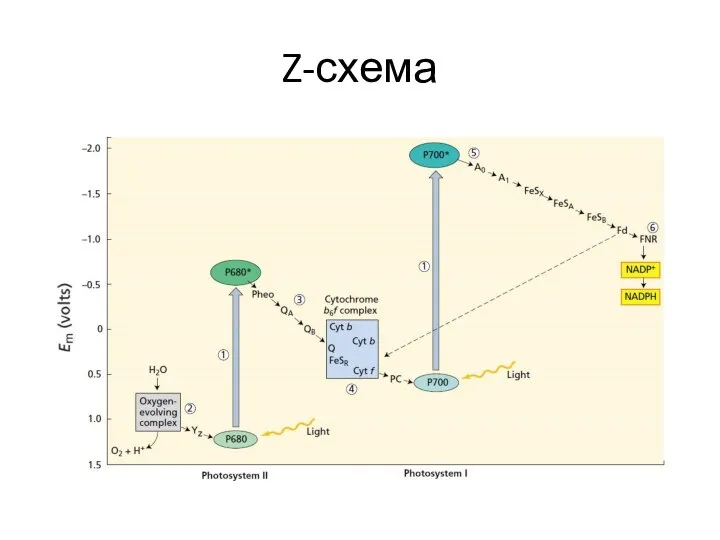
- 29. Z-схема
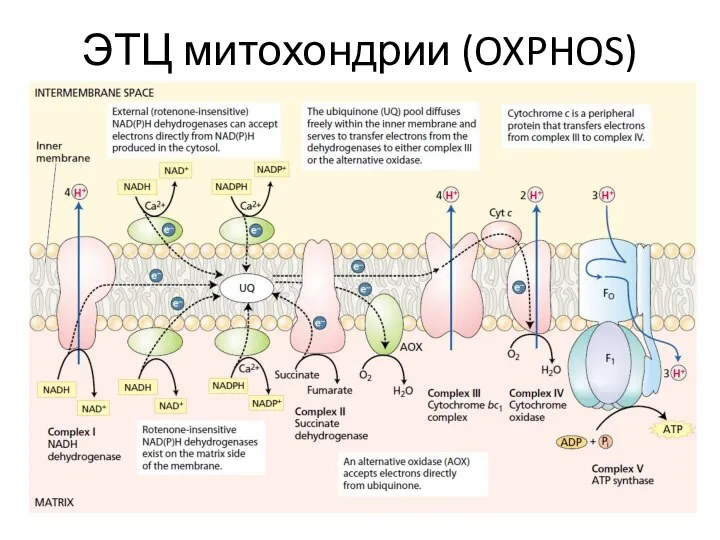
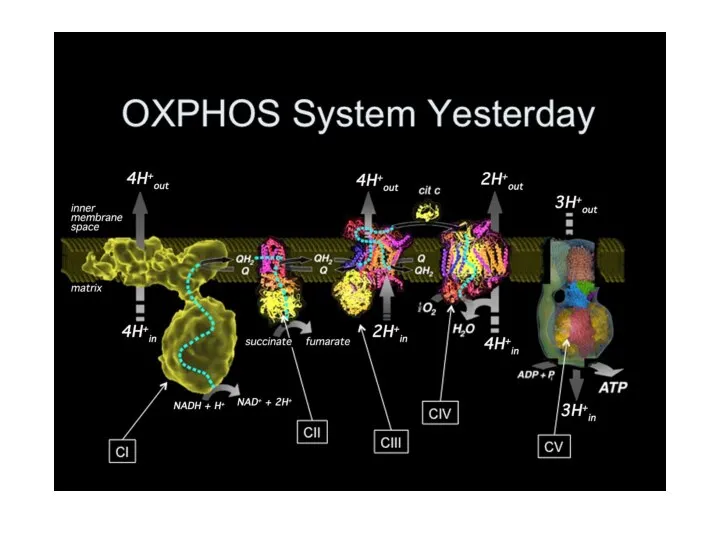
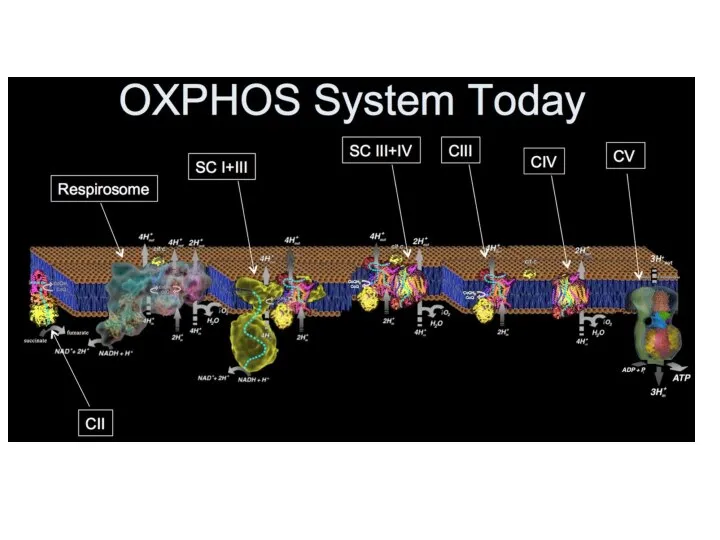
- 30. ЭТЦ митохондрии (OXPHOS)
- 40. Скачать презентацию























 Проводниковый отдел зрительного анализатора. Значение горизонтальных связей в сетчатке
Проводниковый отдел зрительного анализатора. Значение горизонтальных связей в сетчатке Презентация на тему Комменсализм
Презентация на тему Комменсализм  Биоэкологическая характеристика на примере 26 микрорайона г. Челябинска
Биоэкологическая характеристика на примере 26 микрорайона г. Челябинска Стволовые инъекции. История, теория и практика. ООО Евпатор, команда Доктор Лес
Стволовые инъекции. История, теория и практика. ООО Евпатор, команда Доктор Лес Генетика
Генетика Своя игра по биологии
Своя игра по биологии Ребята о зверятах
Ребята о зверятах Йод, Кальций, Витамин А и Витамин К в жизни человека
Йод, Кальций, Витамин А и Витамин К в жизни человека Вегетативные органы растений
Вегетативные органы растений Что такое жизнь?
Что такое жизнь? Влияние физических упражнений на кровеносную, дыхательную и нервную системы
Влияние физических упражнений на кровеносную, дыхательную и нервную системы Терморегуляция организма. Закаливание
Терморегуляция организма. Закаливание Мария Мелентьева
Мария Мелентьева Двудольные. Морфологические особенности
Двудольные. Морфологические особенности Изучение человека. Ученые-анатомы
Изучение человека. Ученые-анатомы Презентация на тему Строение и деятельность внутренних органов земноводных
Презентация на тему Строение и деятельность внутренних органов земноводных  Дыхательная система
Дыхательная система Хордовые. Ланцетник. Внешний вид, размеры, среда обитания
Хордовые. Ланцетник. Внешний вид, размеры, среда обитания Адаптация животных к движению по воздуху
Адаптация животных к движению по воздуху Животные севера
Животные севера Производство микроорганизмов
Производство микроорганизмов Многообразие бактерий
Многообразие бактерий Приспособленность организмов к среде обитания
Приспособленность организмов к среде обитания Нейрогормональная регуляция поведения животных
Нейрогормональная регуляция поведения животных Характеристика царства бактерий. Биология (5 класс)
Характеристика царства бактерий. Биология (5 класс) Тип Кольчатые черви Annellida
Тип Кольчатые черви Annellida Tkáně, základ orgánů
Tkáně, základ orgánů Знакомые незнакомцы. Путешествие с домашними животными
Знакомые незнакомцы. Путешествие с домашними животными