Слайд 2159
ВОПРОСЫ
43. Средняя длина свободного пробега молекул. Эффективный диаметр молекулы. Среднее число соударений

в единицу времени.
44. Явления переноса – диффузия, теплопроводность и вязкость в газах. Коэффициенты диффузии, теплопроводности, вязкости.
Слайд 3159
43. Средняя длина свободного пробега молекул. Эффективный диаметр молекулы. Среднее число соударений

в единицу времени.
Слайд 4159
Микроскопическую теорию процессов, происходящих в неравновесных системах, называют физической кинетикой.
Физическая кинетика

использует представления об
атомно-молекулярном
строении веществ.
Слайд 5159
Она изучает процессы переноса массы вещества, импульса, энергии, заряда и т. д.

в различных физических системах (газах, жидкостях, твердых телах, плазме) и влияние на них внешних полей.
Слайд 6159
Молекулы реальных газов хотя и малы, имеют конечные размеры и, находясь в

состоянии непрерывного хаотического теплового движения, неизбежно сталкиваются друг с другом и со стенками сосуда.
Слайд 8159
Под столкновением двух молекул не будем понимать столкновение двух абсолютно упругих шаров.

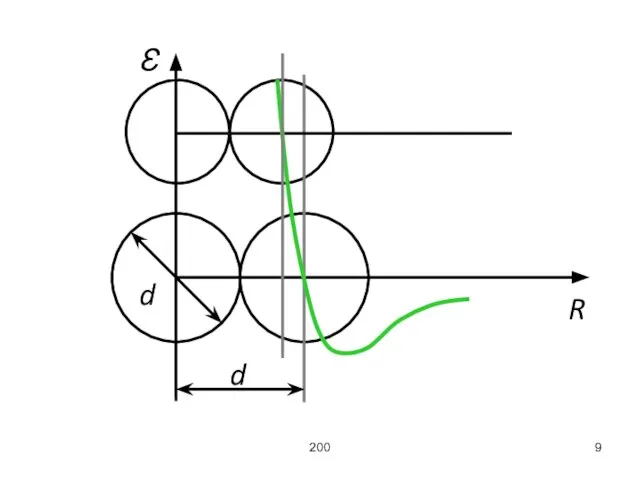
Рассмотрим процесс столкновения двух молекул с помощью зависимости энергии их взаимодействия от расстояния между их центрами.
Слайд 10159
d – диаметр молекулы или эффективный диаметр.
σ = π d2 – эффективное

сечение молекулы.
Если молекула движется со средней скоростью ʋср и претерпевает в среднем ν столкновений за секунду, то средняя длина свободного пробега будет равна
Слайд 11159
Предположим, что все молекулы, кроме одной покоятся. Двигающаяся молекула изменяет своё направление,

если центр неподвижной молекулы находится на расстоянии меньшем эффективного диаметра от линии движения.
Слайд 12159
Таким образом, число столкновений за 1секунду равно числу молекул, центры которых попали

в объём
V = σ ʋср = π d2 ʋср,
то есть
ν' = π d2 ʋср n,
n – концентрация.
Слайд 14159
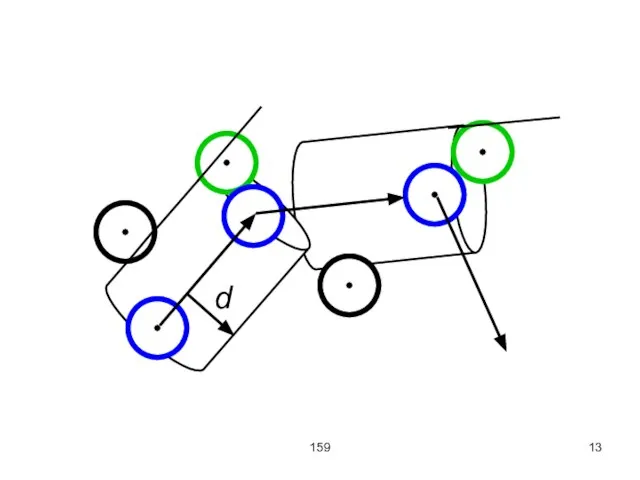
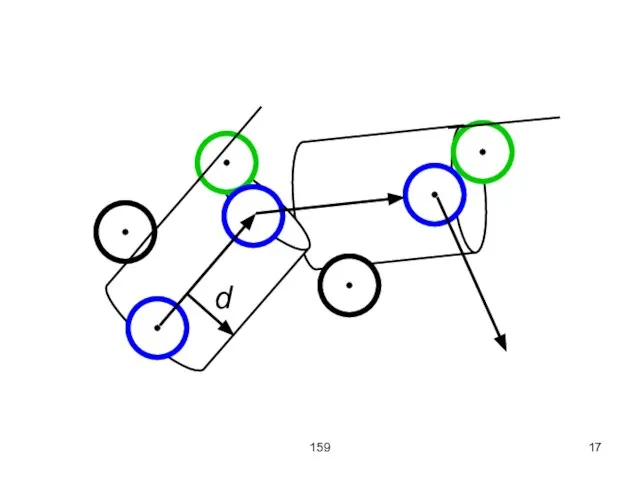
Столкновение происходит тогда, когда расстояние между центрами молекул становится меньше диаметра молекулы

d. Иными словами, при движении молекула описывает некоторый цилиндр, площадь основания которого равняется эффективному сечению
σ = πd2, а ось совпадает с вектором скорости молекулы.
Слайд 15159
Учёт движения всех молекул даст поправку в виде сомножителя √2:
ν =

√2πd2ʋсрn.
Отсюда получаем
Слайд 16159
Длина свободного пробега – расстояние, которое проходит молекула между двумя последовательными соударениями.

Слайд 18159
Связь длины свободного пробега с коэффициентами.
Коэффициент диффузии
Коэффициент теплопроводности
Коэффициент вязкости

Слайд 19159
Здесь ρ – плотность газа,
CVоб – теплоёмкость газа при постоянном объёме на

единицу объёма,
CVуд – теплоёмкость газа при постоянном объёме на единицу массы.
Слайд 21159
44. Явления переноса – диффузия, теплопроводность и вязкость в газах. Молекулярный механизм

процессов переноса. Коэффициенты диффузии, теплопроводности, вязкости; связь между ними.
Слайд 22159
В случае нарушения равновесия возникают потоки либо молекул, либо теплоты и т.п.

Этими процессами занимается физическая кинетика.
Слайд 23159
Диффузия – самопроизвольное выравнивание концентраций в смеси нескольких различных веществ, обусловленное тепловым

движением молекул.
Слайд 24159
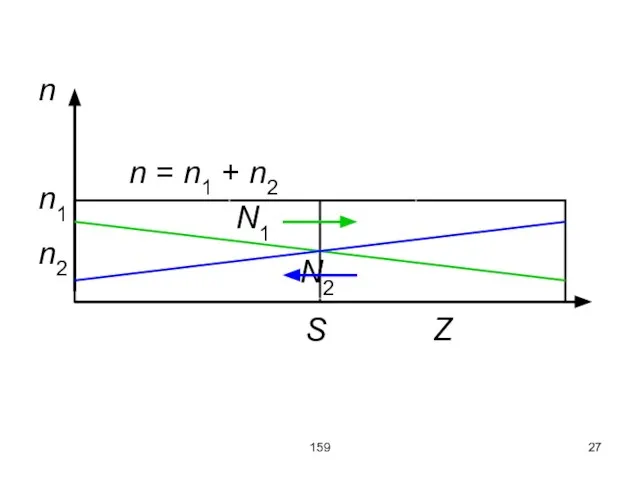
Рассмотрим сосуд, содержащий газ из двух компонент: n1 – концентрация молекул одного

вида, n2 – концентрация молекул другого вида. Полное число молекул на единицу объёма n = n1 + n2.
Слайд 25159
Предположим, что молекулы разных газов распределены неравномерно, но n = const, и

как следствие
p = nkT = const. Поэтому потоки не возникают, но переносятся компоненты, поскольку имеются градиенты концентрации компонент, равные друг другу
Слайд 26159
Сосуд длинный и узкий. На рисунке верхний край сосуда совпадает с величиной

«n». S – поперечное сечение сосуда. N1 и N2 – число молекул первого и второго типа, переносимых в сторону меньшей концентрации данного вещества (этому соответствует знак минус в формуле).
Слайд 28159
Это явление описывается законом Фика
Ni – число частиц переносимых за 1 секунду

через поперечное сечение S. D – коэффициент пропорциональности – коэффициент диффузии (размерность – м2/с).
Слайд 29159
Теплопроводность – перенос тепла (тепловой энергии) от более горячего участка системы к

более холодному (по направлению, противоположному градиенту температуры).
Слайд 30159
Закон Фурье (одномерный и общий случай)
k – коэффициент теплопроводности (размерность – Вт/м*К)

Слайд 31159
Воспользуемся соотношением
и продифференцируем закон Фурье по координате dz:

Слайд 32159
В итоге получим уравнение температуропроводности
– коэффициент температуро-проводности среды, ρ – плотность,

CV – удельная теплоёмкость при постоянном объёме.
Слайд 34159
Вязкость (вязкое трение) – процесс переноса импульса в газе или жидкости от

одного слоя к другому.
В жидкостях вязкость осуществляется непосредственным взаимодействием молекул между собой. Чем меньше подвижность молекул, тем выше коэффициент вязкости – с уменьшением температуры вязкость увеличивается.
Слайд 35159
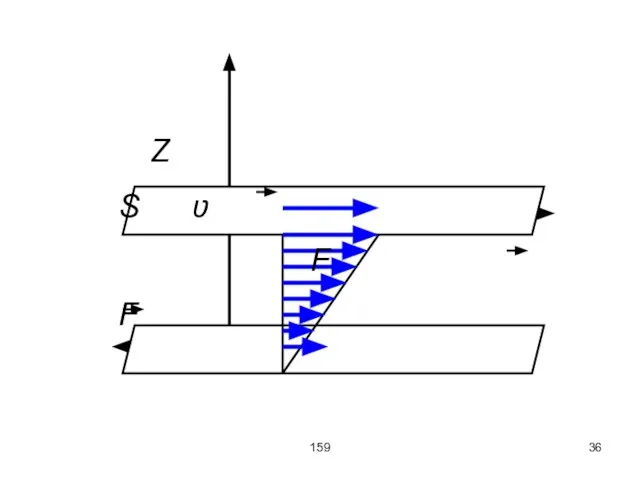
Рассмотрим две параллельные пластины площадью S, одна неподвижна и прикреплена к динамометру,

другая подвижна. Она движется со скорость ʋ по действием некоторой силы F. Динамометр у нижней пластины спустя некоторое время покажет усилие, действующие на неподвижную пластину, равное F.
Слайд 37159
Формула вязкого трения для газов
η – коэффициент вязкости или внутреннего трения (размерность

– Па*с (СИ), Пуаз (СГС),
1 Па*с = 10 П).
Слайд 38159
В газах передача импульса происходит за счёт того, что молекулы перелетают из

одного слоя в другой, с ростом температуры вязкость в газах увеличивается потому, что растёт скорость молекул и они более эффективно переходят из слоя в слой, передавая импульс.
Слайд 39159
Рассмотрим два слоя некоторого газа толщиной dz, скорость слоёв U1 и U2
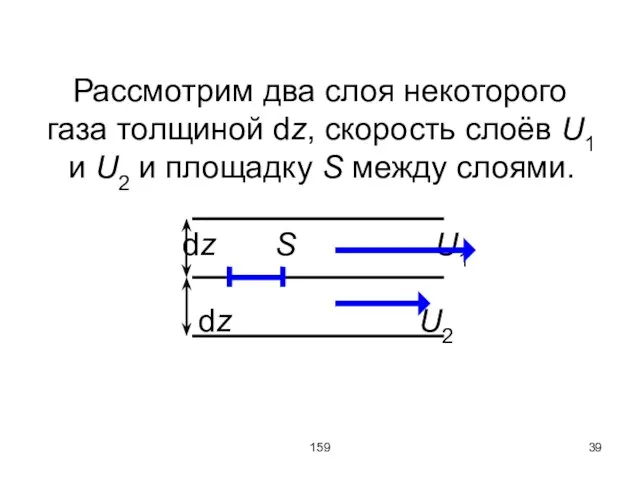
и площадку S между слоями.
dz S U1 dz U2
Слайд 40159
Пусть в какой-то момент времени слои обладают импульсами K1 и K2. Они

постоянно меняются, благодаря переходу молекул из одного слоя в другой. Число молекул, прошедших через площадку S за 1 секунду
Слайд 41159
В итоге, больший импульс уменьшается (он получает молекулы с меньшей упорядоченной скоростью),

меньший – увеличивается.
Запишем импульс, который передаётся от одного слоя к другому через площадку S в единицу времени (m – масса молекулы)
Слайд 42159
Или
Реально, скорость изменяется непрерывно, так как молекула пролетает расстояние λ от удара

до удара, перепишем последнее уравнение
Слайд 43159
Перепишем следующим образом
η – коэффициент вязкости.

Слайд 45159
ЛЕКЦИЯ № 16.
Элементы физической кинетики

Слайд 46159
ВОПРОСЫ
45. Броуновское движение.
46. Элементы неравновесной термодинамики. Кинетической коэффициенты. Теорема Онсагера.

Слайд 48159
Термодинамика неравновесных процессов
Классическая термодинамика даёт полное количественное писание равновесных (обратимых) процессов. Для

неравновесных процессов она устанавливает лишь неравенства, которые указывают возможное направление этих процессов.
Слайд 49159
Задача термодинамики неравновесных процессов – количественное изучение неравновесных процессов для состояний, несильно

отличающихся от равновесного, в частности определение скоростей неравновесных процессов в зависимости от внешних условий.
Слайд 50159
Здесь применяют следующий метод: систему представляют состоящей из элементарных объёмов, которые всё

же настолько велики, что содержат большое число частиц.
Слайд 51159
Рассматривают следующие равновесия:
Неполное равновесие – параметры системы, характеризующие состояние системы, очень слабо

зависят от времени.
Слайд 52159
Локальное равновесие – равновесие в элементарых объёмах среды, можно характеризовать температурой, химическим

потенциалом и другими термодинамическими параметрами, но не постоянными, а зависящими от координат и времени.
Слайд 53159
При локальном термодинамическом равновесии элементов среды состояние среды в целом неравновесно.
На основе

локального равновесия в физической кинетики получают уравнения диффузии, теплопроводности.
Слайд 54159
Время релаксации
Релаксационные явления: равномерное распределение по всей макросистеме температуры, давления, концентрации, установление

ламинарного течения или полное прекращение движения слоёв жидкости относительно друг друга.
Слайд 55159
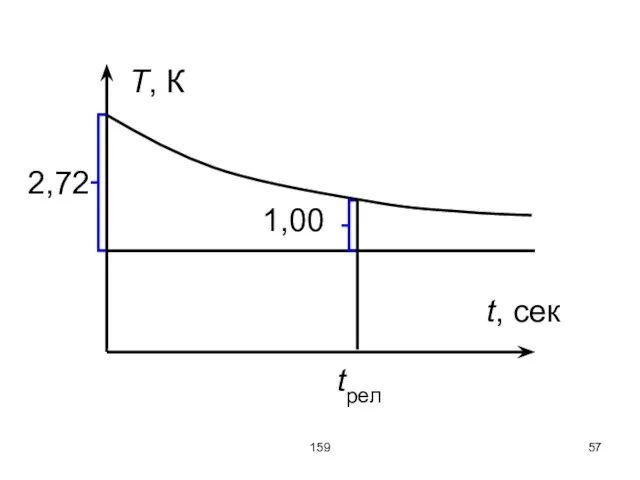
Время релаксации – время, за которое первоначальное отклонение какой-либо величины от равновесного

значения уменьшается в «е» раз.
Слайд 56159
Пример: пуст в теплоизолированном поршне (цилиндрический сосуд) создадим в некотором месте скачёк

давления, что приведёт к возрастанию температуры в этой области, допустим на 2,72 К. временем релаксации здесь будет время, за которое эта разность температур уменьшится в «е» раз и станет равной 1,00 К.
Слайд 58159
Броуновское движение – хаотическое движение взвешенных микрочастиц в газах или жидкостях.
Теорию движения

броуновских частиц разработали А. Эйнштейн и М. Смолуховский.
Слайд 59159
Модель: Блуждание «абсолютно пьяного человек».
Каждый раз человек смещается на 1 шаг вправо

или влево.
Слайд 60159
0-й шаг (начало)
1-й шаг 1 1
2-й шаг 1 2 1
3-й шаг 1
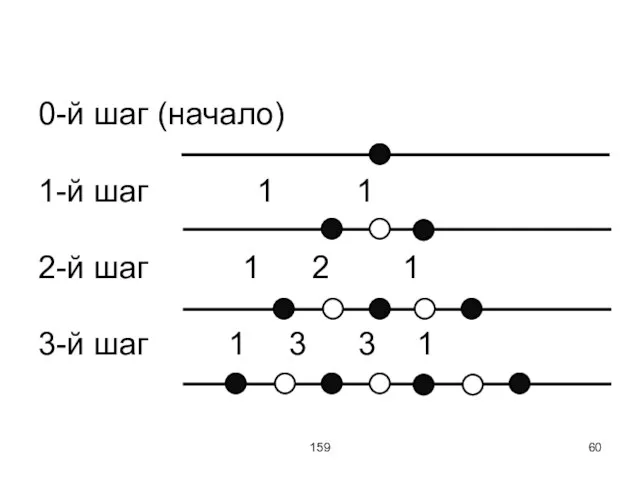
3 3 1
Слайд 61159
Среднее смещение равно нулю, но средний квадрат пропорционален числу шагов или времени.

То же и для броуновской частицы.
Слайд 62159
Уравнение движения
F0 – сила, действующая на броуновскую частицу, m – масса броуновской

частицы, B – коэффициент – подвижность частицы.
Слайд 63159
Движение броуновской частицы определяется хаотически меняющейся силой f, поэтому от постоянной силы

F0 перейдём к f.
Слайд 64159
Используем следующие выражения
умножим на x уравнение движения
и получим:

Слайд 65159
Усредним полученное выражение по времени:
Перепишем энергию теплового движения:

Слайд 66159
Получаем:
Если пропорционален времени
( ~ t), то первый член исчезает, и мы получаем формулу Эйнштейна:

Слайд 67159
В случае движения в плоскости
в объёме

Слайд 68159
Броуновское движение как диффузия
Рассмотрим броуновское движение в поле сил тяжести;

Слайд 69159
в стационарном состоянии, когда установится больцмановское распределение концентрации частиц
поток частиц, движущихся по

направлению силы со скоростью Bf, должен компенсироваться диффузионным потоком в направлении уменьшения концентрации,
Слайд 70159
То есть
Dбр – коэффициент диффузии броуновских частиц.

Слайд 71159
Отсюда
формула Эйнштейна принимает вид

Слайд 73159
46. Элементы неравновесной термодинамики. Кинетической коэффициенты. Теорема Онсагера.

Слайд 74159
В случае изолированной системы выполняется второе начало термодинамики
и в случае равновесного состояния

энтропия максимальна (тепловая смерть вселенной).
Слайд 75159
В открытых системах происходит постоянный обмен с окружающей средой энергией и веществом.

Здесь даже малые воздействия могут привести к значительным последствиям. В описании неравновесных процессов используют понятие возрастание энтропии системы
Слайд 76159
При определённых условиях суммарное уменьшение энтропии за счёт обмена с внешней средой

может превысить её внутреннее производство. Появляется неустойчивость предшествующего неупорядоченного однородного состояния, возникают и возрастают крупномасштабные флуктуации.
Слайд 77159
При этом оказывается возможной самоорганизация – создание определённых структур из хаоса, неупорядоченности
(примеры:

тайфун, торнадо, смерчи).
Эти структуры могут последовательно переходить во всё более упорядоченные состояния. В таких системах энтропия убывает.
Слайд 78159
Принцип Онсагера
Онсагер, на основе выше сказанного, предположил, что при небольших отклонениях от

равновесия существует линейная связь между потоками Ii и термодинамическими силами Xj.
Lij – кинематический или феноменологический коэффициент.
Слайд 79159
В термодинамике необратимых процессов скорость приращения энтропии (производство энтропии) за счёт необратимых

процессов может быть представлена в виде
Слайд 80159
Коэффициент Lij отражает факт существования перекрёстных эффектов (процессов) перенос одной величины (заряд,

масса, энергия и т.д.) неразрывно связан с переносом другой (импульс, температура и т.д.).
Слайд 81159
Шумы
флуктуации накладывают ограничение на чувствительность приборов. Как правило, чувствительность не достигает уровня

флуктуаций (например давление).
Слайд 82159
Тепловой шум: электроны в электрических приборах ведут себя подобно молекулам идеального газа,

соответственно, их концентрация, в различных частях электрической системы, испытывает флуктуации, что приводит к скачкам напряжения и силы тока.
Слайд 83159
Если отношение «сигнал/шум» мало, то сигнал идёт с большим искажением либо его

невозможно обнаружить.
Слайд 84159
Дробовой шум: шум, определяемый дискретностью электрического заряда.
В полупроводниках два типа носителей заряда:

дырки и электроны, которые могут генерироваться и рекомбинировать. Поэтому величина шума в полупроводниках в два раза выше, чем в проводниках.
Слайд 87159
ВОПРОСЫ
47. Кристаллы. Кристаллическая решётка. Преобразования симметрии. Жидкие кристаллы.
48. Неравновесные процессы. Синергетика. Бифуркация.

Слайд 88159
47. Кристаллы. Кристаллическая решётка. Преобразования симметрии. Жидкие кристаллы.

Слайд 89159
Кристаллы (krystallos (греч.) – лёд) – твёрдые тела обладающие трёхмерной периодической атомной

структурой и, при равновесных условиях образования, имеющие естественную форму правильных симметричных многогранников.
Слайд 90159
Кристаллы обладают симметрией. Здесь симметрия это свойство тела совмещаться с самим собой

при определённых перемещениях, называемых преобразованиями или операциями симметрии.
Эти перемещения не должны сопровождаться изменением расстояния между атомами.
Слайд 91159
Преобразования симметрии:
1) параллельный перенос всех точек тела на определённое расстояние (трансляция);
2) поворот

тела вокруг некоторой оси на определённый угол;
3) отражение в плоскости;
4) инверсия или отражение в точке;
а также все комбинации таких преобразований.
Слайд 92159
Таким образом, можно отменить основное отличие кристаллов от жидкостей и аморфных тел:

периодичность пространственного расположения атомов, молекул или ионов, из которых состоит кристалл. Такая периодичность получила название дальнего порядка.
Слайд 93159
В аморфных и жидких телах упорядоченное расположение частиц может распространяться только на

соседние атомы – ближний порядок.
Слайд 94159
Кристаллическая решётка – упорядоченное расположение атомов, молекул или ионов, характеризующиеся периодичной повторяемостью

в трёх измерениях.
Слайд 95159
Плоские грани кристалла, образовавшегося в равновесных условиях, соответствуют атомным плоскостям, рёбра –

рядам атомов. Расположение атомов соответствует минимуму энергии.
Слайд 96159
Для описания кристаллической решётки достаточно знать размещение атомов в её элементарной ячейке,

повторением которой путём параллельных переносов (трансляций) образуется кристаллическая решётка.
Слайд 97159
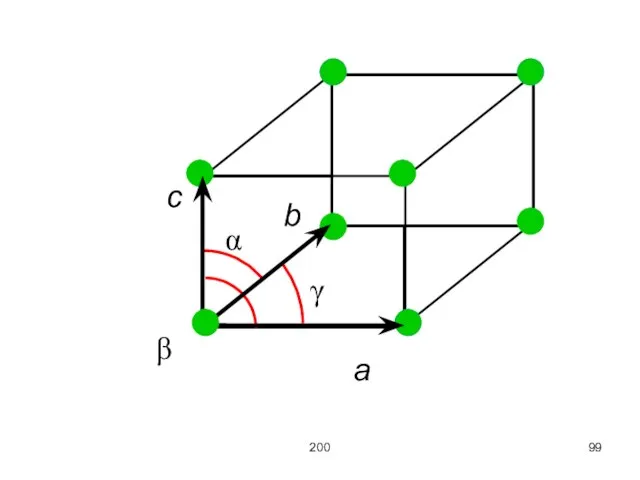
Элементарная ячейка имеет форму параллелепипеда. Рёбра элементарного параллелепипеда a, b, c называются

постоянными или периодами кристаллической решётки либо векторами трансляции. Этот параллелепипед характеризуется также углами α, β, γ между рёбрами.
Слайд 98159
Параллелепипед минимального объёма, содержащий наименьшее число атомов, называется примитивной (элементарной) ячейкой.
Величины a,

b, c и α, β, γ однозначно определяют элементарную ячейку и называются её параметрами.
Слайд 101159
Кристаллическая решётка, как правило, обладает одновременно несколькими видами симметрии. Но возможны всего

230 комбинаций элементов симметрии, которые называются пространственными группами. 230 групп делятся на 32 класса. Классы, по форме элементарной ячейки делятся на семь кристаллических систем (сингоний).
Слайд 102159
1) Триклинная система.
a ≠ b ≠ c и α ≠ β ≠

γ.
Элементарная ячейка имеет форму косоугольного параллелепипеда.
Слайд 103159
2) Моноклинная система.
a ≠ b ≠ c, α = γ = 90º,

β ≠ 90º.
Элементарная ячейка имеет форму прямой призмы, в основании которой лежит параллелограмм (т.е. форму прямого параллелепипеда).
Слайд 104159
3) Ромбическая система.
a ≠ b ≠ c, α = β = γ

= 90º.
Элементарная ячейка имеет форму прямоугольного параллелепипеда.
Слайд 105159
4) Тетрагональная система.
a = b ≠ c, α = β = γ

= 90º.
Элементарная ячейка имеет форму прямой призмы с квадратным основанием.
Слайд 106159
5) Ромбоэдрическая (или тригональная) система.
a = b = c, α = β

= γ ≠ 90º.
Элементарная ячейка имеет форму куба, деформированного сжатием или растяжением вдоль диагонали.
Слайд 107159
6) Гексагональная система.
a = b ≠ c, α = β = 90º,

γ = 120º.
Если составить вместе три элементарные ячейки, то получается правильная шестиугольная призма.
Слайд 108159
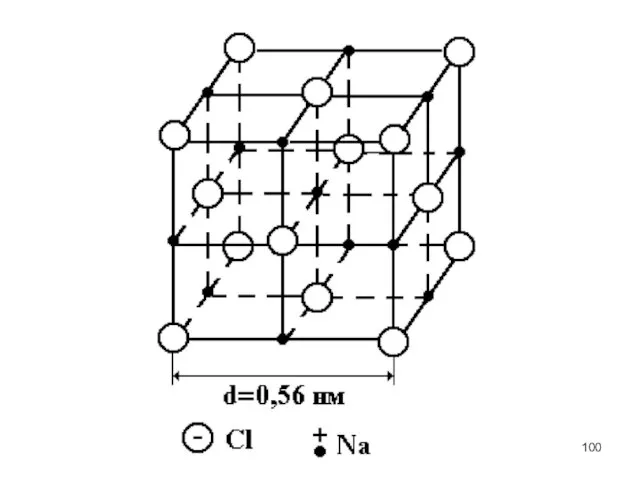
7) Кубическая система.
a = b = c, α = β = γ

= 90º.
Элементарная ячейка имеет форму куба.
Слайд 109159
Жидкие кристаллы
Особое состояние некоторых органических веществ, в котором они обладают свойствами жидкости

– текучестью, но сохраняют определённую упорядоченность в расположении молекул и анизотропию ряда физических свойств, характерную для твёрдых кристаллов.
Слайд 110159
Число химических соединений для которых найдены жидкие кристаллы несколько тысяч. Но для

использования годятся несколько десятков.
Слайд 111159
По способу получения различают два типа жидких кристаллов: термотропные и лиотропные. Первые

образуются при нагревании твердых кристаллов или при охлаждении изотропных жидкостей и существуют в некотором температурном интервале.
Слайд 112159
Вторые образуются при растворении твердых органических веществ, например, в воде или других

растворителях. Оба типа жидких кристаллов имеют несколько модификаций – жидкокристаллических фаз, каждой из которых на фазовой диаграмме соответствует определенная область.
Слайд 113159
Эта область зависит от типа вещества и может находиться как при низких

до − 60 °С, так и при высоких температурах ~ 400 °С.
Слайд 114159
Представителем типичного термотропного жидкого кристалла является 4-метоксибензилиден-4′ – бутиланилина (МББА), по форме
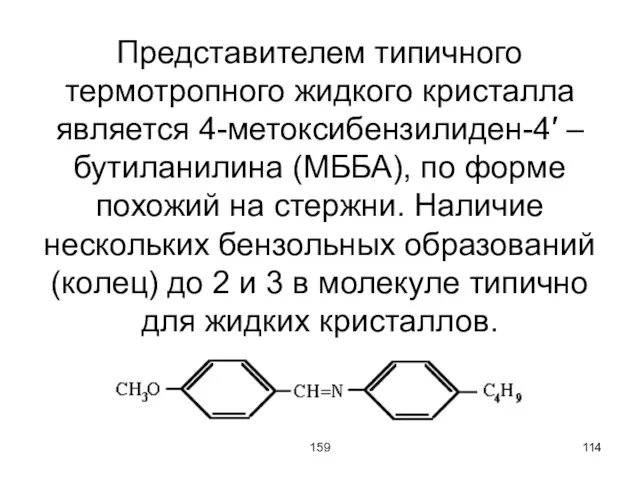
похожий на стержни. Наличие нескольких бензольных образований (колец) до 2 и 3 в молекуле типично для жидких кристаллов.
Слайд 115159
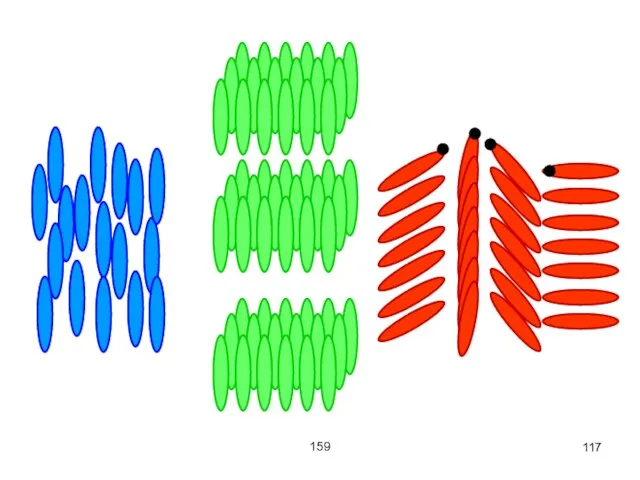
Нематические жидкие кристаллы – молекулы параллельны, но сдвинуты вдоль своих осей, одна

относительно другой на произвольные расстояния.
Слайд 116159
Смектические жидкие кристаллы – молекулы параллельны друг другу и расположены слоями.
Холестерические жидкие

кристаллы – похожи на нематические, но отличаются дополнительным закручиванием молекул в направлении, перпендикулярном их длинным осям.
Слайд 119159
48. Неравновесные процессы. Синергетика. Бифуркация.

Слайд 120159
Неравновесные процессы
Классическая термодинамика описывает стабильность, равновесие. Вблизи равновесия система однозначно реагирует на

не слишком большое возмущение, возвращаясь в состояние равновесия.
Слайд 121159
При этом частицы, составляющие систему, взаимодействуют только на близких расстояниях и ничего

«не знают» о частицах, расположенных достаточно далеко. Здесь вполне адекватна модель замкнутой системы.
Слайд 122159
Однако, если система далеко отклоняется от состояния равновесия, то возврат к начальному

состоянию необязателен.
Здесь целесообразно рассматривать модель открытых диссипативных систем, постоянно обменивающихся с окружающей средой энергией и веществом.
Слайд 123159
Именно в открытых системах для состояний, далёких от равновесия, возникают эффекты согласования,

когда частицы как бы устанавливают связь друг с другом на макроскопических расстояниях, через макроскопические интервалы времени.
Слайд 124159
В результате согласованного взаимодействия надсистем происходят процессы упорядочения, возникновения из хаоса определённых

структур, их преобразования и усложнения.
Слайд 125159
Возникновение макроскопических структур обусловлено рождением коллективных типов движения (мод) под действием крупномасштабных

флуктуаций, их конкуренцией, отбором наиболее приспособленных мод,
Слайд 126159
то есть в конечном счёте спонтанное возникновение структур в неупорядоченных системах связано

с совместным коллективным поведением подсистемы, образующих систему.
Слайд 127159
Область науки, изучающая эти процессы, получила название «синергетика».

Слайд 128159
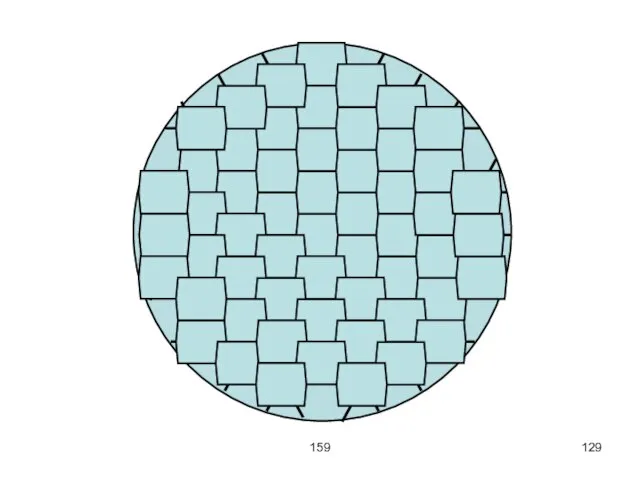
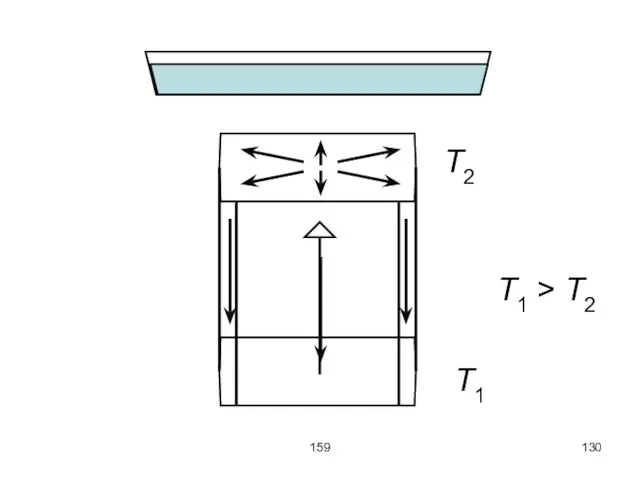
Пример1. Ячейка Бенара.
На сковороду наливают тонкий слой минерального масла (5 мм) и

подогревают снизу горячей водой. При достижении критического градиента в жидкости возникают потоки и образуются красивые шестиугольные ячейки. В центре ячейки конвекционный поток движется вверх, а по краям – вниз.
Слайд 131159
Ячейки Бенара в неравновесной термодинамике играют исключительную роль, поскольку в этом явлении

очень отчётливо проявляются все основные черты термодинамики необратимых процессов.
Слайд 132159
По сравнению с однородным состоянием конвективные ячейки являются более высокоорганизованной структурой –

открытая система отдаёт энтропию. Образование же её связано с неустойчивостью крупномасштабного конвективного движения и обусловлено следующими обстоятельствами.
Слайд 133159
Если слой жидкости сильно нагреть, то возникает разность (градиент) температур ΔT между

нижней и верхней поверхностями. Такой температурный градиент называется инверсным, так как жидкость у нижней поверхности вследствие теплового расширения имеет меньшую плотность, чем вблизи верхней поверхности.
Слайд 134159
Из-за силы тяжести и архимедовой выталкивающей силы такая система оказывается неустойчивой, поскольку

«лёгкий» нижний слой и «тяжёлый» верхний стремятся поменяться местами.
Слайд 135159
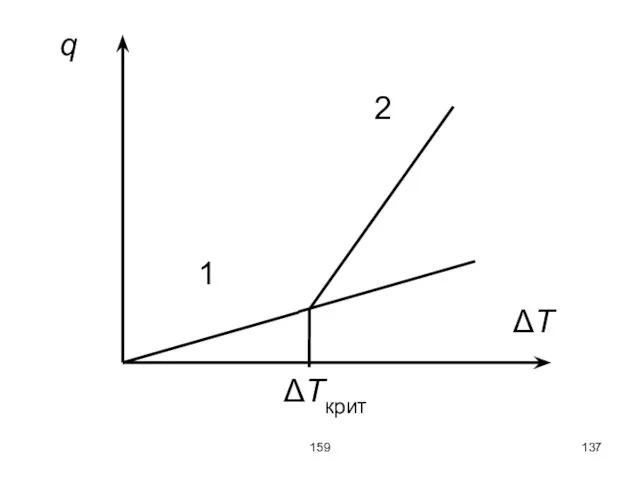
Однако, вследствие вязкости жидкости, при небольших градиентах температуры движение не возникает и

тепло передаётся только путём теплопроводности.
Слайд 136159
Лишь при достижении критического значения температурного градиента появляется конвекционный поток, обладающий характерной

структурой в виде шестиугольных ячеек. Внутри ячеек жидкость поднимается вверх, а по краям спускается вниз.
Слайд 138159
Бифуркация- качественное различие в поведение объекта, при незначительном изменении параметра, от которого

зависит объект.
Слайд 139159
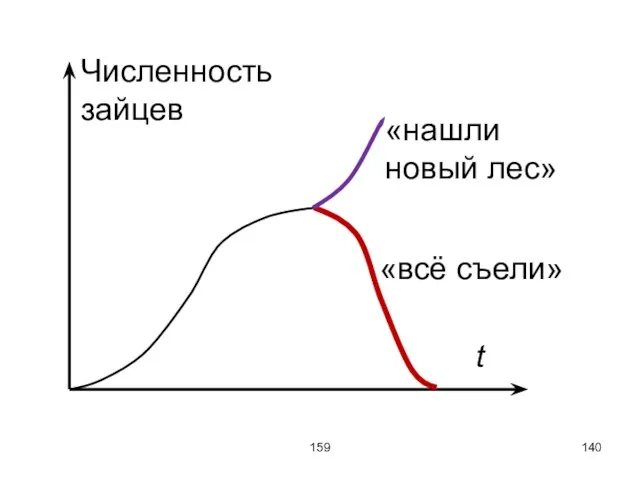
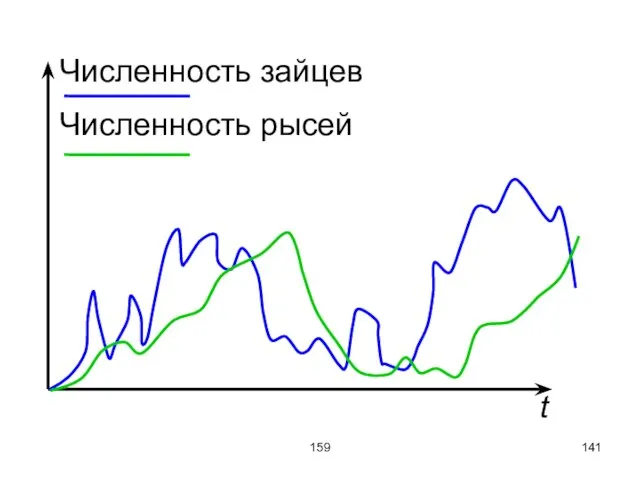
Пример 2.
Эволюция численности зайцев и рысей.
В результате взаимодействия двух биологических систем возникают

периодические колебания численности особей.
Слайд 140159
t
Численность зайцев
«всё съели»
«нашли новый лес»





























































































































 Ускорение свободного падения на Земле идругих небесных телах
Ускорение свободного падения на Земле идругих небесных телах Определение показателя преломления стекла
Определение показателя преломления стекла Экспериментальная ядерная физика
Экспериментальная ядерная физика ИК-спектроскопия (часть 1)
ИК-спектроскопия (часть 1) Последовательное и параллельное соединение проводников
Последовательное и параллельное соединение проводников Презентация на тему Исаак Ньютон
Презентация на тему Исаак Ньютон  Напряженность электрического поля. Урок 52
Напряженность электрического поля. Урок 52 Тиристоры
Тиристоры Сопротивляемость человеческого тела в разных условиях
Сопротивляемость человеческого тела в разных условиях Бином Ньютона. Треугольник Паскаля
Бином Ньютона. Треугольник Паскаля Исследование процессов неупругих столкновений
Исследование процессов неупругих столкновений Презентация на тему Сила трения покоя
Презентация на тему Сила трения покоя  Приборы для измерения давления
Приборы для измерения давления Правила работы с микроскопом
Правила работы с микроскопом Цепные передачи
Цепные передачи Двигатель внутреннего сгорания
Двигатель внутреннего сгорания Технология подготовки машинно-тракторного агрегата для внесение минеральных удобрений и выполнение работ на нем
Технология подготовки машинно-тракторного агрегата для внесение минеральных удобрений и выполнение работ на нем Электрическое сопротивление
Электрическое сопротивление Кинематика
Кинематика Двойное лучепреломление. (Лекция 39)
Двойное лучепреломление. (Лекция 39) Методы, основанные на индуцированном переходе из одной фазы в другую через разделяющую их третью фазу. (Лекция 7)
Методы, основанные на индуцированном переходе из одной фазы в другую через разделяющую их третью фазу. (Лекция 7) Izmerenie_temperatury
Izmerenie_temperatury Методы наблюдения и регистрации элементарных частиц. Тест для 11 класса
Методы наблюдения и регистрации элементарных частиц. Тест для 11 класса Квантовая оптика
Квантовая оптика Тема 4. ФИЗИЧЕСКИЕ КАРТИНЫ МИРА
Тема 4. ФИЗИЧЕСКИЕ КАРТИНЫ МИРА Конструктивные изменения, внесенные в устройства техники ОАО Гомсельмаш
Конструктивные изменения, внесенные в устройства техники ОАО Гомсельмаш 11кл. Электромагн индукция (3)
11кл. Электромагн индукция (3) Физическая викторина
Физическая викторина