Содержание
- 2. Молекулярная физика - раздел физики, изучающий строение и свойства вещества, исходя из молекулярно-кинетических представлений о его
- 3. Таким образом, при исследовании тепловых явлений выделились два научных направления: Термодинамика, изучающая тепловые процессы без учета
- 4. Основные положения МКТ. Уравнение состояния идеального газа.
- 5. Основные положения молекулярно-кинетической теории Молекулярно-кинетическая теория (МКТ) занимается изучением свойств веществ, основываясь при этом на представлениях
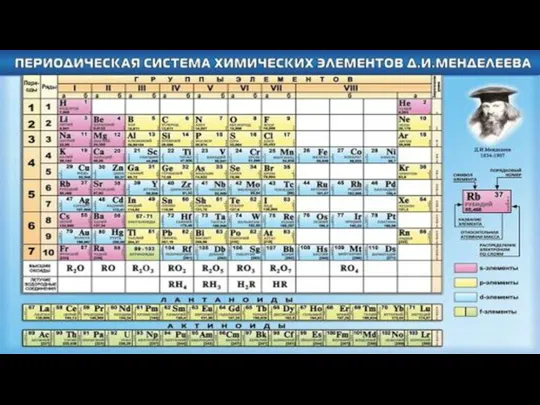
- 6. Атом — это наименьшая частица данного химического элемента, сохраняющая все его химические свойства. Химических элементов не
- 7. Масса и размеры молекул Согласно муждунар. Соглашению массы вех атомов принято сравнивать с массой атома углерода
- 8. 1 моль — количество вещества, в котором содержится столько же молекул или атомов, сколько их в
- 9. Так как, в одном моль вещества содержится число молекул, равное числу Авогадро (Na=6,02×1023 моль-1), а масса
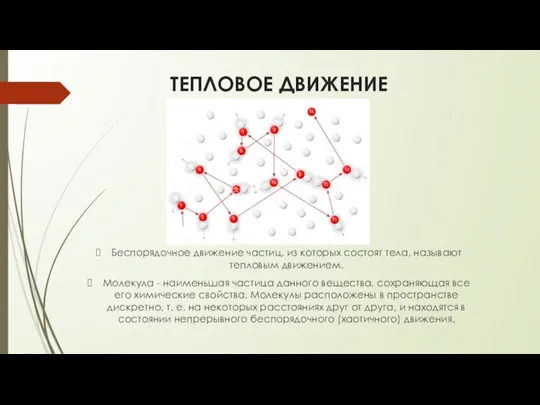
- 10. ТЕПЛОВОЕ ДВИЖЕНИЕ Беспорядочное движение частиц, из которых состоят тела, называют тепловым движением. Молекула - наименьшая частица
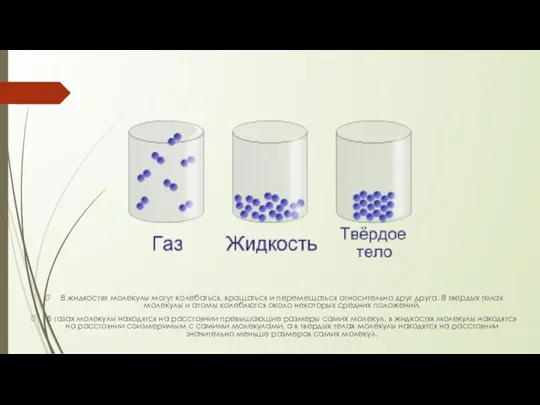
- 11. В жидкостях молекулы могут колебаться, вращаться и перемещаться относительно друг друга. В твердых телах молекулы и
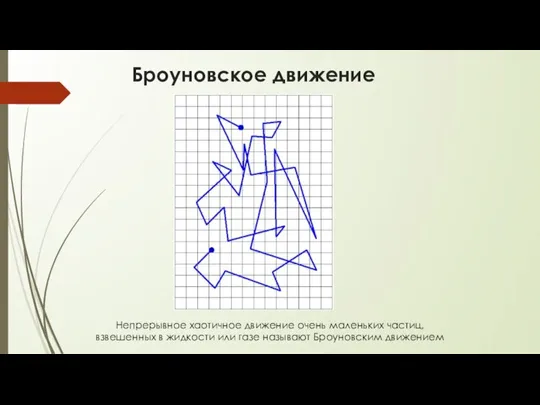
- 12. Броуновское движение Непрерывное хаотичное движение очень маленьких частиц, взвешенных в жидкости или газе называют Броуновским движением
- 13. Диффузия — явление проникновения молекул одного вещества в промежутки между молекулами другого вещества.
- 14. Температура Температура T - - это физическая величина, характеризующая степень нагрева предмета, измеряемую в градусах по
- 15. Приборы для измерения температуры посредством контакта с исследуемой средой (телом) называются термометрами (от греч. therme —
- 16. Температурная шкала, началом отсчёта которой является абсолютный нуль, а единицей температуры — градус Цельсия, называется абсолютной
- 17. Единица абсолютной температуры называется кельвином (K). Абсолютному нулю (T = 0) соответствует температура t = −273,15
- 18. Другим подтверждением существования сил межмолекулярного взаимодействия служит наличие трёх агрегатных состояний вещества
- 19. Уравнение состояния идеального газа Для описания разреженных газов в физике используется модель идеального газа. В рамках
- 20. Таким образом, идеальный газ — это газ, частицы которого являются не взаимодействующими на расстоянии материальными точками
- 21. Первый и второй закон термодинамики. Работа идеального газа. Термодинамической системой называется макроскопическое тело или система тел,
- 22. Термодинамический процесс (или просто процесс) — это изменение состояния газа с течением времени. В ходе термодинамического
- 23. Опираясь на работы Джоуля и Майера, Клаузнус впервые высказал мысль, сформировавшуюся впоследствии в первое начало термодинамики.
- 24. Количество теплоты, сообщенное газу, идет на увеличение внутренней энергии газа и совершение газом внешней работы Q
- 25. Две эквивалентные формулировки второго закона термодинамики принадлежат Клаузиусу и Томсону (лорду Кельвину). Постулат Клаузиуса. Невозможен процесс,
- 26. Второе начало термодинамики (второй закон термодинамики) устанавливает существование энтропии как функции состояния термодинамической системы и вводит
- 27. Основное уравнение это уравнение Больцмана, которое позволяет вычислять параметр энтропия. S = Q/ T S –
- 28. Работу идеального газа можно выразить из 1 закона термодинамики: А=∆ Q-∆U где Q – количество теплоты,
- 29. Задачи 1. В баллоне находится 20 моль газа. Сколько молекул газа находится в баллоне?
- 31. 2. Определить массу молекулы кислорода.
- 32. 3. Сколько молекул содержится в 5 кг кислорода?
- 33. 4. Сколько молекул содержится в 1 л воды?
- 34. 5. Какое значение температуры по шкале Кельвина соответствует температуре 100° C?
- 35. 6. Определить число молекул, содержащихся в 1 г воды.
- 36. 7. Определить количество вещества, содержащегося в медной отливке массой 96 кг.
- 37. 8. Найти число молекул в 2 кг углекислого газа.
- 38. Задача 9. Найти массу природного горючего газа объемом 64 м3, считая, что объем указан при нормальных
- 40. Задача 10. Воздух объемом 1,45 м3, находящийся при температуре 20oC и давлении 100 кПа, превратили в
- 41. Задача 11. Какое количество вещества содержится в газе, если при давлении 200 кПа и температуре 240
- 42. Определить давление кислорода в баллоне объемом V = 1 м3 при температуре t=27 °С. Масса кислорода
- 43. Баллон емкостью V= 12 л содержит углекислый газ. Давление газа Р = 1 МПа, температура Т
- 44. При температуре Т = 309 К и давлении Р = 0,7 МПа плотность газа ρ =
- 45. Какова плотность водорода при нормальном атмосферном давлении и температуре 20°С.
- 46. До какой температуры Т1 надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том
- 47. Газ находился в цилиндре с поршнем площадью поперечного сечения 200 см^2. После того, как газ нагрели,
- 48. Над газом была совершена работа 55 Дж, а его внутренняя энергия увеличилась на 15 Джоулей. Какое
- 49. Кислород нагрели при постоянном давлении p=80 кПа. Объем газа увеличился с 1 до 3 кубических метров.
- 51. Скачать презентацию












































 Закон сохранения массы веществ
Закон сохранения массы веществ Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Стакан-непроливайка
Стакан-непроливайка Автоматическое управление. Типовая упрощенная структура САУ
Автоматическое управление. Типовая упрощенная структура САУ Физические явления языком литературы
Физические явления языком литературы Реактивное движение в технике, животном и растительном мире. 10 класс
Реактивное движение в технике, животном и растительном мире. 10 класс Закон сохранения импульса
Закон сохранения импульса Соединения проводников. Задачи
Соединения проводников. Задачи Рулевое устройство судна
Рулевое устройство судна Импульс. Закон сохранения импульса
Импульс. Закон сохранения импульса Посадочный размер блока. Диаметр ТЭНа
Посадочный размер блока. Диаметр ТЭНа Итоговая контрольная работа
Итоговая контрольная работа Иллюзии и Физика. Вечная Борьба
Иллюзии и Физика. Вечная Борьба Внутренняя энергия. Агрегатные состояния вещества. Занятие 1. Часть 1
Внутренняя энергия. Агрегатные состояния вещества. Занятие 1. Часть 1 Относительность движения
Относительность движения Үйкеліс күшін зерттеу
Үйкеліс күшін зерттеу Преломление света. Закон преломления
Преломление света. Закон преломления Урок4 РПД
Урок4 РПД Механика деформируемого твердого тела
Механика деформируемого твердого тела ЯМР-спектроскопия. Часть 1
ЯМР-спектроскопия. Часть 1 Строение атома
Строение атома Теплофизика процесса резания
Теплофизика процесса резания Курс физики в домашней школе ФОКСФОРД. Базовый уровень
Курс физики в домашней школе ФОКСФОРД. Базовый уровень High-speed Machining
High-speed Machining Изменение внутренней энергии газа в процессе теплообмена и совершения работы. Первое начало термодинамики. Лекция 5
Изменение внутренней энергии газа в процессе теплообмена и совершения работы. Первое начало термодинамики. Лекция 5 The atom
The atom Технология наночастиц металлов. Тема 4
Технология наночастиц металлов. Тема 4 Паровые двигатели
Паровые двигатели