Содержание
- 2. Цель лекции – познакомиться с квантово-механической моделью атома водорода. Вопросы лекции: Атом водорода в квантовой механике
- 3. Вопрос №1 Атом водорода в квантовой механике
- 4. Воспользуемся сферической СК: Электрон движется в кулоновском поле ядра. Это поле – центрально-симметричное, стационарное.
- 5. Потенциальная энергия электрона: Волновая функция (ВФ) электрона: Плотность распределения вероятностей для координат электрона:
- 6. Квантово-механическая модель атома Заряд электрона непрерывно распределен в «электронном облаке» с плотностью Электрон – материальная точка,
- 7. Найти ВФ позволяет стационарное уравнение Шредингера Орбиталь – область пространства, в которой электрон «размазан» с неравномерной
- 8. Уравнение (12) имеет решения для дискретного набора собственных значений энергии:
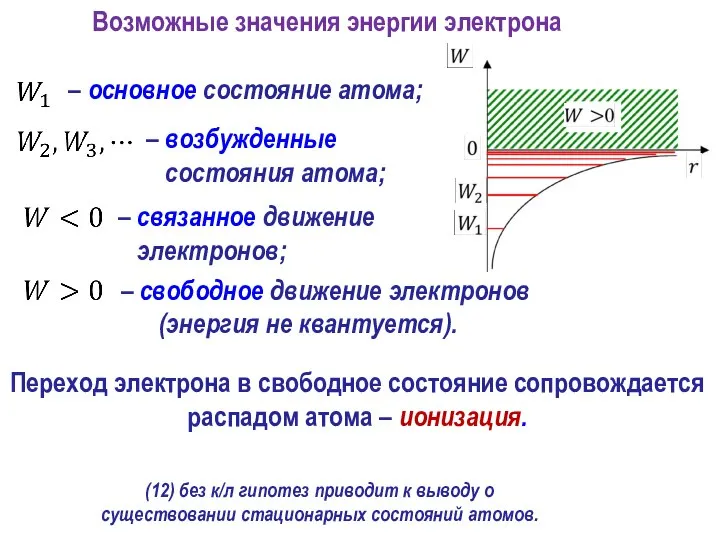
- 9. Возможные значения энергии электрона (12) без к/л гипотез приводит к выводу о существовании стационарных состояний атомов.
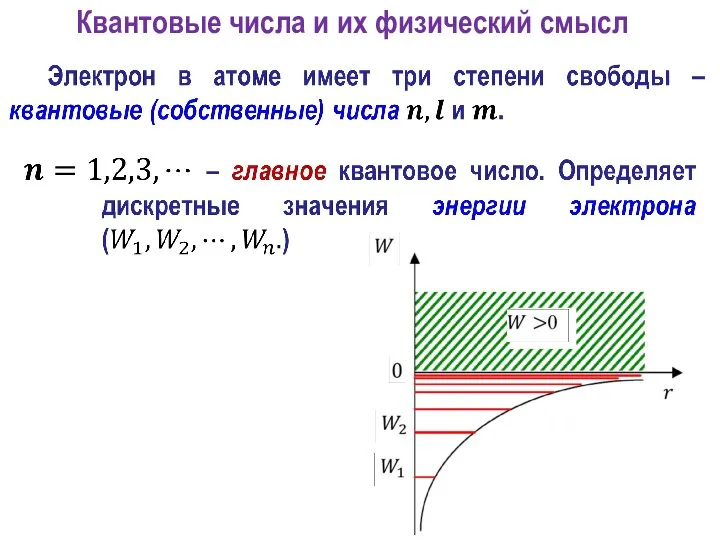
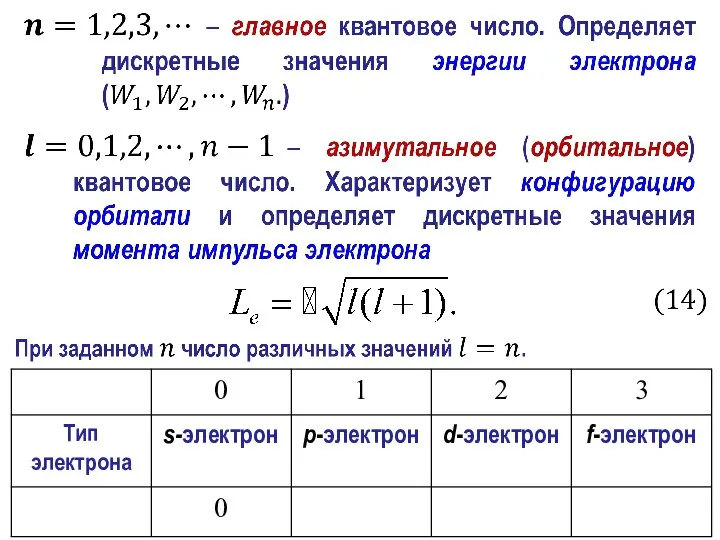
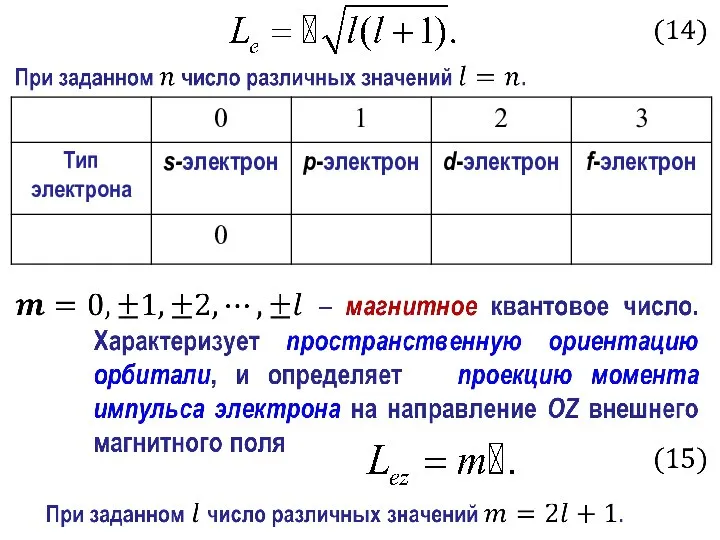
- 10. Квантовые числа и их физический смысл
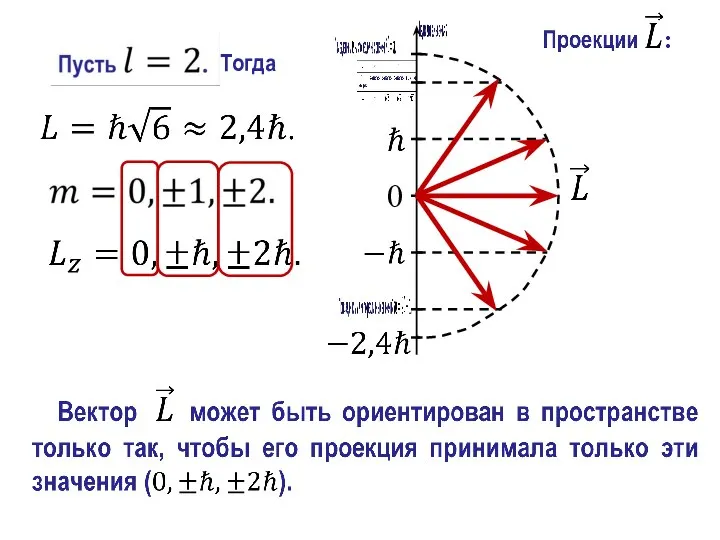
- 13. Тогда
- 14. Такие состояния называются вырожденными, а число вырожденных состояний – кратностью вырождения. Вырождение энергетического уровня Каждое конкретное
- 15. Состояния электрона, соответствующие первым трём энергетическим уровням
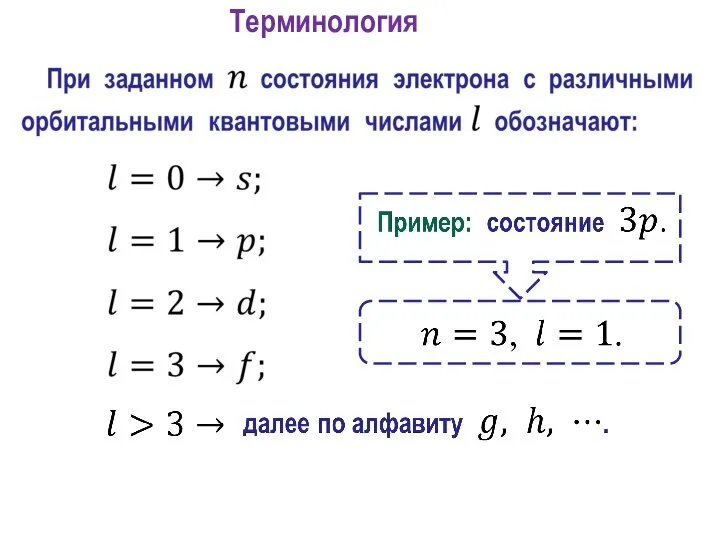
- 16. Терминология
- 17. Вопрос №2 Правила отбора. Спектр атома водорода
- 18. Теория Бора не объясняет различную интенсивность спектральных линий. В квантовой механике доказывается, что переход электрона с
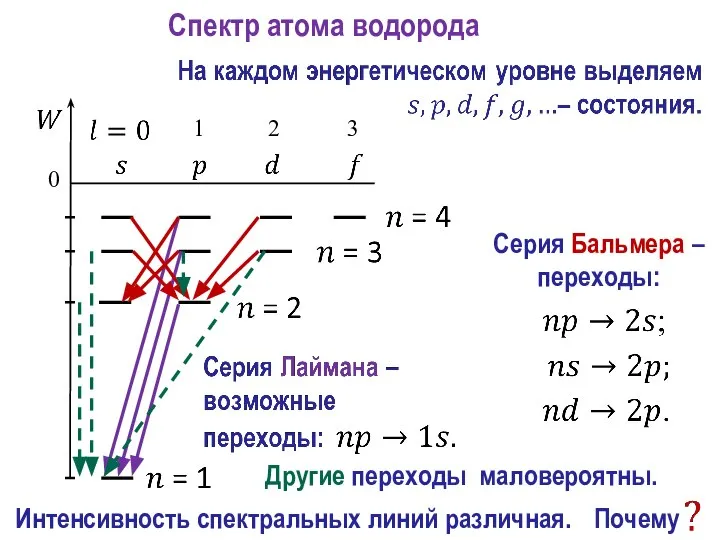
- 19. Спектр атома водорода Серия Бальмера – переходы: Интенсивность спектральных линий различная. Другие переходы маловероятны.
- 20. значит, на него приходится большее число испускаемых фотонов и соответствующая ему спектральная линия ярче.
- 21. Вопрос №3 1s состояние электрона в атоме водорода
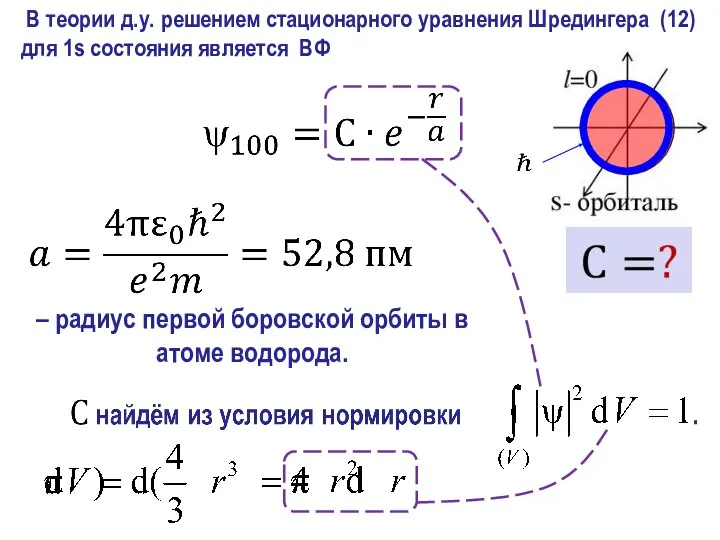
- 22. В теории д.у. решением стационарного уравнения Шредингера (12) для 1s состояния является ВФ 1s состоянию электрона
- 23. – радиус первой боровской орбиты в атоме водорода.
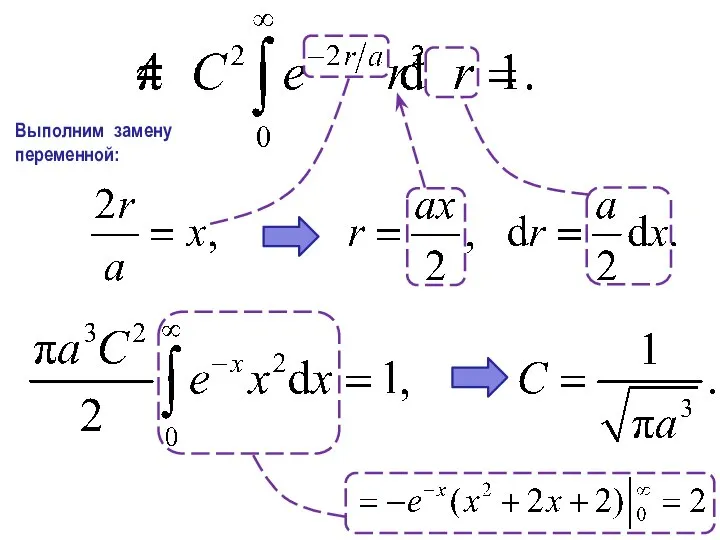
- 24. Выполним замену переменной:
- 26. Анализ решения Пространственная плотность распределения положения электрона: Т. обр. ВФ:
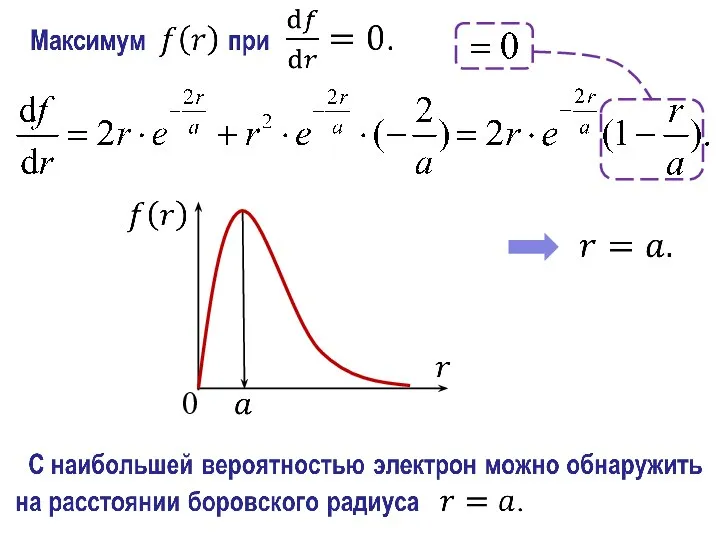
- 27. Вероятность определяется функцией
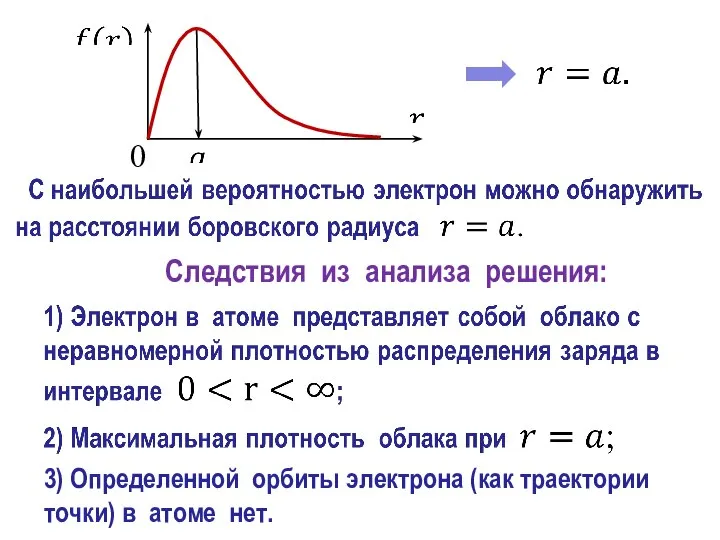
- 29. 3) Определенной орбиты электрона (как траектории точки) в атоме нет. Следствия из анализа решения:
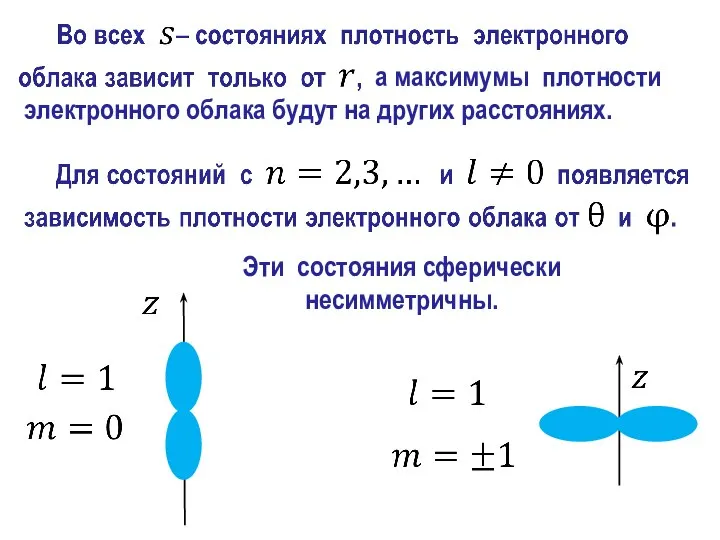
- 30. а максимумы плотности облака будут расположены на других расстояниях. Заключение Эти состояния сферически несимметричны.
- 32. Задание на самоподготовку Повторить тему лекции с использованием конспекта и рекомендованной литературы. Ответить на контрольные вопросы
- 34. Скачать презентацию



















 Презентация на тему Биография Нильса Бора
Презентация на тему Биография Нильса Бора  Драйвер двигателя постоянного тока. Вспомогательные функции
Драйвер двигателя постоянного тока. Вспомогательные функции Тема 7. Действия в условиях негативных и опасных факторов бытового характера
Тема 7. Действия в условиях негативных и опасных факторов бытового характера Физические величины и их измерения. Урок 2. 7 класс
Физические величины и их измерения. Урок 2. 7 класс Законы распространения света
Законы распространения света История создания швейных машин. Виды машин. Устройство швейной машины
История создания швейных машин. Виды машин. Устройство швейной машины 28,09 7АБ физика
28,09 7АБ физика Презентация на тему Шкала Бофорта
Презентация на тему Шкала Бофорта  Динамика моря и Условия судоходства
Динамика моря и Условия судоходства Параллельное соединение проводников
Параллельное соединение проводников Дисперсия света. Опыт И. Ньютона
Дисперсия света. Опыт И. Ньютона Из чего состоит велосипед
Из чего состоит велосипед Радиоэлектроника
Радиоэлектроника Робототехника. Научные достижения в робототехнике и ее влияние на нашу жизнь
Робототехника. Научные достижения в робототехнике и ее влияние на нашу жизнь Силы упругости. Закон Гука
Силы упругости. Закон Гука Основное отличие химических явлений от физических?
Основное отличие химических явлений от физических? Источники света
Источники света Urok_8
Urok_8 Презентация на тему Броуновское движение
Презентация на тему Броуновское движение  Стабильность градуировочных графиков, их роль в оценке качества количественного химического анализа
Стабильность градуировочных графиков, их роль в оценке качества количественного химического анализа Линии влияния усилий в фермах
Линии влияния усилий в фермах Основные процессы поглощения энергии фотонов высокоэнергетических эми
Основные процессы поглощения энергии фотонов высокоэнергетических эми Тормозные системы
Тормозные системы Гармонические колебания
Гармонические колебания Испарение и конденсация
Испарение и конденсация Закон збереження енергії
Закон збереження енергії Экскаваторы
Экскаваторы Самоиндукция. Индуктивность
Самоиндукция. Индуктивность