Содержание
- 2. Первое начало термодинамики Теплота Q, подводимая к системе, идёт на изменение ее внутренней энергии ΔU и
- 3. Значение первого закона термодинамики Первое начало термодинамики запрещает создание вечных двигателей, принцип действия которых основан на
- 4. Применение первого закона термодинамики - работа газа при изменении его объёма от V1 до V2 Расчет
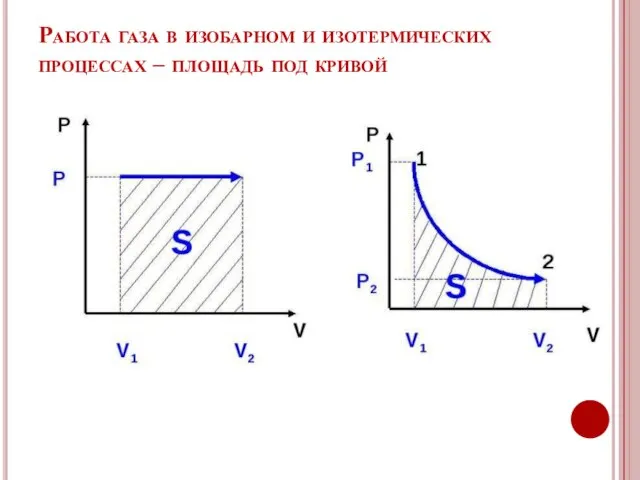
- 5. Работа газа в изобарном и изотермических процессах – площадь под кривой
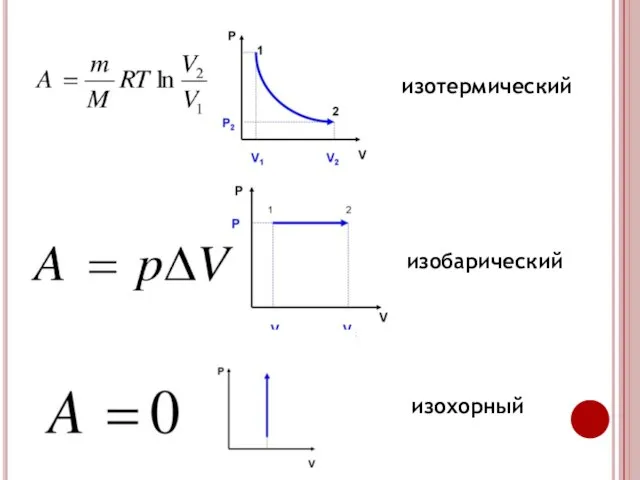
- 6. изотермический изобарический изохорный
- 7. Теплоёмкость тела – количество теплоты, которое требуется, чтобы изменить температуру тела на 1 градус Молярная теплоёмкость
- 9. Теплоёмкость идеального газа Формула Майера: Теплоемкость при постоянном объеме: Теплоемкость при постоянном давлении:
- 10. Адиабатический процесс протекает без теплообмена термодинамической системы с окружающей средой Уравнение Пуассона - уравнение адиабатического процесса
- 11. Адиабатический процесс для одноатомных газов γ = 1,67 для двухатомных газов γ = 1,4 для многоатомных
- 12. Примеры адиабатных процессов в природе Образование облаков и осадков – дождя, снега, града
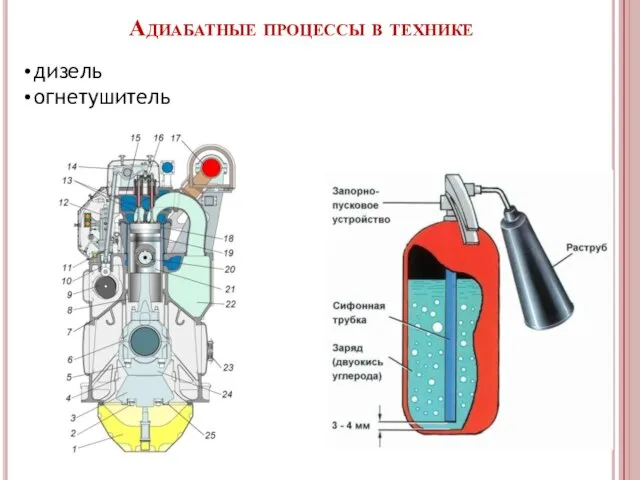
- 13. Адиабатные процессы в технике дизель огнетушитель
- 15. Скачать презентацию









 Теория автоматического управления. Типовые звенья
Теория автоматического управления. Типовые звенья Теоретическая механика. Динамика. Основные понятия и законы динамики
Теоретическая механика. Динамика. Основные понятия и законы динамики Изделие и техническая информация о нем
Изделие и техническая информация о нем Энергосбережение. Исследовательская работа
Энергосбережение. Исследовательская работа Тёмная материя и космология
Тёмная материя и космология Электрическое поле. Лекция № 1
Электрическое поле. Лекция № 1 Теория деформаций. Практическое занятие
Теория деформаций. Практическое занятие Ветровой электрогенератор challenergy
Ветровой электрогенератор challenergy Энергия топлива. Удельная теплота сгорания
Энергия топлива. Удельная теплота сгорания Отражение и преломление. Световые явления
Отражение и преломление. Световые явления Тайна воды, которую мы прием
Тайна воды, которую мы прием Кипение. Парообразование
Кипение. Парообразование Критерии оценки подвески
Критерии оценки подвески Рентгеновские лучи
Рентгеновские лучи Тяга. Ма́ятник
Тяга. Ма́ятник Движение небесных тел под действием сил тяготения
Движение небесных тел под действием сил тяготения Законы постоянного тока
Законы постоянного тока Презентация на тему Электрическая цепь
Презентация на тему Электрическая цепь  Законы сохранения в механике. Часть 3. Подготовка к ЕГЭ
Законы сохранения в механике. Часть 3. Подготовка к ЕГЭ Применение УФЛ
Применение УФЛ Магнитные поля
Магнитные поля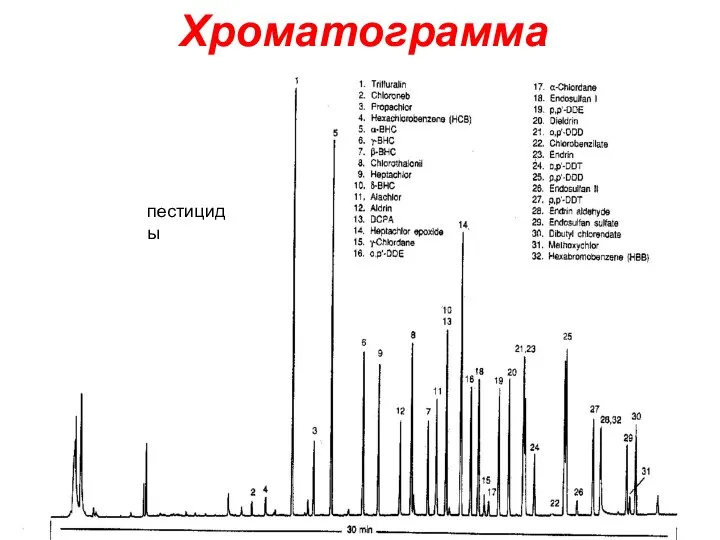 Хроматограмма пестициды
Хроматограмма пестициды Отражение света
Отражение света Основи спектроскопії. Характеристика і діапазони електромагнітного випромінювання
Основи спектроскопії. Характеристика і діапазони електромагнітного випромінювання Почему луна не падает на землю
Почему луна не падает на землю Презентация на тему Механическое движение понятие
Презентация на тему Механическое движение понятие  Инерциальная система отсчета
Инерциальная система отсчета Физические величины. Измерение физических величин. Точность и погрешность измерений
Физические величины. Измерение физических величин. Точность и погрешность измерений