Содержание
- 2. Цель урока: актуализировать знания студентов о распространении, свойствах воды, об экологических проблемах, связанных с загрязнением и
- 3. План урока: Распространение воды Физические свойства воды Строение молекулы воды Химические свойства воды Круговорот воды в
- 4. 1. Распространение воды - распространение воды на Земле - вода в живом организме
- 5. Распространение воды на Земле Вода - это самый распространенный на Земле минерал Почти ¾ поверхности земного
- 6. Вода в организме человека Без воды человек может прожить только 3 дня, в то время как
- 7. Жидкой водой наполнен Мировой океан, поверхностные воды суши и подземные воды Твердый лед можно увидеть и
- 8. 3. Строение молекулы воды Н2О М=18г/моль массовые доли элементов в воде. W (Н) = 11% W(О)
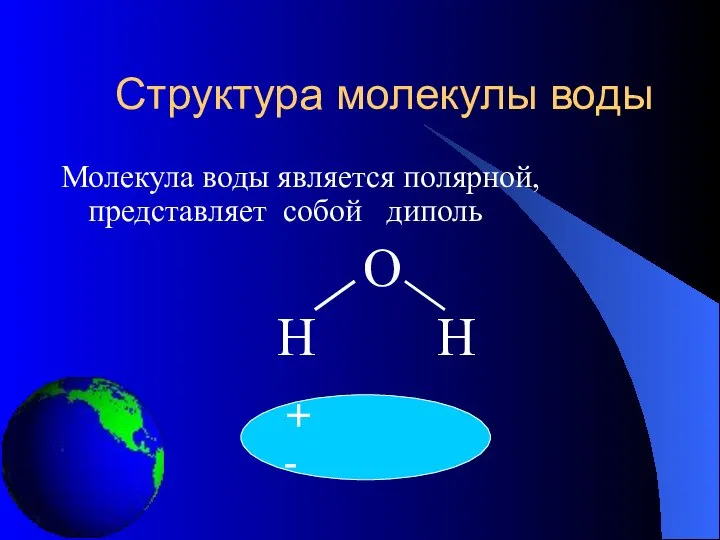
- 9. Структура молекулы воды Молекула воды является полярной, представляет собой диполь О Н Н + -
- 10. По отношению к воде вещества делятся на: - Растворимые - Нерастворимые - Малорастворимые Задание №1 Пользуясь
- 11. Вода – одно из наиболее реакционно – способных веществ. + кислотный оксид = кислота 1.Вода +
- 12. Задание №2 Закончите уранения реакций. SO3 + H2O = SiO2 + H2O = CaO + H2O
- 13. Вода - как окислитель: 2.Взаимодействует с активными (щелочными и щелочноземельными металлами) Na + Н2О = ?
- 14. Вода - как восстановитель 3.Взаимодействует с таким окислителем как фтор (вода горит во фторе). 2 F2
- 15. При t= 2000°C или при пропускании электрического тока вода разлагается на простые вещества – кислород и
- 16. Минута психологической разгрузки. Составление синквейна в рабочих тетрадях. Синквейн будет состоять из 5 строк. Одним словом
- 17. 5. Круговорот воды в природе. Запасы воды остаются неизменными в течение миллиардов лет, т.к. вода совершает
- 18. 6. Охрана водных ресурсов. Природная вода не бывает совершенно чистой, она содержит примеси: растворимые и нерастворимые
- 19. Анализ качества водопроводной воды Определить степень прозрачности Для определения степени прозрачности наберите полный прозрачный стакан воды.
- 20. 2. Цветность воды Определяют аналогичным образом: налейте 100 мл воды в прозрачный стакан и рассмотрите его
- 21. Жесткость воды В домашних условиях жесткость воды легко определить с помощью мыла или геля для душа.
- 22. Запах воды Запах воды также может многое рассказать о ее чистоте. Сначала погрейте воду до 20°С,
- 23. Вкус воды
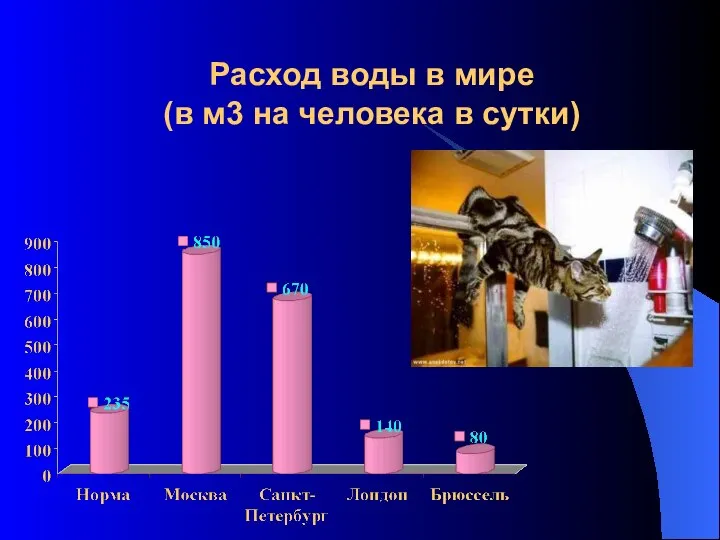
- 24. Расход воды в мире (в м3 на человека в сутки)
- 25. Ответы теста Вариант -1 Вариант -2 2, 3, 2, 4, 4 2, 2, 4, 3, 2
- 26. Выводы: Вода – самое распространенное вещество на Земле. Вода встречается в природе во всех трёх агрегатных
- 27. Рефлексия 3 балла 4 балла 5 баллов
- 29. Скачать презентацию
























 Презентация на тему Достопримечательности г. Омска
Презентация на тему Достопримечательности г. Омска  Пляж с. Тарказы
Пляж с. Тарказы 20140313_prezentatsiya_6_kl_poyasa_osveshchennosti2
20140313_prezentatsiya_6_kl_poyasa_osveshchennosti2 Презентация на тему Волны в океане
Презентация на тему Волны в океане  Особенности океанов
Особенности океанов Отдохни на Урале. Урал для детских групп
Отдохни на Урале. Урал для детских групп Петрова и др_20220405_Io8
Петрова и др_20220405_Io8 Географическая викторина
Географическая викторина Презентация на тему Венгрия
Презентация на тему Венгрия  Секция географии Туманы в Оренбургской области
Секция географии Туманы в Оренбургской области Проверочная работа по теме «Культура Востока»
Проверочная работа по теме «Культура Востока» Природа Океании (1)
Природа Океании (1) Государство на крайнем юго-западе Европы Испания
Государство на крайнем юго-западе Европы Испания История открытия Африки
История открытия Африки Напряжения в грунтах
Напряжения в грунтах Путешествие в в королевство Бифихигео
Путешествие в в королевство Бифихигео Озоновые дыры
Озоновые дыры Презентация на тему Проблемы мирового океана (10 класс)
Презентация на тему Проблемы мирового океана (10 класс)  Озеро Байкал
Озеро Байкал Дьяковский овраг. Точное местоположение оврага
Дьяковский овраг. Точное местоположение оврага Общие сведения по геологии
Общие сведения по геологии מגלי עולם
מגלי עולם Викторина Мой край родной – Башкортостан
Викторина Мой край родной – Башкортостан Страна Топонимия. Земля уральская
Страна Топонимия. Земля уральская Поволжский Район
Поволжский Район Великие путешественники
Великие путешественники Калтанский разрез
Калтанский разрез Биосфера
Биосфера