Содержание
- 2. ЦЕЛИ УРОКА: Цели урока: Формирование знаний о комплексных соединениях; Рассмотрение химических свойства комплексных соединений; Углубление знаний
- 3. Комплексные называют соединения, содержащие сложные ионы и молекулы, способные к существованию, как в кристаллическом виде, так
- 4. Швейцарский химик Альфред Вернер, лауреат Нобелевской премии. Его научная деятельность проходила в Цюрихском университете. Ученый синтезировал
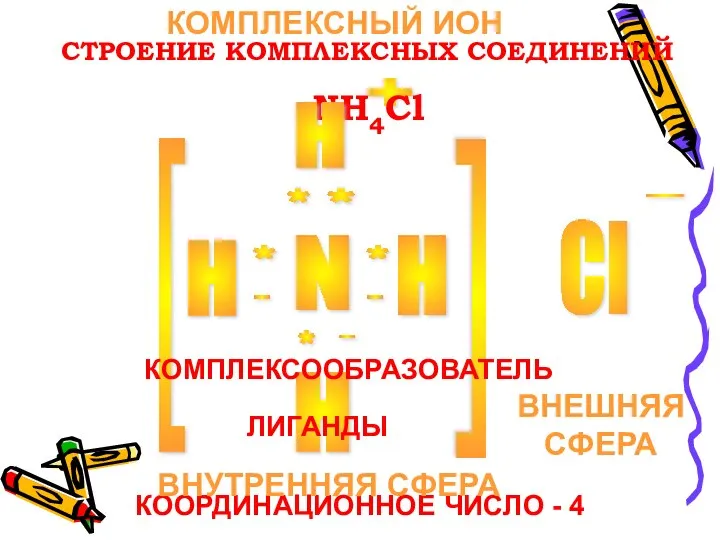
- 5. СТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ N H H H Cl + - [ [ * * * *
- 6. [N-3H+14]Cl-1 КОМПЛЕКСНЫЙ ИОН [NH4]+ ВНУТРЕННЯЯ СФЕРА: КОМПЛЕКСООБРАЗОВАТЕЛЬ N-3 ЛИГАНДЫ H+ ВНЕШНЯЯ СФЕРА АНИОН Cl-
- 7. Лигандами могут быть: а) полярные молекулы: NH3 H2O CO NO б) простые ионы CI- Br- I-
- 8. (OH)- 4 [Zn+x Na+ (+1) + x + (-1) ] 2 ·2 ·4 = 0 x
- 9. НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ 2- 4- 3- 5- 6- ди- три- тетра- пента- гекса- ЧИСЛИТЕЛЬНЫЕ: НАЗВАНИЯ ЛИГАНДОВ:
- 10. НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ НАЗВАНИЯ КАТИОНОВ: Fe - феррат Cu - купрат Ag - аргентат Au -
- 11. тетра гидроксо цинкат НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2 4] (OH)- [Zn+2 натрия [Cr+3 (H2O)0 6] Cl-3 хлорид
- 12. НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na3[AlF6] Na[Al(OH)4] K4[Fe(CN)6] Гексафтороалюминат натрия Тетрагидроксоалюминат натрия Гексационоферрат (II) калия
- 13. ХИМИЧЕСКИЕ СВОЙСТВА 1. Диссоциация комплексных соединений. [Cu(NH3)4](OH)2. = [Cu(NH3)4]2++2ОН-. [Cu(NH3)4]2+ ↔ Cu2++ 4NH3
- 14. Химические свойства 2. Комплексные соединения взаимодействуют с оксидом углерода (IV): Na[AL(OH) 4] + CO2 = AL(OH)
- 15. Химические свойства 3. Комплексные соединения взаимодействуют с кислотами: [Cu(NH3)4]SO4 + BaCl2 = BaSO4 + [Cu(NH3)4]Cl2 FeCl3
- 16. Химические свойства 4. Комплексные соединения взаимодействуют с солями – реакции обмена: Na[AL(OH) 4] + ALCL3 =
- 17. Химические свойства 5 .Комплексные соединения вступают в окислительно-восстановительные реакции: K3[Fe3+(CN)6]3 + H2O2 + 2KOH = 2K4[Fe2+(CN)6]4
- 19. Скачать презентацию



![[N-3H+14]Cl-1 КОМПЛЕКСНЫЙ ИОН [NH4]+ ВНУТРЕННЯЯ СФЕРА: КОМПЛЕКСООБРАЗОВАТЕЛЬ N-3 ЛИГАНДЫ H+ ВНЕШНЯЯ СФЕРА АНИОН Cl-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-5.jpg)

![(OH)- 4 [Zn+x Na+ (+1) + x + (-1) ] 2 ·2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-7.jpg)


![тетра гидроксо цинкат НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙ Na+2 4] (OH)- [Zn+2 натрия [Cr+3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-10.jpg)
![НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Na3[AlF6] Na[Al(OH)4] K4[Fe(CN)6] Гексафтороалюминат натрия Тетрагидроксоалюминат натрия Гексационоферрат (II) калия](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-11.jpg)
2. = [Cu(NH3)4]2++2ОН-. [Cu(NH3)4]2+ ↔ Cu2++ 4NH3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-12.jpg)
![Химические свойства 2. Комплексные соединения взаимодействуют с оксидом углерода (IV): Na[AL(OH) 4]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-13.jpg)
![Химические свойства 3. Комплексные соединения взаимодействуют с кислотами: [Cu(NH3)4]SO4 + BaCl2 =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-14.jpg)

![Химические свойства 5 .Комплексные соединения вступают в окислительно-восстановительные реакции: K3[Fe3+(CN)6]3 + H2O2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1054365/slide-16.jpg)
 Иван Суриков. Стихотворение Зима
Иван Суриков. Стихотворение Зима Анализ сказки М. Е. Салтыкова - Щедрина Дикий помещик
Анализ сказки М. Е. Салтыкова - Щедрина Дикий помещик Георгий Васильевич Чичерин
Георгий Васильевич Чичерин Работа с текстом художественного произведения
Работа с текстом художественного произведения Волшебник Дед Мороз. Новогодняя сказка
Волшебник Дед Мороз. Новогодняя сказка Джонни Депп
Джонни Депп Пословицы и поговорки Владимира Ивановича Даля
Пословицы и поговорки Владимира Ивановича Даля Максим Горький. Биография
Максим Горький. Биография Сочинение по роману в стихах Евгений Онегин А. С. Пушкина
Сочинение по роману в стихах Евгений Онегин А. С. Пушкина Биография Некрасова. Ярославская гимназия
Биография Некрасова. Ярославская гимназия Маяковский
Маяковский Презентация на тему Сергей Есенин
Презентация на тему Сергей Есенин  Теория Р. Раскольникова. Ф.М. Достоевский Преступление и наказание
Теория Р. Раскольникова. Ф.М. Достоевский Преступление и наказание Знаток народной жизни. К 200-летию Николая Некрасова
Знаток народной жизни. К 200-летию Николая Некрасова Биография Дмитрия Ивановича Менделеева. История открытия периодического закона
Биография Дмитрия Ивановича Менделеева. История открытия периодического закона Презентация на тему Бунин
Презентация на тему Бунин  Презентация на тему Двухсотлетию победы в Отечественной войне 1812 года
Презентация на тему Двухсотлетию победы в Отечественной войне 1812 года  Презентация на тему Дары волхвов
Презентация на тему Дары волхвов  Михаил Васильевич Ломоносов. Сборник карт по географии
Михаил Васильевич Ломоносов. Сборник карт по географии Антон Павлович Чехов. Тест
Антон Павлович Чехов. Тест К 100 – летию Жана Александровича Зимина
К 100 – летию Жана Александровича Зимина Литература и искусство, их влияние на развитие духовного мира населения страны
Литература и искусство, их влияние на развитие духовного мира населения страны Monsters, Inc. Read-Along
Monsters, Inc. Read-Along Презентация на тему "М. А. Шолохов «Донские рассказы»" - презентации по Литературе
Презентация на тему "М. А. Шолохов «Донские рассказы»" - презентации по Литературе Что ценнее- «серебро» или «золото» русской поэзии? Коротаева Н.В. МБОУ Туголуковская СОШ Жердевского района
Что ценнее- «серебро» или «золото» русской поэзии? Коротаева Н.В. МБОУ Туголуковская СОШ Жердевского района Биография Н. Носова
Биография Н. Носова Библиографический калейдоскоп. Игра для 5 классов
Библиографический калейдоскоп. Игра для 5 классов Звёзды мировой оперной сцены
Звёзды мировой оперной сцены