Содержание
- 2. Безопасность в химической лаборатории; Правила хранения веществ; Назначение химической посуды и оборудования; Химия в быту; Химия
- 3. 1) Все опыты с любыми растворами кислот и щелочей следует проводить в резиновых перчатках. 2) При
- 4. 5) Опыты с горючими и едкими веществами необходимо проводить в очках — собственных или лабораторных. I.
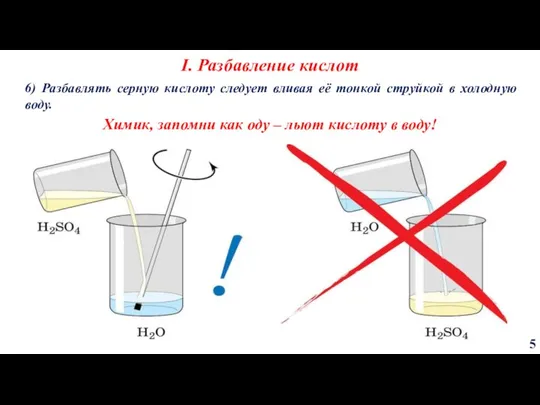
- 5. 6) Разбавлять серную кислоту следует вливая её тонкой струйкой в холодную воду. I. Разбавление кислот 5
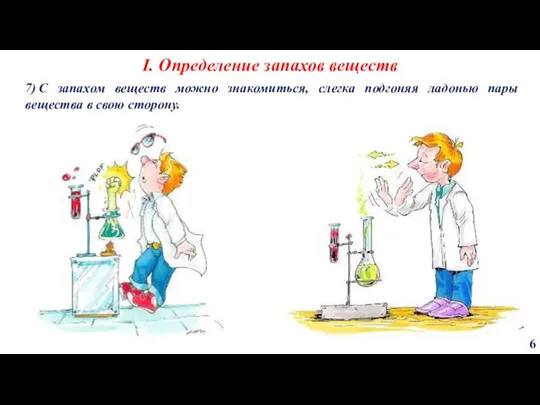
- 6. 7) C запахом веществ можно знакомиться, слегка подгоняя ладонью пары вещества в свою сторону. I. Определение
- 7. 9) Хлор (и другие летучие ядовитые вещества) получают в вытяжном шкафу. I. Получение газообразных веществ 7
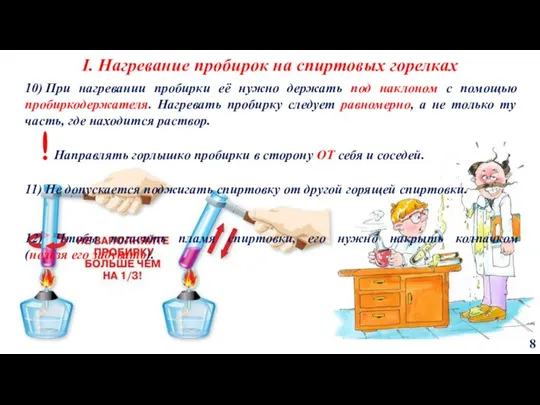
- 8. I. Нагревание пробирок на спиртовых горелках 8 10) При нагревании пробирки её нужно держать под наклоном
- 9. I. Отбор и добавление реактивов 9 13) Отбор реактивов нужно осуществлять с помощью пипетки.
- 10. I. Еда и лаборатория несовместимы! 10 14) Вещества, находящиеся в лаборатории, запрещается пробовать на вкус, даже
- 11. II. Правила хранения веществ 11 1) Все склянки и ёмкости, содержащие химические вещества, должны иметь этикетки
- 12. II. Правила хранения веществ 12 4) Для приготовления растворов кислот в химической лаборатории не следует брать
- 13. III. Назначение посуды и оборудования 13 1) В мензурке можно нагревать воду. Мерные стаканы, мензурки и
- 14. III. Назначение посуды и оборудования 14 2) Для измерения объёма жидкости используют пробирку. 3) Для пересыпания
- 15. III. Назначение посуды и оборудования 15 5) Для выпаривания раствора можно использовать фарфоровую ступку. 6) Воду
- 16. III А. Аппарат Киппа 16 Аппарат Киппа – прибор для получения газов действием растворов кислот и
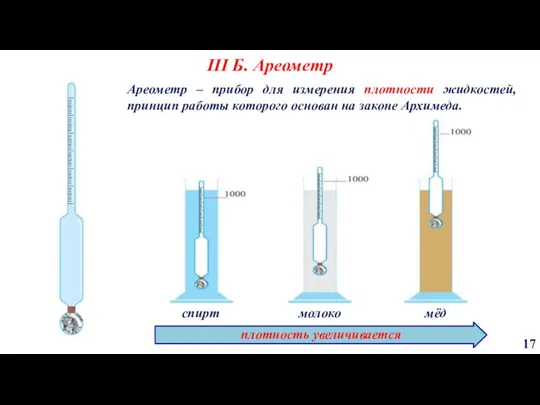
- 17. III Б. Ареометр 17 Ареометр – прибор для измерения плотности жидкостей, принцип работы которого основан на
- 18. III В. Калориметр 18 Калори́метр – прибор для измерения количества теплоты, выделяющейся или поглощающейся в каком-либо
- 19. IV. Химия в быту 19 1) Разбитый ртутный термометр и вытекшую из него ртуть следует выбросить
- 20. IV. Химия в быту 20 2) Красками, содержащими ионы свинца, не рекомендуется покрывать детские игрушки и
- 21. IV. Химия в быту 21 8) Водопроводная вода содержит примеси растворимых солей – сульфатов и гидрокарбонатов.
- 22. V. Химия в экологии 22 1) НЕ рекомендуется употреблять в пищу плодоовощные культуры, выращенные вблизи железных
- 23. V. Химия в экологии 23 6) Морская вода обладает большей плотностью, чем речная, так как содержит
- 24. VI. Физические и химические явления 24 Явления, при которых из одних веществ образуются другие, отличающиеся от
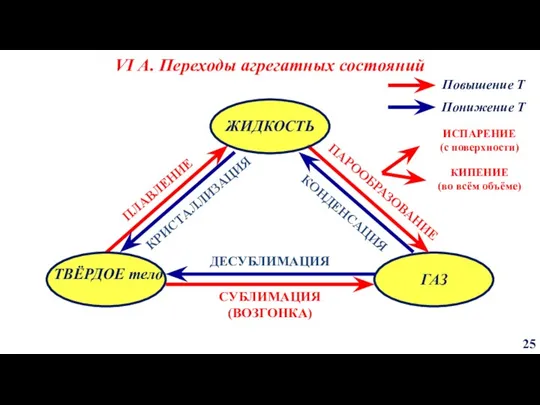
- 25. VI А. Переходы агрегатных состояний 25 ИСПАРЕНИЕ (с поверхности) КИПЕНИЕ (во всём объёме)
- 26. VII. Индивидуальное вещество или смесь 26 Несколько вещество; Непостоянный состав (разное соотношение компонентов); Непостоянные физические свойства
- 27. VIII. Смеси однородные и неоднородные 27 В общем объёме смеси частицы распределены друг в друге неравномерно
- 28. IX. Разделение смесей 28 ВЫПАРИВАНИЕ; КРИСТАЛЛИЗАЦИЯ; ДИСТИЛЛЯЦИЯ (ПЕРЕГОНКА); ХРОМАТОГРАФИЯ. ФИЛЬТРОВАНИЕ; ОТСТАИВАНИЕ и ДЕКАНТАЦИЯ; МАГНИТНАЯ СЕПАРАЦИЯ. Это
- 29. IX А. Разделение гетерогенных смесей 29 1) ФИЛЬТРОВАНИЕ – отделение твёрдых частиц от жидкостей или газов
- 30. IX А. Разделение гетерогенных смесей 30 ДЕКАНТАЦИЯ – отделение двух несмешивающихся жидкостей, путём сливания более плотной
- 31. IX А. Разделение гетерогенных смесей 31 3) МАГНИТНАЯ СЕПАРАЦИЯ – разделение смеси за счёт способности одного
- 32. IX Б. Разделение гомогенных смесей 32 1) ВЫПАРИВАНИЕ – выделение твёрдого вещества из раствора путём нагревания,
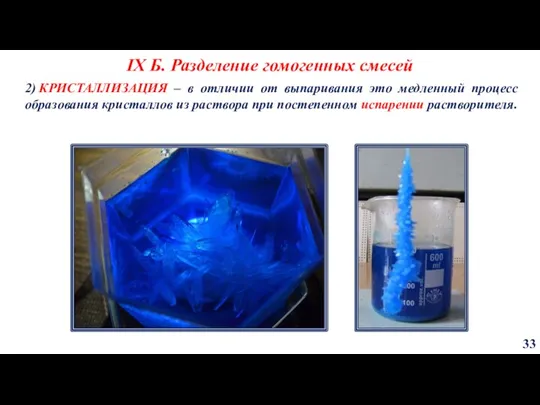
- 33. IX Б. Разделение гомогенных смесей 33 2) КРИСТАЛЛИЗАЦИЯ – в отличии от выпаривания это медленный процесс
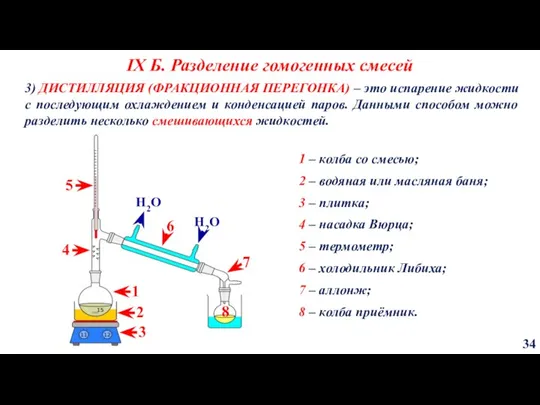
- 34. IX Б. Разделение гомогенных смесей 34 3) ДИСТИЛЛЯЦИЯ (ФРАКЦИОННАЯ ПЕРЕГОНКА) – это испарение жидкости с последующим
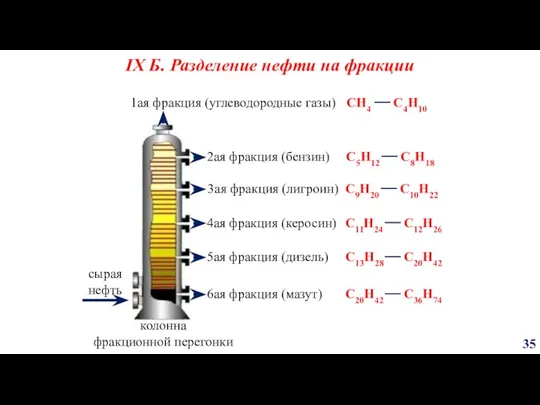
- 35. колонна фракционной перегонки сырая нефть 1ая фракция (углеводородные газы) 2ая фракция (бензин) 5ая фракция (дизель) 4ая
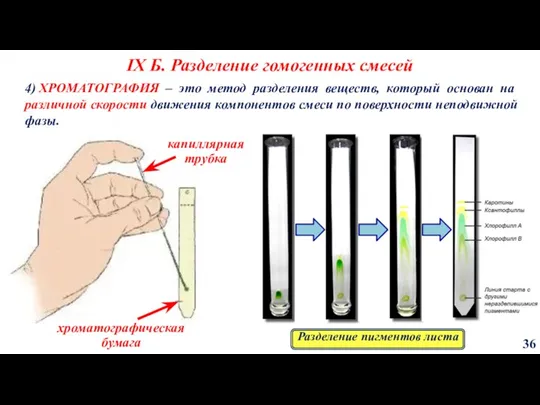
- 36. IX Б. Разделение гомогенных смесей 36 4) ХРОМАТОГРАФИЯ – это метод разделения веществ, который основан на
- 37. Подпишись на мой канал!
- 39. Скачать презентацию



























 Производственные травмы
Производственные травмы Видеонаблюдение в детских садах
Видеонаблюдение в детских садах Я здоровье берегу – сам себе я помогу
Я здоровье берегу – сам себе я помогу Основы здорового образа жизни
Основы здорового образа жизни Гигиена сердечно-сосудистой системы. Первая помощь при кровотечениях
Гигиена сердечно-сосудистой системы. Первая помощь при кровотечениях Презентация на тему Влияние человека на экосистему
Презентация на тему Влияние человека на экосистему  РСЧС
РСЧС 66839feaa0bdacb550817a9dd40091a2
66839feaa0bdacb550817a9dd40091a2 Руководящие документы
Руководящие документы Что делать, если ты порезался? Элементарное представление о помощи
Что делать, если ты порезался? Элементарное представление о помощи Первая помощь при кровотечениях
Первая помощь при кровотечениях Природные бедствия и техногенные катастрофы. Обязанности спасателей
Природные бедствия и техногенные катастрофы. Обязанности спасателей Правила поведения в школе
Правила поведения в школе Дорожно-транспортное происшествие
Дорожно-транспортное происшествие тест Общие положения
тест Общие положения Мир вокруг нас. Наша безопасность. Занятие 2. 3 класс
Мир вокруг нас. Наша безопасность. Занятие 2. 3 класс Презентация на тему Организация дорожного движения. Обязанности пешеходов и пассажиров
Презентация на тему Организация дорожного движения. Обязанности пешеходов и пассажиров  ВПР география 6 класс
ВПР география 6 класс Кроссворд по правилам дорожного движения
Кроссворд по правилам дорожного движения Шоколад: вред и польза
Шоколад: вред и польза Фликеры и безопасность детей на дороге
Фликеры и безопасность детей на дороге Правила пожарной безопасности для детей для дошкольного возраста
Правила пожарной безопасности для детей для дошкольного возраста Координация и регуляция. Влияние алкоголя, курения и других наркотических веществ на работу нервной системы
Координация и регуляция. Влияние алкоголя, курения и других наркотических веществ на работу нервной системы Презентация на тему Заповедники Казахстана
Презентация на тему Заповедники Казахстана  Электронные системы управления
Электронные системы управления Молодёжь выбирает жизнь без наркотиков
Молодёжь выбирает жизнь без наркотиков Правила дорожного движения. Правила жизни
Правила дорожного движения. Правила жизни Безопасность на ЖД
Безопасность на ЖД