Содержание
- 2. Аммиак может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке караванных
- 3. По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех
- 4. Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый -
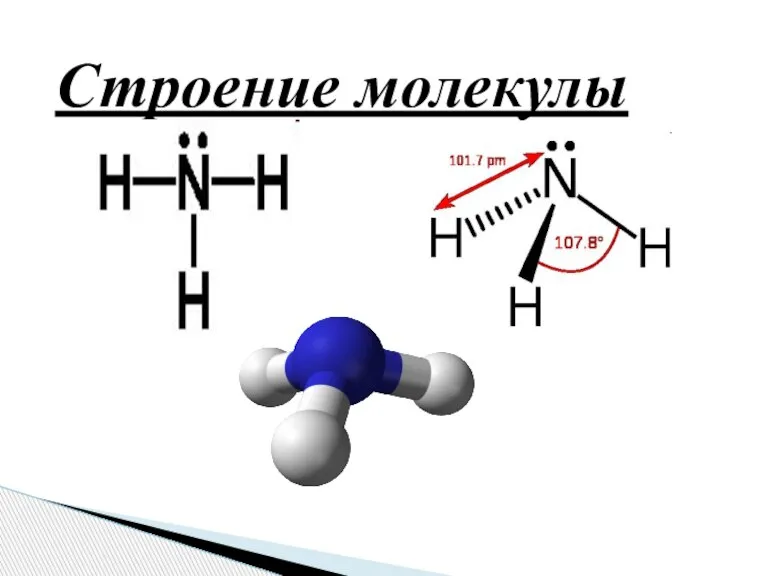
- 5. Строение молекулы
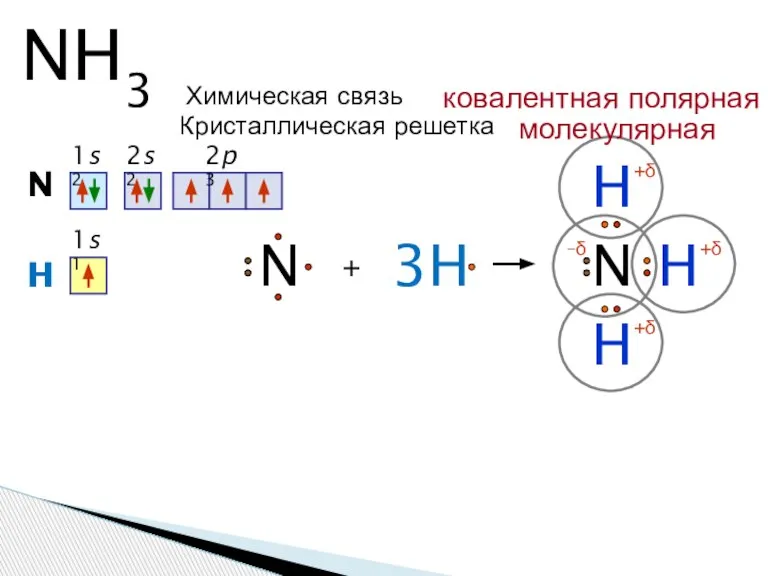
- 6. NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ
- 7. Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота
- 8. Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха
- 9. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных вызвать токсический
- 10. Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl +
- 11. Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г)
- 12. Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления);
- 13. Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0→ N+2 NH3-сильный восстановитель
- 14. с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление амииака
- 15. с оксидами металлов 2NH3 +3CuO =3Cu + N2 +3H2O
- 16. с сильными окислителями 2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
- 17. Реакции без изменения степени окисления атома азота (присоединение - образование иона аммония NH4+ по донорно-акцепторному механизму
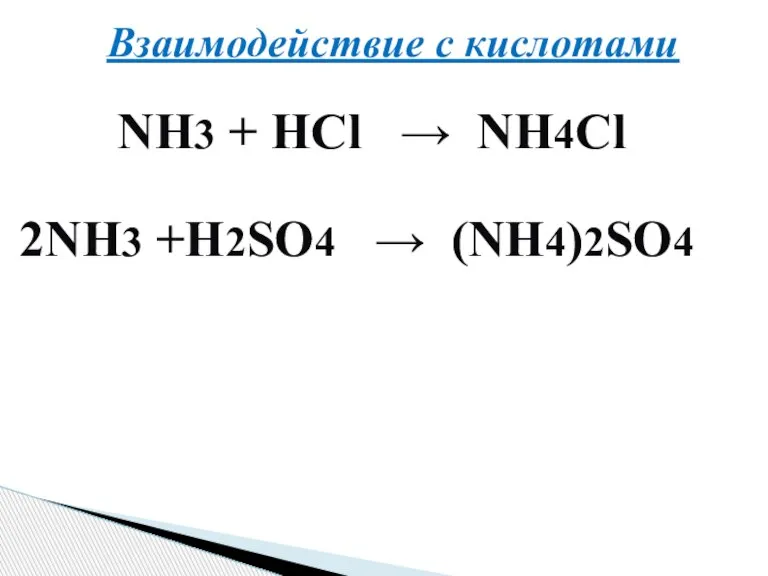
- 18. Взаимодействие с кислотами NH3 + HCl → NH4Cl 2NH3 +H2SO4 → (NH4)2SO4
- 19. Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как
- 20. Применение аммиака Производство пластмасс и волокон 2. В составе моющих средств
- 21. 3. Производство азотных удобрений 4. В сельском хозяйстве
- 22. 5. Производство азотной кислоты 6. Получение взрывчатых веществ
- 23. 7. В медицине
- 24. По объемам производства аммиак занимает одно из первых мест; ежегодно во всем мире получают около 100
- 26. Скачать презентацию




















 Обеспечение двигательной активности учащихся средствами физической культуры
Обеспечение двигательной активности учащихся средствами физической культуры Деньги и финансовые институты
Деньги и финансовые институты 20140511_urok_evraziya
20140511_urok_evraziya Презентация на тему Умножение многозначного числа на двузначное число
Презентация на тему Умножение многозначного числа на двузначное число  Окно Овертона, как технология социального изменения
Окно Овертона, как технология социального изменения Боровичский край
Боровичский край Тема урока «АЛГОРИТМЫ»
Тема урока «АЛГОРИТМЫ» Эмоциональное состояние личности
Эмоциональное состояние личности Дегтебетон. Классификация дегтебетона
Дегтебетон. Классификация дегтебетона Культурные традиции народов Европы. 11 класс
Культурные традиции народов Европы. 11 класс 1 сентября - День знаний
1 сентября - День знаний Древняя Русь
Древняя Русь Мексиканский медичи. Евгенио Лопез Алоносо
Мексиканский медичи. Евгенио Лопез Алоносо Способы очистки питьевой воды
Способы очистки питьевой воды Модель
Модель МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕДОШКОЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «ДЕТСКИЙ САД № 47 «ЗЕЛЕНЫЙ ОГОНЕК» КОМПЕНСИРУЮЩЕГО ВИДА» г. Север
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕДОШКОЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «ДЕТСКИЙ САД № 47 «ЗЕЛЕНЫЙ ОГОНЕК» КОМПЕНСИРУЮЩЕГО ВИДА» г. Север Курсовое проектирование
Курсовое проектирование Основы дизайн-проектирования. Геометрические построения как способ гармонизации. Работы учащихся
Основы дизайн-проектирования. Геометрические построения как способ гармонизации. Работы учащихся Г.Р. Державин
Г.Р. Державин Отдел продаж ОТК
Отдел продаж ОТК Школа Саммерхилл. Великобритания, Лейстон
Школа Саммерхилл. Великобритания, Лейстон Компьютерная графика
Компьютерная графика Великая цель образования – это не знания, а действия. Герберт Спенсер
Великая цель образования – это не знания, а действия. Герберт Спенсер Выбор профессии
Выбор профессии Семья Ермолаевых
Семья Ермолаевых Бизнес-проект на тему: Игровое будущее
Бизнес-проект на тему: Игровое будущее World informational sources. Advertising
World informational sources. Advertising Снег и лёд в поэзии, пословицах, поговорках.Веселая викторина
Снег и лёд в поэзии, пословицах, поговорках.Веселая викторина