Слайд 2Основные вопросы
Строение молекулы азотной кислоты.
Физические свойства.
Получение азотной кислоты.
Химические свойства.
Свойства нитратов.
Применение азотной кислоты

и нитратов.
Слайд 4Физические свойства
Дымящаяся жидкость, ρ=1,52 г/мл, безцветная, едкий запах, Ткип=82,6ºС Т=-42ºС - прозрачные

кристаллы, очень гигроскопична
Сильный окислитель. Разрушает животные и растительные ткани
Слайд 5Получение HNO3
В лаборатории NaNO3(ТВ.)+H2SO4(КОНЦ)=NaHSO4 + HNO3↑
В промышлености 4NH3 + 5O2 =
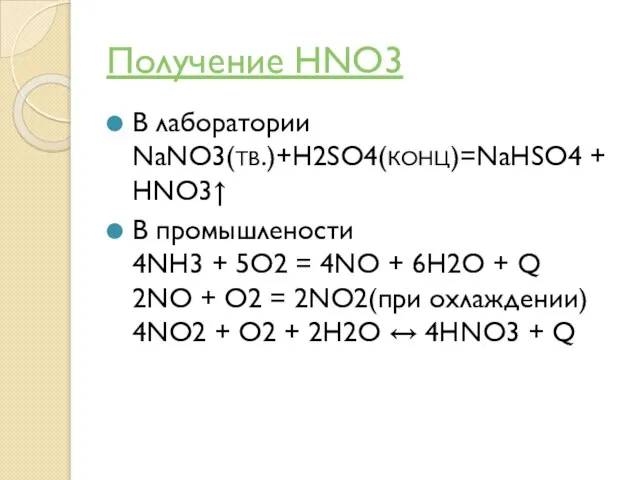
4NO + 6H2O + Q 2NO + O2 = 2NO2(при охлаждении) 4NO2 + O2 + 2H2O ↔ 4HNO3 + Q
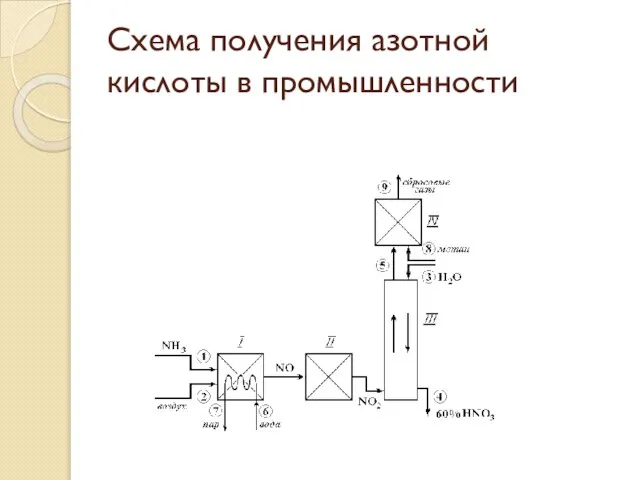
Слайд 6Схема получения азотной кислоты в промышленности
Слайд 7Химические свойства
Азотная кислота является сильным окислителем, концентрированная азотная кислота окисляет серу до

серной, а фосфор - до фосфорной кислот, некоторые органические соединения (например амины и гидразины, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Слайд 8Свойства общие с другими кислотами
Составьте уравнения реакций
HNO3 + Mg(OH)2 =
HNO3 +

Al2O3 =
HNO3 + (NH4)2CO3 =
Слайд 9Проверьте уравнения
2HNO3 + Mg(OH)2 = Mg(NO3)2 + 2H2O (реакция нейтрализации)
6HNO3 + Al2O3

= 2Al(NO3)3 + 3H2O (реакция обмена)
2HNO3 + (NH4)2CO3 = 2NH4NO3 + CO2î + H2O (реакция обмена)
Слайд 11Лабораторный эксперимент № 1
В пробирку с концентрированной азотной кислотой осторожно добавляйте

несколько тонких кусочков медной проволоки. Реакция идёт без нагревания, учащиеся наблюдают изменение цвета раствора и выделение красно-бурого газа NO2
Составьте уравнение происходящей реакции
Слайд 12Проверьте себя
Cu + HNO3 (КОНЦ.) = Сu(NO3)2 + NO2 + H2O
Слайд 13Лабораторный эксперимент № 2
В пробирку с разбавленной азотной кислотой осторожно добавляйте

несколько тонких кусочков медной проволоки. Реакция идёт при нагревании. Наблюдайте изменение цвета раствора и выделение бесцветного газа NO
Составьте уравнение происходящей реакции
Слайд 14Проверьте себя
Cu + HNO3(разб.) = Cu(NO3)2 + NO + H2O
0 +1

Cu – 2e = Cu 3 восстановитель окисляется
+5 +2
N + 3e = N 2окислитель восстанавливается 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
Слайд 15Подведение итогов
Каковы физические свойства азотной кислоты?
Почему азотную кислоту хранят в склянках из

тёмного стекла?
Почему азотную кислоту используют для получения взрывчатых веществ?
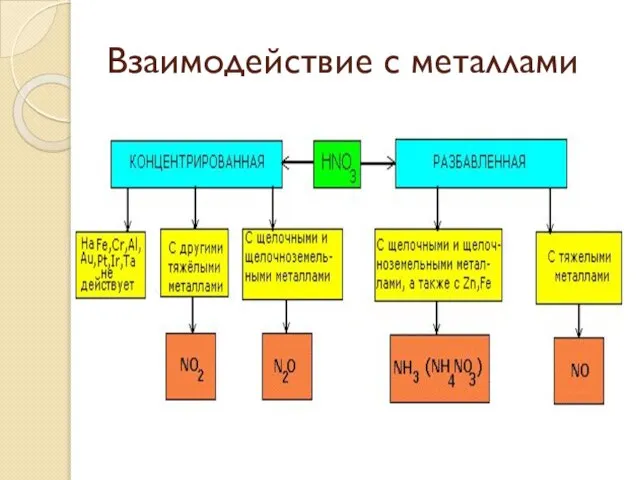
Перечислите особенности взаимодействия азотной кислоты с металлами.
С какими металлами не реагирует азотная кислота?












 Красноярская ТЭЦ-3
Красноярская ТЭЦ-3 15 – среднее количество жалоб Информация о количестве поступивших жалоб по комплексу потребительского рынка и услуг, поступивших
15 – среднее количество жалоб Информация о количестве поступивших жалоб по комплексу потребительского рынка и услуг, поступивших  Воинские звания
Воинские звания Управление сроками производства. Планирование загрузки производственных мощностей
Управление сроками производства. Планирование загрузки производственных мощностей Рецепты здорового питания
Рецепты здорового питания Транспортная логистика
Транспортная логистика Выдающие спортсмены
Выдающие спортсмены ПЕДАГОГИЧЕСКИЙ СОВЕТ Развитие учительского потенциала как одно из требований модернизации образования 27.03.12.
ПЕДАГОГИЧЕСКИЙ СОВЕТ Развитие учительского потенциала как одно из требований модернизации образования 27.03.12. 20180213_ns_akva_achilovoy
20180213_ns_akva_achilovoy Искусство Испании XVI - XVII вв
Искусство Испании XVI - XVII вв Функции государства
Функции государства Feelings
Feelings Этапы работы поисковой системы
Этапы работы поисковой системы  Основы социальных коммуникаций. Курсы обучения
Основы социальных коммуникаций. Курсы обучения ОСНОВЫ ГРАФИЧЕСКОГО ДИЗАЙНА В ЦЕЛЯХ СОЗДАНИЯ КОНТЕНТА Создаете
ОСНОВЫ ГРАФИЧЕСКОГО ДИЗАЙНА В ЦЕЛЯХ СОЗДАНИЯ КОНТЕНТА Создаете Новый подход в дизайне швейного изделия
Новый подход в дизайне швейного изделия Правила дорожного движения
Правила дорожного движения 1.Интерпсихическое взаимодействие как обыкновенное чудо. 2.Лонгитюдное исследование поисковой активности учащихся в начальной и о
1.Интерпсихическое взаимодействие как обыкновенное чудо. 2.Лонгитюдное исследование поисковой активности учащихся в начальной и о Ускорение проекта на PHP на примере
Ускорение проекта на PHP на примере Презентация на тему Марийский народный орнамент
Презентация на тему Марийский народный орнамент Один дома. Правила поведения
Один дома. Правила поведения Perfect Conpetition and the supply Curve
Perfect Conpetition and the supply Curve Оправданы ли вложения в технологическое образование? Гудзенко Дмитрий Юрьевич, к.т.н., CPP
Оправданы ли вложения в технологическое образование? Гудзенко Дмитрий Юрьевич, к.т.н., CPP  Министерство транспорта Российской Федерации
Министерство транспорта Российской Федерации Работа над собой ( или как я сбросила 26 кг ) Собственная фотоистория Авт. Маскаева Наталья Экспресс – Версия.
Работа над собой ( или как я сбросила 26 кг ) Собственная фотоистория Авт. Маскаева Наталья Экспресс – Версия. Имя существительное. Обобщение
Имя существительное. Обобщение Наш школьный двор
Наш школьный двор Новое творчество – современное и неординарное искусство наив-примитивизм
Новое творчество – современное и неординарное искусство наив-примитивизм