Содержание
- 2. Структура части С КИМов по химии в 2006 году С1. Окислительно-восстановительные реакции С2. Составление возможных уравнений
- 3. Окислительно-восстановительные реакции Основное правило, которое используется при определении продуктов ОВР: один элемент понижает свою степень окисления,
- 4. Окислительно-восстановительные реакции С1. Используя метод электронного баланса, составьте уравнение реакции: P + HClO3 + ...= HCl
- 5. Окислительно-восстановительные реакции С1. Используя метод электронного баланса, составьте уравнение: Al + K2Cr2O7 + … = …
- 6. Окислительно-восстановительные реакции Примеры окислительно-восстановительных реак-ций в заданиях С1: a) SO2 + K2Cr2O7 + … = K2SO4
- 7. Составление возможных уравнений реакций С2. Даны водные растворы: сульфида натрия, сероводорода, хлорида алюминия и хлора. Напишите
- 8. Составление возможных уравнений реакций С2. Даны водные растворы: гексагидроксоалюмината калия K3[Al(OH)6], хлорида алюминия, сероводорода и гидроксида
- 9. Составление возможных уравнений реакций С2. Даны водные растворы: гексагидроксохромата натрия Na3[Cr(OH)6], хлорида железа (III), сернистого газа
- 10. Составление возможных уравнений реакций C2. Даны водные растворы: гексагидроксоалюмината калия K3[Al(OH)6], хлорида хрома (III), карбоната калия
- 11. Взаимосвязь органических веществ C3. Напишите уравнения реакций, с помощью которых можно осуществить превращения: H2SO4(конц.),t Br2 H2O,
- 12. Взаимосвязь органических веществ C3. Напишите уравнения реакций, с помощью которых можно осуществить превращения: KOH(спирт.), t t,
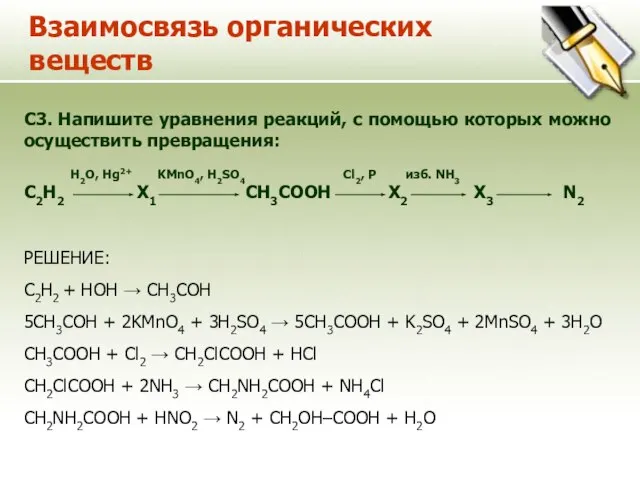
- 13. Взаимосвязь органических веществ C3. Напишите уравнения реакций, с помощью которых можно осуществить превращения: H2O, Hg2+ KMnO4,
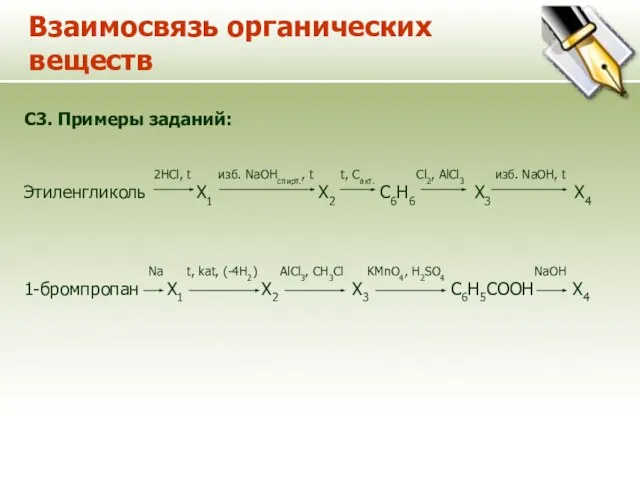
- 14. Взаимосвязь органических веществ C3. Примеры заданий: 2HCl, t изб. NaOHспирт., t t, Cакт. Cl2, AlCl3 изб.
- 15. Расчёты по уравнениям реакций С4. Для окисления некоторого количества серы потребовался такой объем кислорода (н.у.), который
- 16. Расчёты по уравнениям реакций C4. Примеры заданий: а) Для окисления некоторого количества аммиака потребовался такой объём
- 17. Расчёты по теме «Растворы» С4. Смешали 100 мл 15% раствора гидроксида калия (плотностью 1,10 г/мл) и
- 18. Расчёты по теме «Растворы» С4. Примеры заданий: К раствору, полученному при добавлении 8 г гидрида лития
- 19. Задачи на вывод формулы вещества С5. При сгорании газообразного органического вещества, не содержащего кислород, выделилось 2,24
- 21. Скачать презентацию






![Составление возможных уравнений реакций С2. Даны водные растворы: гексагидроксоалюмината калия K3[Al(OH)6], хлорида](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/361865/slide-7.jpg)
![Составление возможных уравнений реакций С2. Даны водные растворы: гексагидроксохромата натрия Na3[Cr(OH)6], хлорида](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/361865/slide-8.jpg)
![Составление возможных уравнений реакций C2. Даны водные растворы: гексагидроксоалюмината калия K3[Al(OH)6], хлорида](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/361865/slide-9.jpg)







 Преференции членов СНО
Преференции членов СНО Презентация на тему Профессии бывают разные
Презентация на тему Профессии бывают разные Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности
Ответственность, предусмотренная за нарушение требований трудового права, охраны труда и промышленной безопасности Проблема проекта: Ненадлежащий вид электричек в Москве
Проблема проекта: Ненадлежащий вид электричек в Москве Я и мои права
Я и мои права Лекція 6
Лекція 6 Математика вокруг нас
Математика вокруг нас Афоризмы. Дружба
Афоризмы. Дружба Договор мены
Договор мены Форма государственного правления Российской Федерации
Форма государственного правления Российской Федерации Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества
Битумы (от лат. bitumen горная смола), твердые или смолоподобные продукты. Свойства битумов зависят от способов производства, качества  Ata
Ata Юрий Визбор
Юрий Визбор Презентация на тему Становление личностных характеристик ученика начальной школы
Презентация на тему Становление личностных характеристик ученика начальной школы  Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда
Дизайн проект помещений пилотного центра занятости ГКУ ЦЗН г. Волгограда Still loving you
Still loving you Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1
Особенности электроснабжения обогатительных фабрик. Категории качества электроэнергии. Лекция №1 Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз
Александр Анатольевич Емельянов Кафедра Математических и инструментальных методов экономики (МиИМЭ) Современные аспекты и раз Реконструкция
Реконструкция Римское право
Римское право Город, улица, микрорайон
Город, улица, микрорайон Презентация на тему Перспективы использования интерактивных технологий в учебном процессе
Презентация на тему Перспективы использования интерактивных технологий в учебном процессе О пчелах, колоколах и вечном двигателе
О пчелах, колоколах и вечном двигателе Материнство глазами художников
Материнство глазами художников Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт
Как пополнить электронный кошелек «RBK money» через Интернет-банк Банка Русский Стандарт Особенности построения сибирской избы
Особенности построения сибирской избы Презентация на тему Демографические перспективы
Презентация на тему Демографические перспективы 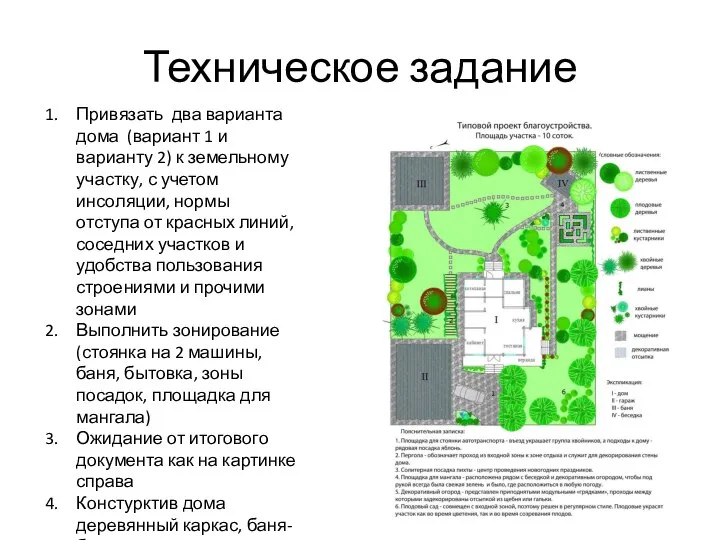 Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку
Техническое задание: привязать два варианта дома (вариант 1 и вариант 2) к земельному участку