Содержание
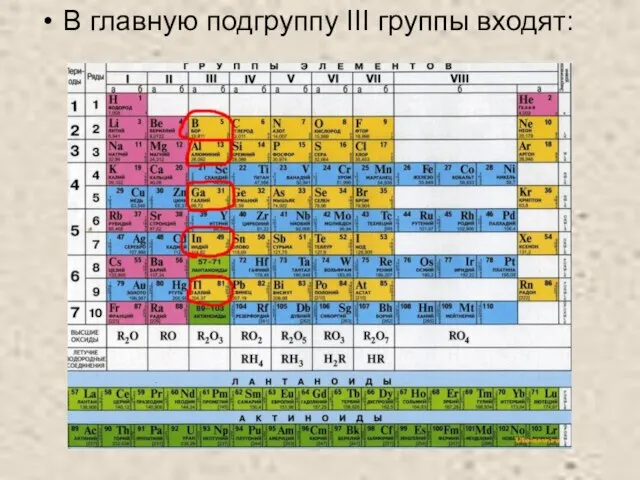
- 2. В главную подгруппу III группы входят:
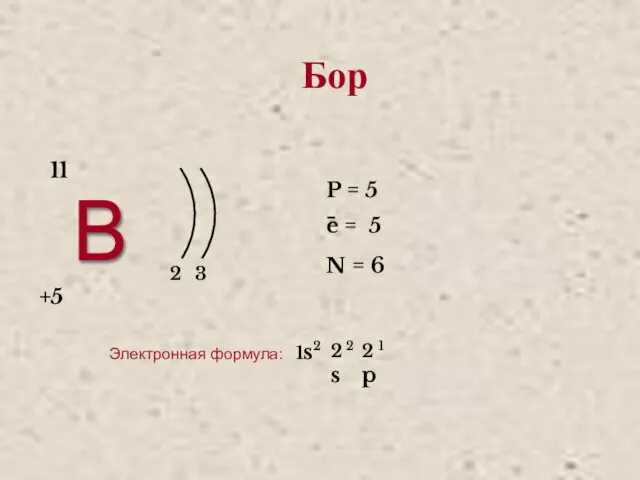
- 3. В 2 3 +5 11 P = 5 e = 5 N = 6 − Электронная
- 4. Алюминий Al 27 +13 0 2 8 3 P = 13 e = 13 N =
- 5. Галлий Ga +31 70 2 8 18 3 P = 31 e = 31 N =
- 6. Индий In 115 +49 8 18 3 18 2 P = 49 e = 49 N
- 7. Таллий − Tl 8 18 32 2 18 3 P = 81 e = 81 N
- 8. Общая характеристика На внешнем электронном уровне элементов главной подгруппы имеется по три электрона (s2р1). Они легко
- 9. Бор Бор (от лат. Borum). В свободном состоянии бор — бесцветное, серое или красное кристаллическое либо
- 10. Алюминий Алюми́ний (от лат. Aluminium)-лёгкий, парамагнитный металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Относится
- 11. Галлий. Га́ллий (от лат. Gallium) мягкий пластичный металл серебристо-белого цвета с синеватым оттенком. Относится к группе
- 12. Индий. И́ндий (от лат. Indium) ковкий, легкоплавкий, очень мягкий металл серебристо-белого цвета. Относится к группе лёгких
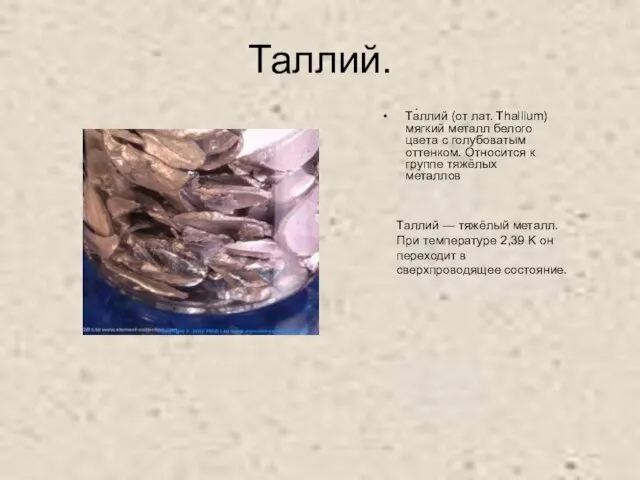
- 13. Таллий. Та́ллий (от лат. Thallium) мягкий металл белого цвета с голубоватым оттенком. Относится к группе тяжёлых
- 14. Применение. Бор
- 15. Применение Алюминий
- 16. Применение. Галлий
- 17. Применение. Индий
- 18. Применение. Таллий
- 19. Химические свойства Легко реагирует с простыми веществами: 1. С кислородом, образуя оксид алюминия: Al + O2
- 20. 2. С галогенами (кроме фтора), образуя хлорид, бромид или иодид алюминия: Al + Cl2 = Задание
- 21. с другими неметаллами реагирует при нагревании: с фтором, образуя фторид алюминия: Al + F2 = Задание
- 22. с серой, образуя сульфид алюминия: 2Al + S = Задание №4 Составьте уравнение реакции, расставьте коэффициенты
- 23. с азотом, образуя нитрид алюминия: 2Al + N = Задание №5 Составьте уравнение реакции, расставьте коэффициенты
- 24. с углеродом, образуя карбид алюминия: Al + 3С = Задание №6 Составьте уравнение реакции, расставьте коэффициенты
- 25. Со сложными веществами: с водой (после удаления защитной оксидной пленки, например, амальгамированием или растворами горячей щёлочи):
- 27. Скачать презентацию





















 Утилизация шлама в оксид магния и карналлит
Утилизация шлама в оксид магния и карналлит Суточный биоритм
Суточный биоритм Тазове передлежання плода: ведення вагітності та пологів
Тазове передлежання плода: ведення вагітності та пологів  Методические рекомендации по работе над творческим проектом
Методические рекомендации по работе над творческим проектом Очистители топливной системы, впускного клапана и распылителя форсунки
Очистители топливной системы, впускного клапана и распылителя форсунки до встречи 1 сентября!
до встречи 1 сентября! Welcome box. Наша история
Welcome box. Наша история Кризисные ситуации и методы их преодоления ( нет подростковому суициду)
Кризисные ситуации и методы их преодоления ( нет подростковому суициду) К ЗВЕЗДАМ !
К ЗВЕЗДАМ ! Итальянская школа Геоэкономики
Итальянская школа Геоэкономики ва
ва Искусство – образная модель мира
Искусство – образная модель мира БИБЛИОТЕКА ГОУ ДПО ПОИПКРО
БИБЛИОТЕКА ГОУ ДПО ПОИПКРО Технические регламенты
Технические регламенты открытая тз (2)
открытая тз (2) Логистическая компания АРЭС
Логистическая компания АРЭС The Incredible Sun
The Incredible Sun  Государственная символика РОССИИ и КБР
Государственная символика РОССИИ и КБР Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей
Презентация на тему Ограниченность ресурсов. Кривая производственных возможностей Растения сада
Растения сада Декоративный натюрморт Коми мотив
Декоративный натюрморт Коми мотив Гидроизоляция блочного фундамента (включая демонтаж)
Гидроизоляция блочного фундамента (включая демонтаж) Моя малая родина – село Красный Яр
Моя малая родина – село Красный Яр Рыцари средневековья
Рыцари средневековья Презентация на тему Теория вероятностей
Презентация на тему Теория вероятностей  Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663
Модуль вывода унифицированных аналоговых сигналов ТПТС55.1663 Mykola Platonovich Bazhan
Mykola Platonovich Bazhan Индукционный нагрев
Индукционный нагрев