Содержание
- 2. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Атомно-молекулярное учение В 1741 г. М.В.Ломоносов впервые высказал предположения
- 3. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Позже, в 1803 г., Дж.Дальтон также приходит к выводу
- 4. Крыжановская Т.Н., СОШ № 12. г. Северодонецк 1. Все вещества состоят из молекул, т.е. химическое соединение
- 5. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Закон постоянства состава вещества (Ж.Л.Пруст, 1799 г.). Качественный и
- 6. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Закон сохранения массы (М.В.Ломоносов, 1748 г., А.Л.Лавуазье, 1789 г.).
- 7. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Закон Авогадро (А.Авогадро, 1811 г., С.Канниццаро, 1858 г.) В
- 8. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Следствия из закона Авогадро: 1) При одинаковых условиях равные
- 9. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Закон эквивалентов (И.В.Рихтер, 1792 г.). Массы веществ, вступающих в
- 10. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Химический эквивалент элемента – такая его масса, которая соединяется
- 11. Крыжановская Т.Н., СОШ № 12. г. Северодонецк На основе закона эквивалентов выведены формулы для расчета эквивалентных
- 12. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Э(кислоты) = молярная масса кислоты /основность кислоты, например: Э(H2SO4)
- 13. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Э(основания) = молярная масса основания/кислотность основания, например: Э(Ca(OH)2) =
- 14. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Э(соли) = молярная масса соли/(валентность металла•число атомов металла), например:
- 15. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Для определения эквивалентной массы элемента необходимо знать состав его
- 16. Крыжановская Т.Н., СОШ № 12. г. Северодонецк При решении задач на вычисление эквивалентных масс необходимо иметь
- 17. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Для вычисления эквивалентной массы кислоты необходимо разделить её мольную
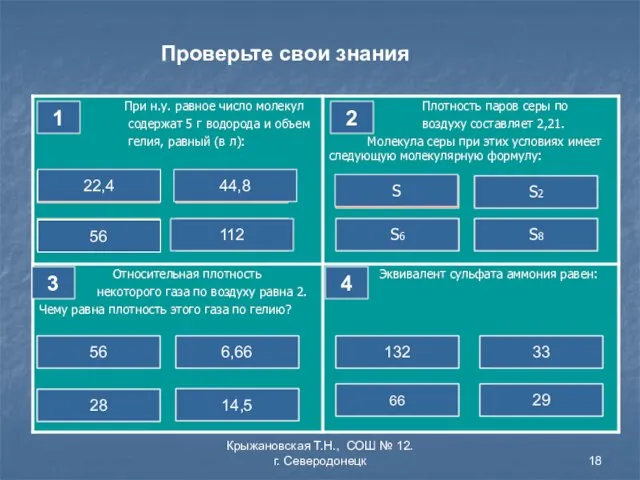
- 18. Крыжановская Т.Н., СОШ № 12. г. Северодонецк Правильно! Ошибка Ошибка Ошибка 1 22,4 44,8 112 56
- 20. Скачать презентацию
















 Презентация к иллюстрациям по мифу Индии Богиня Лакшми Малышевой Анжелики
Презентация к иллюстрациям по мифу Индии Богиня Лакшми Малышевой Анжелики Фернан Магеллан (8 класс)
Фернан Магеллан (8 класс) Речник Карта
Речник Карта Храмовый синтез искусств
Храмовый синтез искусств Маска - модно и безопасно
Маска - модно и безопасно Сочинение-описание внешнего облика героя (по картине Ф.П.Решетникова «Опять двойка!»)
Сочинение-описание внешнего облика героя (по картине Ф.П.Решетникова «Опять двойка!») Презентация на тему Былины. Виды былин. Мир былины
Презентация на тему Былины. Виды былин. Мир былины  Население России. История переписи населения
Население России. История переписи населения Вопросы профилактики суицидального проведения несовершеннолетних (теория)
Вопросы профилактики суицидального проведения несовершеннолетних (теория) История олимпийских игр
История олимпийских игр Архитектура компьютера и характеристики
Архитектура компьютера и характеристики Налоги и налогообложие
Налоги и налогообложие Научная социальная сеть «Crimpravo.ru»
Научная социальная сеть «Crimpravo.ru» Подготовка к ЕГЭ. Полезно знать
Подготовка к ЕГЭ. Полезно знать N … 2s22p3
N … 2s22p3 Готические соборы
Готические соборы Итоги регулирования тарифов на коммунальные ресурсы на 2012 год. Основные цели и задачи РСТ на 2013 год
Итоги регулирования тарифов на коммунальные ресурсы на 2012 год. Основные цели и задачи РСТ на 2013 год Машинное и глубокое обучение для Интернета вещей и тактильного интернета. СПб ГУТ. Магистратура
Машинное и глубокое обучение для Интернета вещей и тактильного интернета. СПб ГУТ. Магистратура Вопросы по учету межбюджетных трансфертов в 2019 году
Вопросы по учету межбюджетных трансфертов в 2019 году «Свежий ветер» (команда ГОУСОШ № 108)
«Свежий ветер» (команда ГОУСОШ № 108) Программадетского объединения«Учимся жить вместе»(по правам человека)Руководитель:Долгина Тамара ГеоргиевнаТомск - 2008 г.
Программадетского объединения«Учимся жить вместе»(по правам человека)Руководитель:Долгина Тамара ГеоргиевнаТомск - 2008 г. Скандий. Характеристики технологии извлечения скандия
Скандий. Характеристики технологии извлечения скандия ПТИЧЬИ ГНЕЗДА
ПТИЧЬИ ГНЕЗДА Кресло Бюрократ CH-400/Black
Кресло Бюрократ CH-400/Black Вёр=ё темипе =ыхённё уроксенче усё курмалли материал
Вёр=ё темипе =ыхённё уроксенче усё курмалли материал Путешествуем по восемнадцати столицам Пермского края. Часть 8
Путешествуем по восемнадцати столицам Пермского края. Часть 8 Люди войны
Люди войны Выделка кожи у алтайцев
Выделка кожи у алтайцев