Содержание
- 2. Как наша прожила б планета? Как люди жили бы на ней Без теплоты, магнита, света И
- 3. Проблемный вопрос. Что произойдёт, если в раствор или расплав электролита опустить электроды, которые присоединены к источнику
- 4. Электролиз – дословно: «лизис» – разложение, «электро» – электрическим током. Цель урока: изучить сущность и применение
- 5. Электролиз – это окислительно- -восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через расплав
- 6. Электролиз План Электролиз расплава. Электролиз раствора. Сущность электролиза. Применение. Выводы.
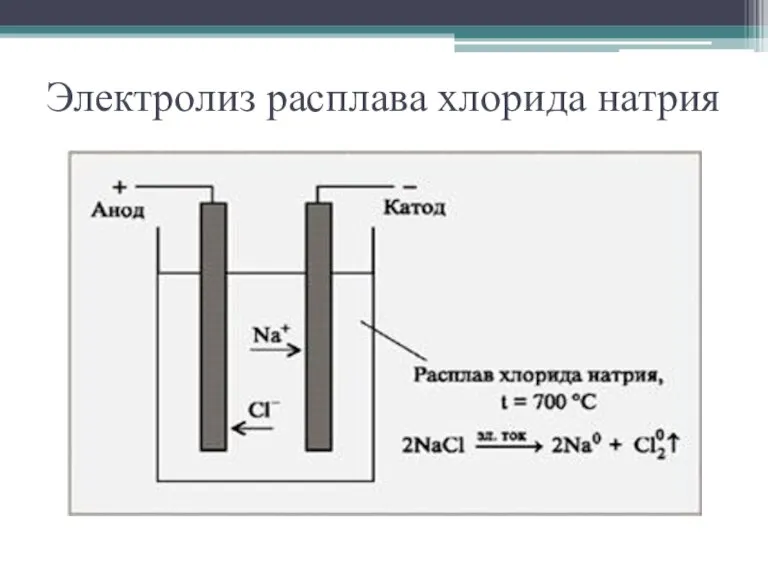
- 7. Электролиз расплава хлорида натрия
- 8. Электролиз является окислительно – - восстановительным процессом: на катоде всегда идёт процесс восстановления, на аноде всегда
- 9. Для определения результатов электролиза водных растворов существуют следующие правила: Процесс на катоде не зависит от материала
- 10. Процесс на аноде зависит от материала анода и от природы аниона. Если анод нерастворимый, т.е. инертный
- 11. Электрическая энергия Химическая энергия Электролиз Раствор NaCl Катод(-) Анод(+) H2О Расплав NaCl Катод(-) Анод(+) Na+ +
- 12. Работа с учебником (стр. 109-110) Проанализируйте процесс электролиза водного раствора сульфата натрия. Используя инструкции, запишите катодный
- 13. Сущность электролиза состоит в том, что за счёт электрической энергии осуществляется химическая реакция, которая не может
- 14. Внимательно наблюдайте за результатами электролиза сульфата меди. 1. Запишите катодный и анодный процессы, суммарное уравнение процесса.
- 15. Проверь себя! CuSO4 → Cu2+ + SO42- H2O Катод (-) Cu2+ SO42- Анод (+) Cu2+ +
- 16. Применение электролиза Катодные процессы Анодные процессы В гальваностегии ( никелирование, серебрение). В гальванопластике (изготовление копий). Получение
- 17. Гальванопластика политехнического государственного музея «Георгий Победоносец» Барельеф «Портрет Б.С.Якоби»
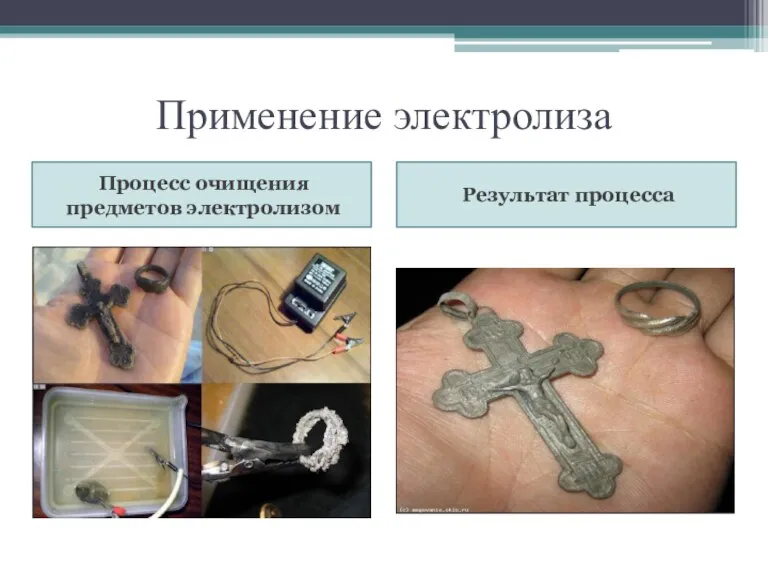
- 18. Применение электролиза Процесс очищения предметов электролизом Результат процесса
- 19. Установите правильную последовательность. окислительно-восстановительные реакции если через раствор или расплав Электролиз – это протекающие на электродах
- 20. Ответьте на вопросы. 1. При электролизе к аноду движутся: а) катионы б) анионы в) все ионы
- 21. Рефлексия. Если вы согласны с утверждениями, поставьте плюс, а если нет, то минус. 1. Я узнал
- 22. Домашнее задание Записи в тетради. Учебник «Химия – 10», стр. 107 - 111 (читать). Выполнить упр.
- 24. Скачать презентацию



















 Презентация на тему Инструктаж по поведению на льду
Презентация на тему Инструктаж по поведению на льду  Документознавство
Документознавство Союз промышленников и предпринимателей Санкт – Петербурга.Обзор основных направленийработы.
Союз промышленников и предпринимателей Санкт – Петербурга.Обзор основных направленийработы. Презентация на тему Сербия
Презентация на тему Сербия  Русская матрёшка
Русская матрёшка Жизнь и творчество И.С. Тургенева (1818 – 1883)
Жизнь и творчество И.С. Тургенева (1818 – 1883) Щелкни здесь
Щелкни здесь СХЕМА САЙТА
СХЕМА САЙТА Виды и свойства текстильных материалов из химических волокон
Виды и свойства текстильных материалов из химических волокон Семейные каникулы 2022 Конкурс
Семейные каникулы 2022 Конкурс Электронная почта
Электронная почта Управление деятельностью предприятия трубопроводного транспорта нефти с применением системы сбалансированных показателей
Управление деятельностью предприятия трубопроводного транспорта нефти с применением системы сбалансированных показателей Пример 2 (процедура принятия решений)
Пример 2 (процедура принятия решений) Отчетность НОБ. Порядок учета работы ОКР ТК и предоставление отчетов
Отчетность НОБ. Порядок учета работы ОКР ТК и предоставление отчетов Feste in Osterreich
Feste in Osterreich Ходаки. Отчет группы
Ходаки. Отчет группы Факультет «МОСТЫ и ТОННЕЛИ» ФГОУ ВПО ПГУПС свою основную научно-техническую деятельность ведет в области осуществления различны
Факультет «МОСТЫ и ТОННЕЛИ» ФГОУ ВПО ПГУПС свою основную научно-техническую деятельность ведет в области осуществления различны Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Научное общество учащихся (НОУ) «Мысль»
Научное общество учащихся (НОУ) «Мысль» Презентация на тему Типы экологических взаимодействий
Презентация на тему Типы экологических взаимодействий  Удивительный мир симметрии
Удивительный мир симметрии Химическое оружие и его поражающие свойства
Химическое оружие и его поражающие свойства Решение вопросов местного значения Костомукшского городского округа
Решение вопросов местного значения Костомукшского городского округа По литературным местам Гаврилов-Ямского района
По литературным местам Гаврилов-Ямского района Витамины укрепляют организм
Витамины укрепляют организм Урок-КВН по творчеству Н. А. Некрасова
Урок-КВН по творчеству Н. А. Некрасова Рефлексивный анализ Чтений-2008 под углом зрения понятия «практики методологии»Вячеслав Марача –
Рефлексивный анализ Чтений-2008 под углом зрения понятия «практики методологии»Вячеслав Марача –  Материалы для дистанционной поддержки учащихся по дополнительной программе Мечты в красках. Город в технике граттаж
Материалы для дистанционной поддержки учащихся по дополнительной программе Мечты в красках. Город в технике граттаж