Содержание
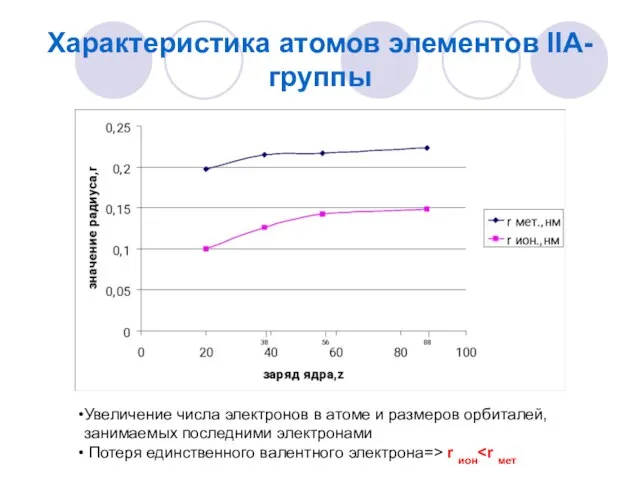
- 2. Характеристика атомов элементов IIA-группы Увеличение числа электронов в атоме и размеров орбиталей, занимаемых последними электронами Потеря
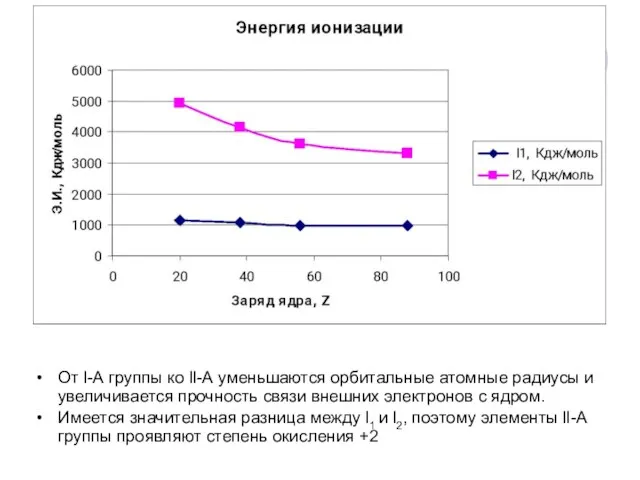
- 3. От l-А группы ко ll-А уменьшаются орбитальные атомные радиусы и увеличивается прочность связи внешних электронов с
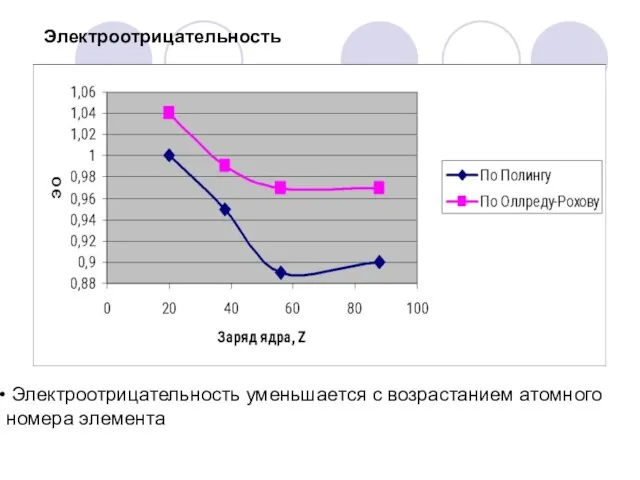
- 4. Электроотрицательность Электроотрицательность уменьшается с возрастанием атомного номера элемента
- 5. Особенности химии бериллия Ион Be2+ устойчив лишь в газовой фазе при высокой температуре Химическая связь в
- 6. В чистом виде Be, Mg и щелочноземельные металлы имеют серебристо-белый цвет. Все металлы, кроме Be, очень
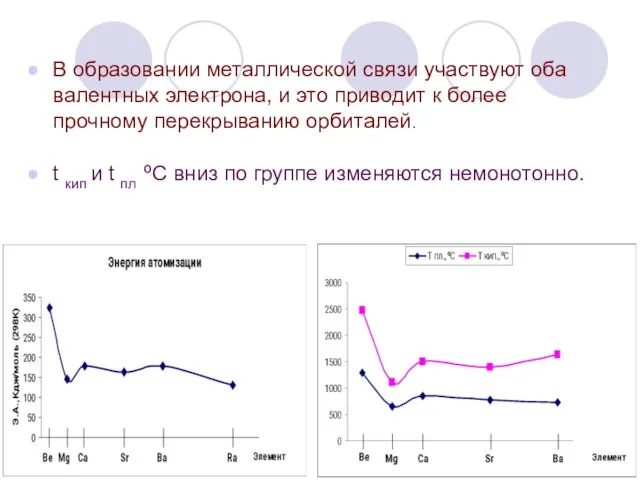
- 7. В образовании металлической связи участвуют оба валентных электрона, и это приводит к более прочному перекрыванию орбиталей.
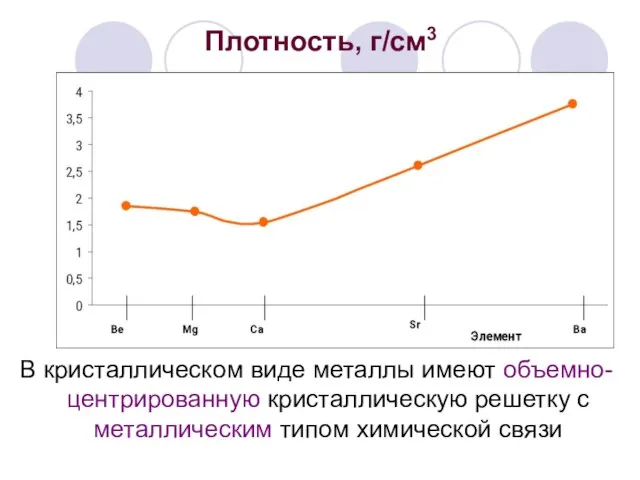
- 8. Плотность, г/см3 В кристаллическом виде металлы имеют объемно-центрированную кристаллическую решетку с металлическим типом химической связи
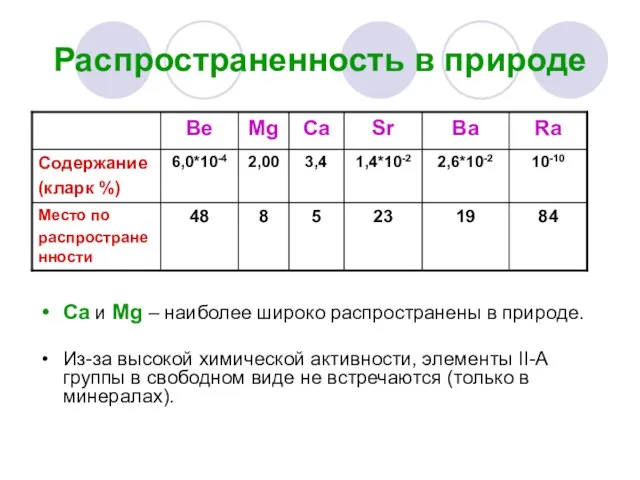
- 9. Распространенность в природе Ca и Mg – наиболее широко распространены в природе. Из-за высокой химической активности,
- 10. Минералы 2MgO*SiO2 (оливин) 3MgO*4SiO2*4H2O (тальк)
- 11. CaCO3 кальцит (известняк, мрамор, мел) SrSO4 (целестин)
- 12. BaSO4 (барит)
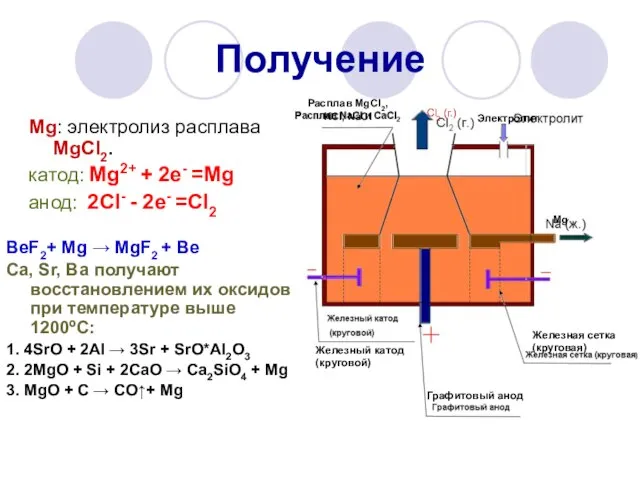
- 13. Получение Расплав MgCl2, KCl, NaCl Cl2 (г.) Электролит Железный катод (круговой) Графитовый анод Железная сетка (круговая)
- 14. Применение Be и его сплавы применяются в самолето- и ракетостроении, ядерной энергетике. Mg и его сплавы
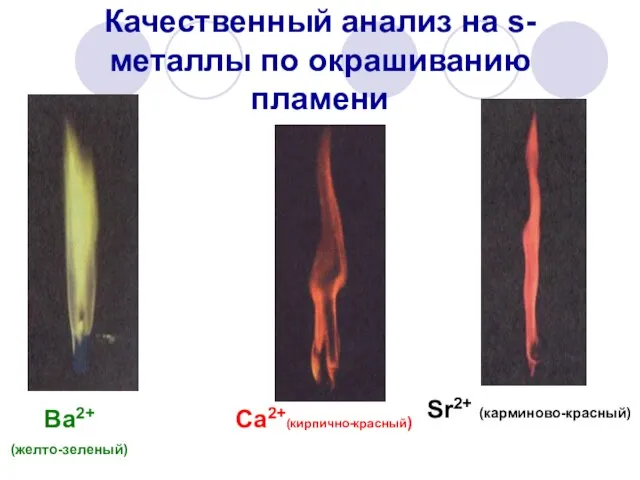
- 15. Качественный анализ на s-металлы по окрашиванию пламени Ba2+ (желто-зеленый) Ca2+(кирпично-красный) Sr2+ (карминово-красный)
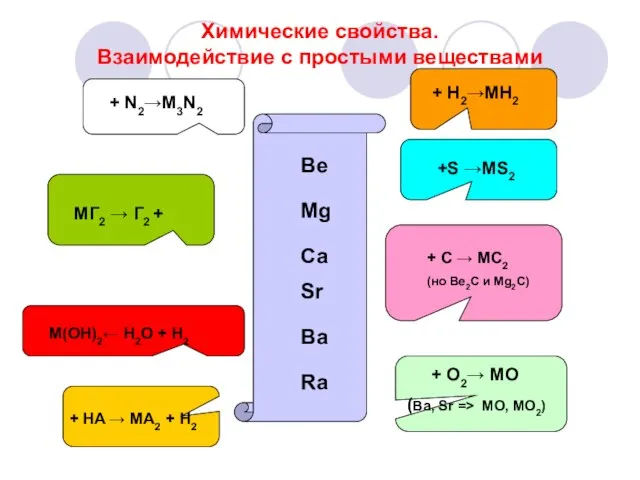
- 16. Химические свойства. Взаимодействие с простыми веществами Be Mg Ca Sr Ba Ra + H2→MH2 +S →MS2
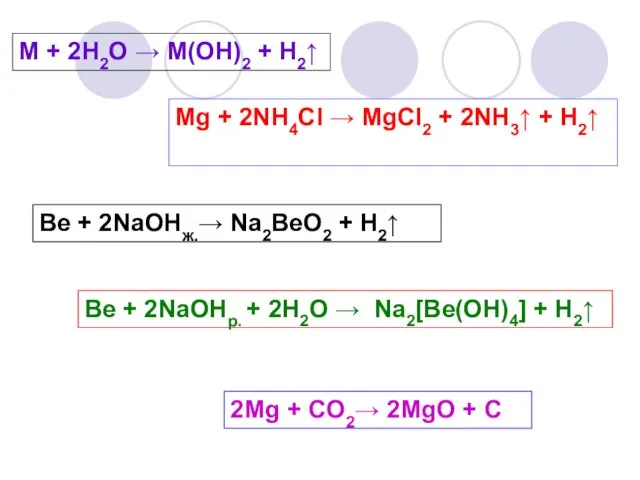
- 17. M + 2H2O → M(OH)2 + H2↑ Mg + 2NH4Cl → MgCl2 + 2NH3↑ + H2↑
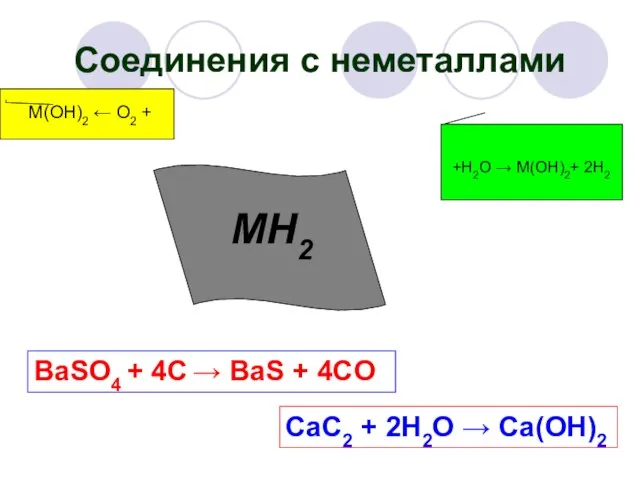
- 18. Соединения с неметаллами MH2 M(OH)2 ← O2 + +H2O → M(OH)2+ 2H2 BaSO4 + 4C →
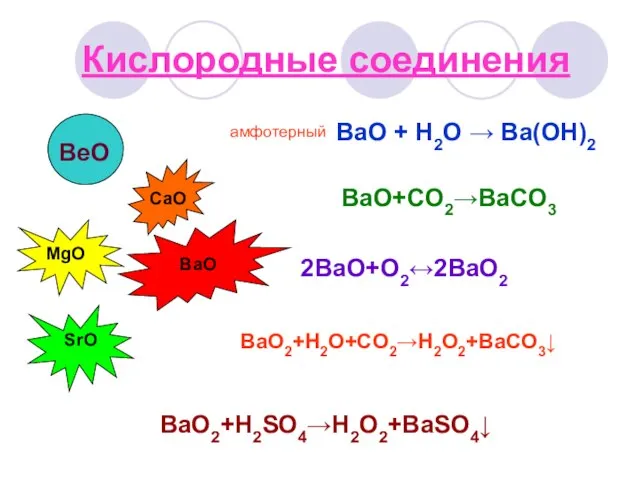
- 19. Кислородные соединения BeO амфотерный MgO CaO SrO BaO BaO + H2O → Ba(OH)2 BaO+CO2→BaCO3 2BaO+O2↔2BaO2 BaO2+H2O+CO2→H2O2+BaCO3↓
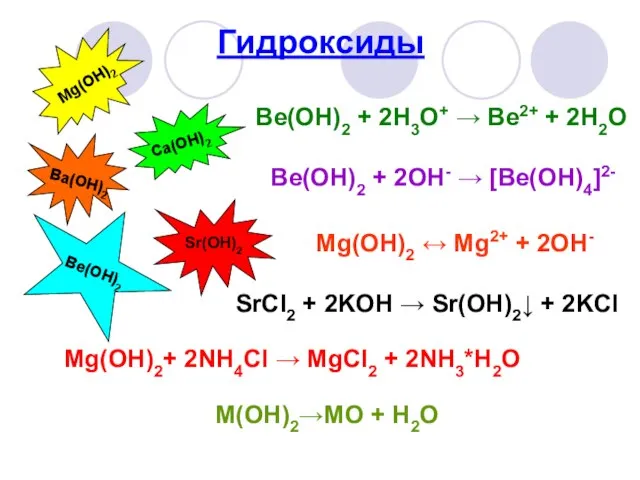
- 20. Гидроксиды Mg(OH)2 Ca(OH)2 Sr(OH)2 Ba(OH)2 Be(OH)2 Be(OH)2 + 2H3O+ → Be2+ + 2H2O Be(OH)2 + 2OH-
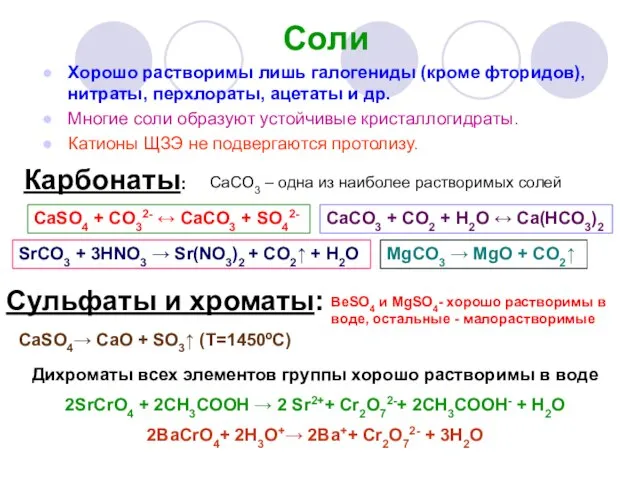
- 21. Хорошо растворимы лишь галогениды (кроме фторидов), нитраты, перхлораты, ацетаты и др. Многие соли образуют устойчивые кристаллогидраты.
- 22. Нитраты Ba(NO3)2 кристаллизуется в безводном состоянии Остальные соли образуют кристаллогидраты 2Mg(NO3)2→ 2MgO + 4NO2 + O2
- 23. Образование комплексных соединений более характерно, чем для щелочных металлов. В водном растворе Be входит в состав
- 24. Элементы II-А группы содержат на внешнем энергетическом уровне два электрона. Вниз по группе радиус атомов растет,
- 26. Скачать презентацию









 Корейская война
Корейская война Святослав Игоревич – Великий полководец древней Руси.
Святослав Игоревич – Великий полководец древней Руси. Материнская плата
Материнская плата Предприятие EcoCorp
Предприятие EcoCorp БАЗЫ ДАННЫХ
БАЗЫ ДАННЫХ Авторы: Вабищевич Мария Владимировна, учитель химии МОУСОШ № 37 г. Шахты
Авторы: Вабищевич Мария Владимировна, учитель химии МОУСОШ № 37 г. Шахты Живая память
Живая память Coffeе-art Сладкая фантазия
Coffeе-art Сладкая фантазия Живи здраво (о ВИЧ и не только)
Живи здраво (о ВИЧ и не только) Смеситель металлический
Смеситель металлический Order Letter
Order Letter Изменения в налоговом законодательстве осенняя сессия 2011 г.
Изменения в налоговом законодательстве осенняя сессия 2011 г. «Принципы и направления развития таможенных органов.» Работу выполнили студентки 1-го курса ФТД группы Т-116 Сафонова Эллина и Панк
«Принципы и направления развития таможенных органов.» Работу выполнили студентки 1-го курса ФТД группы Т-116 Сафонова Эллина и Панк Как опубликовать сообщение в блоге
Как опубликовать сообщение в блоге Искусство графики
Искусство графики Свойства нервной системы в профессиональной деятельности
Свойства нервной системы в профессиональной деятельности Ядерная сделка с Ираном
Ядерная сделка с Ираном Русская народная одежда
Русская народная одежда Описание предмета Городецкая роспись
Описание предмета Городецкая роспись Minsk. Capitale de Bielorussie
Minsk. Capitale de Bielorussie Пейзажная лирика Ф.И.Тютчева
Пейзажная лирика Ф.И.Тютчева Презентация на тему Профилактика ВИЧ и СПИД
Презентация на тему Профилактика ВИЧ и СПИД Защита зоны электродуговой сварки от окисления
Защита зоны электродуговой сварки от окисления Театральное искусство XVII – XVIII вв
Театральное искусство XVII – XVIII вв Колебания и волны
Колебания и волны Бизнес инсайт. Продвижение бренда при нулевом бюджете
Бизнес инсайт. Продвижение бренда при нулевом бюджете Формирование Совета Федерации
Формирование Совета Федерации AL-1035WH - - Произведение Искусств
AL-1035WH - - Произведение Искусств