Слайд 2Цели урока:
организовать деятельность учащихся по изучению особенностей строения атома фосфора на основании

его положения в ПСХЭ Д.Менделеева
выяснить аллотропные возможности фосфора
изучить химические свойства фосфора как простого вещества на основе его строения
развивать познавательную самостоятельность учащихся при работе с учебником, дополнительной литературой, сайтами Интернета
формировать умения составления химических уравнений на основе химического эксперимента, навыки решения расчетных задач
воспитывать ответственность за конечный результат работы.
Слайд 3
Мотивационно-ориентационный этап.
Академик А.Е.Ферсман назвал этот элемент « элементом мысли и

жизни», без него невозможно существование на Земле живого, в теле человека его примерно 0,8 кг. Он - основа нервных, мышечных, мозговых и костных тканей. Является жителем V-A подгруппы периодической системы химических элементов Д.И.Менделеева. О каком элементе идет речь?
Слайд 4Какие сведения о фосфоре вам были известны до сегодняшнего урока?
ФОСФОР
Слайд 5История открытия фосфора
1669 г- Х.Бранд-первооткрыватель
фосфора
1682г- Р.Бойль в химической

лаборатории при работе с фосфором.
Слайд 7
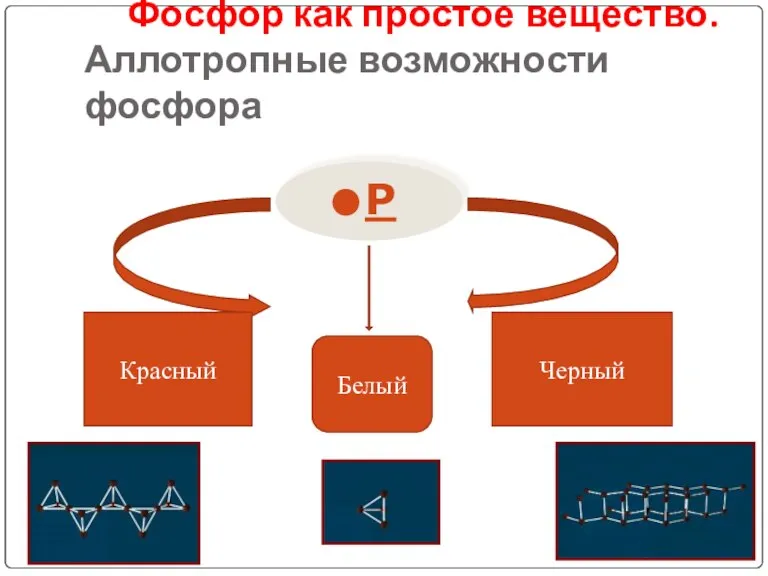
Фосфор как простое вещество. Аллотропные возможности фосфора
Р
Красный
Белый
Черный
Слайд 9Прокомментируйте отрывок из романа А.Конан-Дойля « Собака Баскервилей». Попытайте определить, где правда,

а где вымысел автора?
«...Да! Это была собака, огромная, черная, как смоль. Но такой собаки еще никто из нас, смертных, не видывал. Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь .Ее огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте. - Фосфор, – сказал я».
Слайд 10Химические свойства фосфора.
( Работа с учебником стр.160 и дополнительной литературой)

Слайд 11« Сжигание красного фосфора и исследование продуктов его сгорания»

Слайд 12Видеоролик
«Сгорание фосфора в хлоре»
2 Р + 3Cl2 ( нед) →2 PCI3
2
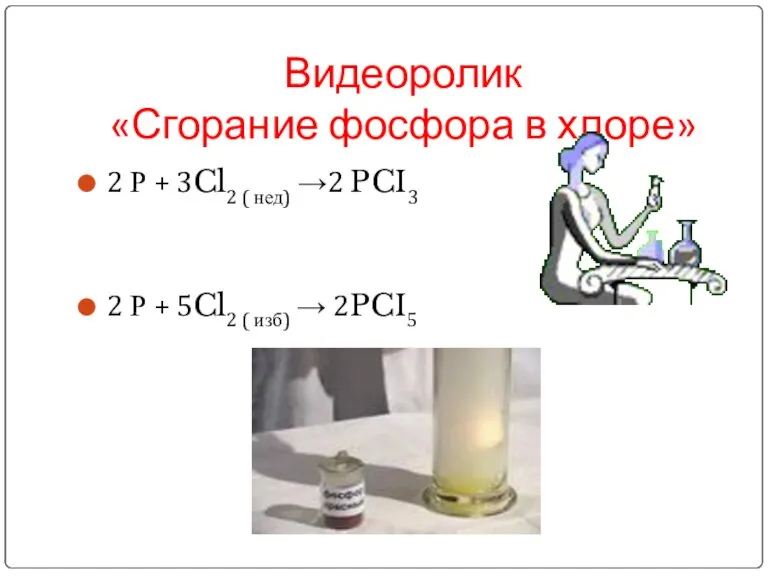
Р + 5Cl2 ( изб) → 2PCI5
Слайд 14Первичное закрепление полученных знаний.
Учащиеся выбирают для закрепления материала задания разных уровней сложности:
1

уровень: упр. №1 стр. 163 учебника ( О.С.Габриелян, «Химия-9»)
2 уровень:упр.№2 стр. 163 учебника
3 уровень: решение расчетной задачи №5 стр.163 учебника.
Слайд 15Домашнее задание:
п.28 ( до стр.160- соединения фосфора), упр.№3,6 ( по выбору

учащихся); творческое задание: презентация темы « Биологическое значение фосфора».
Слайд 16Итоги урока. Рефлексивно- оценочный этап.
Рефлексия « Телеграмма» ученика учителю о впечатлениях об

уроке.
















 План маркетинга. Цена
План маркетинга. Цена "Тема и поэтическая идея стихотворения А. С. Пушкина "Зимнее утро."
"Тема и поэтическая идея стихотворения А. С. Пушкина "Зимнее утро." Новогодний Маскарад!
Новогодний Маскарад! Обзор технологий и решений PeerApp
Обзор технологий и решений PeerApp The five senses
The five senses Как размножаются живые организмы
Как размножаются живые организмы Орнамент. Новогодняя открытка
Орнамент. Новогодняя открытка День Победы!
День Победы! Соблюдение работниками профессиональной и служебной этики, морально-этических норм при проведении экзамена
Соблюдение работниками профессиональной и служебной этики, морально-этических норм при проведении экзамена Юморина
Юморина Places
Places ДОСУГШКОЛЬНИКОВ
ДОСУГШКОЛЬНИКОВ о вреде алкоголя
о вреде алкоголя Детский писатель Борис Заходер
Детский писатель Борис Заходер Конференция «Бизнес и этика»
Конференция «Бизнес и этика» …и долго буду тем любезен я народу, что чувства добрые я лирой пробуждал, что в мой жестокий век восславил я свободу и милость к пад
…и долго буду тем любезен я народу, что чувства добрые я лирой пробуждал, что в мой жестокий век восславил я свободу и милость к пад Викторина: Знаете ли вы зимние виды спорта?
Викторина: Знаете ли вы зимние виды спорта? Рекламное агентство Профиль, Нижний Новгород Агентство возникло не так давно, тем не менее, имеет хороший потенциал развития, что
Рекламное агентство Профиль, Нижний Новгород Агентство возникло не так давно, тем не менее, имеет хороший потенциал развития, что  " Пресс-Центр"
" Пресс-Центр" Обзор ситуации со стандартами НАПФ в свете изменения законодательства
Обзор ситуации со стандартами НАПФ в свете изменения законодательства Основы экстренной психологической помощи
Основы экстренной психологической помощи Per aspera ad Astra - Через тернии - к звёздам
Per aspera ad Astra - Через тернии - к звёздам Презентация на тему Файлы и папки
Презентация на тему Файлы и папки  Физические лица
Физические лица Занятия в школе ИнтелектУм
Занятия в школе ИнтелектУм Методические решения по индексированию документов:классы 2 и 9
Методические решения по индексированию документов:классы 2 и 9 Предоставление государственной услуги по выплате компенсации, взимаемой с родителей за содержание в образовательных учреждениях
Предоставление государственной услуги по выплате компенсации, взимаемой с родителей за содержание в образовательных учреждениях Делимость чисел
Делимость чисел